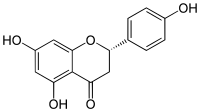
Naringenina - Naringenin
|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
(2 S ) -4 ′, 5,7-Trihidroxiflavan-4-ona
|
|
|
Nombre IUPAC preferido
(2 S ) -5,7-Dihidroxi-2- (4-hidroxifenil) -2,3-dihidro- 4H -1-benzopiran-4-ona |
|
| Otros nombres
Naringetol; Salipurol; Salipurpol
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Tarjeta de información ECHA |
100.006.865 |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 15 H 12 O 5 | |
| Masa molar | 272,256 g · mol −1 |
| Punto de fusion | 251 ° C (484 ° F; 524 K) |
| 475 mg / L | |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
La naringenina es una flavanona incolora y sin sabor , un tipo de flavonoide . Es la flavanona predominante en la toronja y se encuentra en una variedad de frutas y hierbas.
Estructura
La naringenina tiene la estructura esquelética de una flavanona con tres grupos hidroxi en los carbonos 4 ', 5 y 7. Se puede encontrar tanto en forma de aglicol , naringenina, como en su forma glicosídica , naringina , que tiene la adición del disacárido neohesperidosa unido a través de un enlace glicosídico en el carbono 7.
Como la mayoría de las flavanonas, la naringenina tiene un solo centro quiral en el carbono 2, aunque la pureza óptica es variable. Se ha demostrado que la racemización de S (-) - naringenina ocurre con bastante rapidez.
Fuentes y biodisponibilidad
La naringenina y su glucósido se han encontrado en una variedad de hierbas y frutas , que incluyen pomelo , bergamota , naranja agria , cerezas ácidas , tomates , cacao , orégano griego , menta acuática y frijoles . Las proporciones de naringenina a naringina varían entre las fuentes, al igual que las proporciones enantioméricas.
La forma de naringenina-7-glucósido parece menos biodisponible que la forma de aglicol .
El jugo de toronja puede proporcionar concentraciones plasmáticas de naringenina mucho más altas que el jugo de naranja. También se encuentra en la toronja el compuesto relacionado kaempferol , que tiene un grupo hidroxilo junto al grupo cetona.
La naringenina se puede absorber de la pasta de tomate cocida. Hay 3,8 mg de naringenina en 150 gramos de pasta de tomate.
Biosíntesis y metabolismo
Se deriva de malonil CoA y 4-cumaroil CoA . Este último se deriva de la fenilalanina . La chalcona sintasa actúa sobre el tetraketido resultante para dar la chalcona que luego sufre un cierre de anillo a naringenina.
La enzima naringenina 8-dimetilaliltransferasa utiliza dimetilalil difosfato y (-) - (2 S ) -naringenina para producir difosfato y 8-prenilnaringenina . Cunninghamella elegans , un organismo modelo fúngico del metabolismo de los mamíferos, se puede utilizar para estudiar la sulfatación de naringenina .
Efectos biológicos potenciales
Enfermedad de Alzheimer
La naringenina se está investigando como un tratamiento potencial para la enfermedad de Alzheimer . Se ha demostrado que la naringenina mejora la memoria y reduce las proteínas amiloides y tau en un estudio que utilizó un modelo de ratón de la enfermedad de Alzheimer. Se cree que el efecto se debe a una proteína presente en las neuronas conocida como CRMP2 a la que se une la naringenina.
Antibacteriano, antifúngico y antiviral.
La naringenina tiene un efecto antimicrobiano en S. epidermidis , así como Staphylococcus aureus , Bacillus subtilis , Micrococcus luteus , y Escherichia coli . La investigación adicional ha añadido evidencia de los efectos antimicrobianos contra Lactococcus lactis , Lactobacillus acidophilus , Actinomyces naeslundii , oralis Prevotella , melaninogencia Prevotella , Porphyromonas gingivalis , así como levaduras tales como Candida albicans , Candida tropicalis , y Candida krusei . También hay evidencia de efectos antibacterianos sobre H. pylori , aunque no se ha demostrado que la naringenina tenga ninguna inhibición sobre la actividad ureasa del microbio.
También se ha demostrado que la naringenina reduce la producción del virus de la hepatitis C por los hepatocitos infectados (células del hígado) en cultivos celulares . Esto parece ser secundario a la capacidad de la naringenina para inhibir la secreción de lipoproteínas de muy baja densidad por parte de las células. Los efectos antivirales de la naringenina se encuentran actualmente bajo investigación clínica. También se han realizado informes de efectos antivirales sobre poliovirus , HSV-1 y HSV-2 , aunque no se ha inhibido la replicación de los virus. En experimentos in vitro, Naringenin también mostró una fuerte actividad antiviral contra el SARS-CoV-2.
Antiinflamatorio
A pesar de la evidencia de actividad antiinflamatoria de la naringina, se ha observado que la actividad antiinflamatoria de la naringenina es de escasa a inexistente.
Antioxidante
Se ha demostrado que la naringenina tiene importantes propiedades antioxidantes . Se ha demostrado que reduce el daño oxidativo al ADN in vitro y en estudios con animales.
Anticáncer
Se ha informado que la naringenina ha inducido citotoxicidad en células cancerosas de tejidos de mama , estómago , hígado , cuello uterino , páncreas y colon , junto con células leucémicas . Se han examinado los mecanismos detrás de la inhibición del crecimiento del carcinoma de mama humano y se han propuesto dos teorías. La primera teoría es que la naringenina inhibe la aromatasa , reduciendo así el crecimiento del tumor. El segundo mecanismo propone que las interacciones con los receptores de estrógenos son la causa de la modulación del crecimiento. Se encontró que los nuevos derivados de la naringenina son activos contra el cáncer multirresistente.
Lectura adicional
- efecto inhibidor sobre la isoforma CYP1A2 del citocromo P450 humano, lo que resulta en carcinógenos de sustancias que de otro modo serían inofensivas. Fuhr U, Klittich K, Staib AH (abril de 1993). "Efecto inhibidor del jugo de toronja y su principal amargo, naringenina, sobre el metabolismo dependiente de CYP1A2 de la cafeína en el hombre" . Br J Clin Pharmacol . 35 (4): 431–6. doi : 10.1111 / j.1365-2125.1993.tb04162.x . PMC 1381556 . PMID 8485024 .Ueng YF, Chang YL, Oda Y, Park SS, Liao JF, Lin MF, Chen CF (1999). "Efectos in vitro e in vivo de la naringina sobre la monooxigenasa dependiente del citocromo P450 en hígado de ratón". Life Sci . 65 (24): 2591–602. doi : 10.1016 / s0024-3205 (99) 00528-7 . PMID 10619367 .
- Wistuba, Dorothee; Trapp, Oliver; Gel-Moreto, Nuria; Galensa, Rudolf; Schurig, Volker (1 de mayo de 2006). "Separación estereoisomérica de flavanonas y flavanona-7-O-glucósidos por electroforesis capilar y determinación de barreras de interconversión". Química analítica . 78 (10): 3424–3433. doi : 10.1021 / ac0600499 . ISSN 0003-2700 . PMID 16689546 .
- Krause, Martin; Galensa, Rudolf (1991). "Cromatografía líquida de alto rendimiento de glucósidos de flavanona diastereoméricos en cítricos en una fase estacionaria unida a β-ciclodextrina (Cyclobond I)". Journal of Chromatography A . 588 (1–2): 41–45. doi : 10.1016 / 0021-9673 (91) 85005-z .
- Gaggeri, Raffaella; Rossi, Daniela; Collina, Simona; Mannucci, Barbara; Baierl, Marcel; Juza, Markus (12 de agosto de 2011). "Desarrollo rápido de una separación por cromatografía líquida de alto rendimiento enantioselectiva analítica y escalamiento preparativo para el flavonoide Naringenina". Journal of Chromatography A . 1218 (32): 5414–5422. doi : 10.1016 / j.chroma.2011.02.038 . PMID 21397238 .
- Wan, Lili; Sun, Xipeng; Li, Yan; Yu, Qi; Guo, Cheng; Wang, Xiangwei (1 de abril de 2011). "Un método de HPLC estereoespecífico y su aplicación en la determinación del perfil farmacocinético de dos enantiómeros de naringenina en ratas" . Revista de ciencia cromatográfica . 49 (4): 316-320. doi : 10.1093 / chrsci / 49.4.316 . ISSN 0021-9665 . PMID 21439124 .
- La naringenina también produce efectos similares a los antidepresivos dependientes de BDNF en ratones. Yi LT, Liu BB, Li J, Luo L, Liu Q, Geng D, Tang Y, Xia Y, Wu D (octubre de 2013). "La señalización de BDNF es necesaria para el efecto antidepresivo de la naringenina". Prog. Neuropsychopharmacol. Biol. Psiquiatría . 48C : 135-141. doi : 10.1016 / j.pnpbp.2013.10.002 . PMID 24121063 . S2CID 24620048 .
- Gao, K; Henning, S; Niu, Y; Youssefian, A; Seeram, N; Xu, A; Heber, D (2006). "El flavonoide cítrico naringenina estimula la reparación del ADN en las células del cáncer de próstata". La Revista de Bioquímica Nutricional . 17 (2): 89–95. doi : 10.1016 / j.jnutbio.2005.05.009 . PMID 16111881 .
- Katavic PL, Lamb K, Navarro H, Prisinzano TE (agosto de 2007). "Flavonoides como ligandos del receptor de opioides: identificación y relaciones preliminares estructura-actividad" . J. Nat. Prod . 70 (8): 1278–82. doi : 10.1021 / np070194x . PMC 2265593 . PMID 17685652 .
- Se ha informado que la naringenina induce apoptosis en preadipocitos . Hsu, Chin-Lin; Huang, Shih-Li; Yen, Gow-Chin (1 de junio de 2006). "Efecto inhibidor de los ácidos fenólicos sobre la proliferación de preadipocitos 3T3-L1 en relación con su actividad antioxidante". Revista de Química Agrícola y Alimentaria . 54 (12): 4191–4197. doi : 10.1021 / jf0609882 . ISSN 0021-8561 . PMID 16756346 .
- La naringenina parece proteger a los ratones con deficiencia de LDLR de los efectos sobre la obesidad de una dieta rica en grasas. Mulvihill EE, Allister EM, Sutherland BG, Telford DE, Sawyez CG, Edwards JY, Markle JM, Hegele RA, Huff MW (octubre de 2009). "La naringenina previene la dislipidemia, la sobreproducción de apolipoproteína B y la hiperinsulinemia en ratones sin receptor de LDL con resistencia a la insulina inducida por la dieta" . Diabetes . 58 (10): 2198–210. doi : 10.2337 / db09-0634 . PMC 2750228 . PMID 19592617 .
- La naringenina reduce las concentraciones de colesterol plasmático y hepático al suprimir la HMG-CoA reductasa y ACAT en ratas alimentadas con una dieta alta en colesterol. Lee SH, Park YB, Bae KH, Bok SH, Kwon YK, Lee ES, Choi MS (1999). "Actividad reductora de colesterol de la naringenina mediante la inhibición de la 3-hidroxi-3-metilglutaril coenzima A reductasa y acil coenzima A: colesterol aciltransferasa en ratas". Ana. Nutr. Metab . 43 (3): 173–80. doi : 10.1159 / 000012783 . PMID 10545673 . S2CID 5685548 .
- Se ha demostrado que la naringenina mejora la memoria y reduce las proteínas amiloides y tau en un estudio que utilizó un modelo de ratón de la enfermedad de Alzheimer. Ghofraniab, Saeed; Joghataei, Mohammad-Taghi; Mohsenia, Simin; Baluchnejadmojaradd, Tourandokht; Bagheriac, Maryam; Khamsee, Safoura; Roghani, Mehrdad (5 de octubre de 2015). "Naringenin mejora el aprendizaje y la memoria en un modelo de rata con enfermedad de Alzheimer: información sobre los mecanismos subyacentes" . Revista europea de farmacología . 764 : 195-201. doi : 10.1016 / j.ejphar.2015.07.001 . PMID 26148826 .Yang, Zhiyou; Kuboyama, Tomoharu; Tohda, Chihiro (15 de febrero de 2019). "Naringenin promueve la polarización M2 microglial y la expresión de la enzima de degradación Aβ". Investigación en Fitoterapia . 33 (4): 1114-1121. doi : 10.1002 / ptr.6305 . ISSN 1099-1573 . PMID 30768735 .Yang, Zhiyou; Kuboyama, Tomoharu; Tohda, Chihiro (19 de junio de 2017). "Una estrategia sistemática para descubrir un fármaco terapéutico para la enfermedad de Alzheimer y su molécula diana" . Fronteras en farmacología . 8 : 340. doi : 10.3389 / fphar.2017.00340 . PMC 5474478 . PMID 28674493 .
