NADPH oxidasa - NADPH oxidase
| NAD (P) H oxidasa | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| CE no. | 1.6.3.1 | ||||||||
| No CAS. | 77106-92-4 | ||||||||
| Bases de datos | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| FÁCIL | NiceZyme vista | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | camino metabólico | ||||||||
| PRIAM | perfil | ||||||||
| Estructuras PDB | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
| Reductasa férrica | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | NADPH oxidasa | ||||||||
| Pfam | PF01794 | ||||||||
| InterPro | IPR013130 | ||||||||
| TCDB | 5.B.1 | ||||||||
| Superfamilia OPM | 464 | ||||||||
| Proteína OPM | 5o05 | ||||||||
| |||||||||
NADPH oxidasa (nicotinamida adenina dinucleótido fosfato oxidasa) es uncomplejo enzimático unido a la membranaque se enfrenta al espacio extracelular. Se puede encontrar en la membrana plasmática, así como en las membranas de los fagosomas que utilizanlos glóbulos blancos neutrófilos para engullir los microorganismos. Las isoformas humanasdel componente catalítico del complejo incluyen NOX1 , NOX2 , NOX3 , NOX4 , NOX5 , DUOX1 y DUOX2 .
Reacción
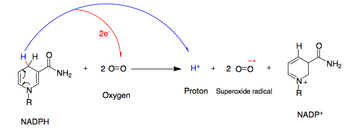
La NADPH oxidasa cataliza la producción de un radical libre superóxido transfiriendo un electrón al oxígeno del NADPH . Durante este proceso, el O 2 se transporta desde el espacio extracelular al interior de la célula y se exporta el H + .
- NADPH + 2O 2 ↔ NADP + + 2O 2 - + H +
Función biológica
Las oxidasas NADPH (NOX) son una de las principales fuentes de especies de oxígeno reactivo celular (ROS) , y todavía son el foco de un gran interés de investigación debido a su función exclusiva en la producción de ROS en condiciones fisiológicas normales. El complejo de NADPH oxidasa está inactivo en circunstancias normales, pero se activa para ensamblarse en las membranas durante el estallido respiratorio . La NADPH oxidasa activada genera superóxido que tiene funciones en la respuesta inmune de los animales y la señalización de las plantas.
El superóxido se puede producir en fagosomas que han ingerido bacterias y hongos , o se puede producir fuera de la célula. El superóxido mata bacterias y hongos por mecanismos que aún no se comprenden completamente. Se presume que el superóxido mata a las bacterias directamente, ya que la virulencia de muchos patógenos se atenúa drásticamente cuando se eliminan sus genes de superóxido dismutasa (SOD). Sin embargo, el superóxido también puede formar espontáneamente peróxido de hidrógeno que sufre más reacciones para generar otras especies reactivas de oxígeno (ROS) como el ácido hipocloroso (el agente reactivo en la lejía ). También puede inactivar enzimas metabólicas críticas, iniciar la peroxidación de lípidos , dañar los grupos de hierro-azufre y liberar hierro con actividad redox, lo que permite la generación de oxidantes indiscriminados como el radical hidroxilo.
En insectos , los NOX tenían algunas funciones aclaradas. Los artrópodos tienen tres tipos de NOX (NOX4-art, un NOX4 independiente de p22-phox específico de artrópodos y dos enzimas dependientes del calcio, DUOX). En el intestino, la producción de ROS dependientes de DUOX a partir de la mucosa de Drosophila melanogaster estimulada por bacterias es un mecanismo importante para matar patógenos y puede aumentar la defecación como respuesta de defensa. En Aedes aegypti , DUOX participa en el control de la microbiota autóctona intestinal. Rhodnius prolixus tiene DUOX activado por calcio, que interviene en el endurecimiento de la cáscara de huevo, y NOX5, que interviene en el control de la motilidad intestinal y la digestión de la sangre.
Regulación
La regulación cuidadosa de la actividad oxidasa de NADPH es crucial para mantener un nivel saludable de ROS en el cuerpo. La enzima está inactiva en las células en reposo, pero se activa rápidamente por varios estímulos, incluidos productos bacterianos y citocinas. Las oxidasas vasculares NADPH están reguladas por una variedad de hormonas y factores que se sabe que son actores importantes en la remodelación y la enfermedad vasculares. Estos incluyen trombina , factor de crecimiento derivado de plaquetas (PDGF), factor de necrosis tumoral (TNFa), lactosilceramida , interleucina-1 y LDL oxidada . También es estimulado por agonistas y ácido araquidónico . A la inversa, el ensamblaje del complejo puede inhibirse mediante apocinina y difenilen yodonio . La apocinina disminuye la inflamación pulmonar inducida por la influenza en ratones in vivo y, por lo tanto, puede tener beneficios clínicos en el tratamiento de la influenza.
Tipos
En los mamíferos, la NADPH oxidasa se encuentra en dos tipos: uno en los glóbulos blancos (neutrófilos) y el otro en las células vasculares , que difieren en su estructura y funciones bioquímicas. La NADPH oxidasa neutrofílica produce superóxido casi instantáneamente, mientras que la enzima vascular produce superóxido en minutos u horas. Además, en los glóbulos blancos, se ha descubierto que el superóxido transfiere electrones a través de la membrana al oxígeno extracelular, mientras que en las células vasculares, el anión radical parece liberarse principalmente de forma intracelular.
Patología
Los superóxidos son cruciales para matar bacterias extrañas en el cuerpo humano. En consecuencia, la falta de actividad puede conducir a una mayor susceptibilidad a organismos como los microbios catalasa positivos, y la sobreactividad puede conducir a estrés oxidativo y daño celular.
La producción excesiva de ROS en las células vasculares causa muchas formas de enfermedad cardiovascular, incluida la hipertensión , la aterosclerosis , el infarto de miocardio y el accidente cerebrovascular isquémico . La aterosclerosis es causada por la acumulación de macrófagos que contienen colesterol ( células espumosas ) en las paredes de las arterias (en la íntima ). Las ROS producidas por la NADPH oxidasa activan una enzima que hace que los macrófagos se adhieran a la pared arterial (al polimerizar las fibras de actina). Este proceso es contrarrestado por los inhibidores de la oxidasa NADPH y por los antioxidantes. Un desequilibrio a favor de ROS produce aterosclerosis. Estudios in vitro han encontrado que los inhibidores de la NADPH oxidasa apocinina y difenileniodonio, junto con los antioxidantes N-acetilcisteína y resveratrol, despolimerizaron la actina, rompieron las adherencias y permitieron que las células espumosas migraran fuera de la íntima.
Un estudio sugiere un papel de la NADPH oxidasa en la pérdida de parvalbúmina neuronal y expresión de GAD67 inducida por ketamina . Se observa una pérdida similar en la esquizofrenia , y los resultados pueden apuntar a la NADPH oxidasa como un posible jugador en la fisiopatología de la enfermedad. El nitro azul tetrazolio se utiliza en una prueba de diagnóstico, en particular, para la enfermedad granulomatosa crónica, una enfermedad en la que hay un defecto en la NADPH oxidasa; por lo tanto, el fagocito es incapaz de producir las especies reactivas de oxígeno o los radicales requeridos para la muerte bacteriana, lo que da como resultado que las bacterias prosperen dentro del fagocito. Cuanto mayor sea la puntuación azul, mejor será la célula para producir especies reactivas de oxígeno.
También se ha demostrado que la NADPH oxidasa juega un papel en el mecanismo que induce la formación de sFlt-1 , una proteína que desactiva ciertos factores proangiogénicos que juegan un papel en el desarrollo de la placenta, al facilitar la formación de especies reactivas de oxígeno , que son supuestos intermediarios en la formación de sFlt-1. Estos efectos son en parte responsables de inducir la preeclampsia en mujeres embarazadas.
Mutaciones
Las mutaciones en los genes de la subunidad de NADPH oxidasa causan varias Enfermedades Granulomatosas Crónicas (EGC), caracterizadas por una susceptibilidad extrema a la infección. Éstas incluyen:
- Enfermedad granulomatosa crónica ligada al cromosoma X (EGC)
- CGD autosómica recesiva citocromo b negativa
- CGD tipo I autosómico recesivo citocromo b positivo
- CGD tipo II autosómica recesiva positiva con citocromo b .
En estas enfermedades, las células tienen una baja capacidad de fagocitosis y se producen infecciones bacterianas persistentes. Las áreas de células infectadas son comunes, granulomas. Un trastorno similar llamado síndrome de inmunodeficiencia de neutrófilos está relacionado con una mutación en el RAC2, que también forma parte del complejo.
Inhibición
La NADPH oxidasa puede inhibirse mediante apocinina , óxido nítrico (NO) y difenilen yodonio . La apocinina actúa impidiendo el ensamblaje de las subunidades de NADPH oxidasa. La apocinina disminuye la inflamación pulmonar inducida por la influenza en ratones in vivo y, por lo tanto, puede tener beneficios clínicos en el tratamiento de la influenza.
La inhibición de la NADPH oxidasa por el NO bloquea la fuente de estrés oxidativo en la vasculatura. Por lo tanto, los medicamentos de donantes NO ( nitrovasodilatadores ) se han utilizado durante más de un siglo para tratar la enfermedad de las arterias coronarias , la hipertensión y la insuficiencia cardíaca al evitar que el exceso de superóxido deteriore las células vasculares sanas.
Los inhibidores de la oxidasa NADPH más avanzados incluyen GKT-831 (anteriormente GKT137831 ), un inhibidor dual de las isoformas NOX4 y NOX1 que se patentó en 2007. El compuesto se desarrolló inicialmente para la fibrosis pulmonar idiopática y obtuvo la designación de fármaco huérfano por la FDA y la EMA al final de 2010.
Estructura
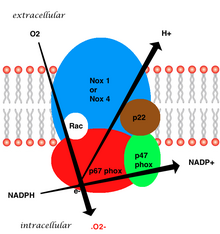
La estructura completa de la enzima vascular unida a la membrana se compone de cinco partes: dos subunidades citosólicas (p47phox y p67phox), un citocromo b558 que consta de gp91phox, p22phox y una pequeña proteína G Rac. La generación del superóxido en el NADPH vascular se produce mediante una reducción de un electrón de oxígeno a través de la subunidad gp91phox, utilizando NADPH reducido como donante de electrones. La proteína G pequeña tiene un papel esencial en la activación de la oxidasa al cambiar entre una forma unida a GDP (inactiva) y una forma unida a GTP (activa).
Tipo neutrófilo
La isoforma que se encuentra en los neutrófilos se compone de seis subunidades. Estas subunidades son:
- una Rho GTPasa , generalmente Rac1 o Rac2 (Rac significa sustrato de toxina botulínica C3 relacionada con Rho )
- Cinco subunidades de oxidasa fagocítica :
Tipo vascular
Hay varias isoformas vasculares del complejo que utilizan parálogos de la subunidad NOX2:
Tipo de tiroides
Hay dos parálogos más de la subunidad NOX2 en la tiroides:
Referencias
enlaces externos
- NADPH + oxidasa en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- EC 1.6.3.1