Androsterona - Androsterone
 | |
 | |
| Datos clinicos | |
|---|---|
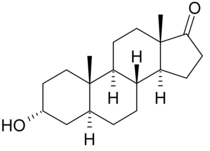
| Otros nombres | 3α-hidroxi-5α-androstan-17-ona, 5α-androstan-3α-ol-17-one |
| Código ATC | |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| CHEBI | |
| CHEMBL | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA |
100.000.159 |
| Datos químicos y físicos | |
| Fórmula | C 19 H 30 O 2 |
| Masa molar | 290,447 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
| (verificar) | |
La androsterona , o 3α-hidroxi-5α-androstan-17-ona , es una hormona esteroidea endógena , un neuroesteroide y una supuesta feromona . Es un andrógeno débil con una potencia que es aproximadamente 1/7 de la testosterona . La androsterona es un metabolito de la testosterona y la dihidrotestosterona (DHT). Además, se puede convertir de nuevo en DHT a través de la 3α-hidroxiesteroide deshidrogenasa y la 17β-hidroxiesteroide deshidrogenasa , sin pasar por intermedios convencionales como la androstanodiona y la testosterona, y como tal, puede considerarse un intermedio metabólico por derecho propio.
También se sabe que la androsterona es un neurosteroide androstano inhibidor , que actúa como un modulador alostérico positivo del receptor GABA A y posee efectos anticonvulsivos . El enantiómero no natural de la androsterona es más potente como modulador alostérico positivo de los receptores GABA A y como anticonvulsivo que la forma natural. El isómero 3β de la androsterona es la epiandrosterona y su epímero 5β es la etiocolanolona . El isómero 3β, 5β es epietiocolanolona .
Función biológica
En general, se ha considerado que la androsterona es un metabolito inactivo de la testosterona, que cuando se conjuga mediante glucuronidación y sulfatación permite que la testosterona se elimine del cuerpo, pero es un neurosteroide débil que puede atravesar el cerebro y podría tener efectos sobre la función cerebral.
Sin embargo, la opinión de que la androsterona es generalmente de baja importancia parece necesitar una revisión a la luz de la investigación del siglo XXI, que sugiere que la androsterona afecta significativamente la masculinización en los fetos de mamíferos. La masculinización de los genitales externos en humanos está sujeta a la dihidrotestosterona (DHT) derivada a través de la vía androgénica reconocida y también a través de una vía de puerta trasera . Por lo tanto, el androstanodiol puede usarse como marcador de la vía de puerta trasera de la síntesis de DHT. Los estudios espectrométricos identifican a la androsterona como el principal andrógeno de puerta trasera en el feto masculino humano. Los niveles circulantes dependen del sexo, estando la DHT esencialmente ausente en la mujer, en la que los títulos de intermediarios de puerta trasera también son muy bajos.
En los hombres, los intermediarios de puerta trasera ocurren principalmente en el hígado y las suprarrenales del feto, y en la placenta, casi nada en los testículos. En cambio, la progesterona en la placenta es el principal sustrato de puerta trasera para la síntesis de andrógenos. Esto también es consistente con la observación de que la insuficiencia placentaria se ha asociado con alteraciones del desarrollo de los genitales fetales.
Feromona
La androsterona se encuentra en la axila y la piel humanas , así como en la orina . También puede ser secretada por las glándulas sebáceas humanas . Se describe que tiene un olor almizclado similar al del androstenol . Se ha descubierto que la androsterona afecta el comportamiento humano cuando se huele.
Bioquímica
Biosíntesis
La androsterona y su isómero 5β, etiocolanolona , se producen en el cuerpo como metabolitos de la testosterona . La testosterona se convierte en 5α-dihidrotestosterona y 5β-dihidrotestosterona por la 5α-reductasa y la 5β-reductasa , respectivamente. La enzima 3α-hidroxiesteroide deshidrogenasa convierte las formas reducidas en 3α-androstanodiol y 3β-androstanodiol , que posteriormente son convertidas por la 17β-hidroxiesteroide deshidrogenasa en androsterona y etiocolanolona, respectivamente. La androsterona y la etiocolanolona también se pueden formar a partir de la androstenediona mediante la acción de la 5α-reductasa y la 5β-reductasa formando 5α-androstanodiona y 5β-androstanodiona que luego se convierten en androsterona y etiocolanolona por la 3α-hidroxiesteroide deshidrogenasa y la 3β-hidroxiesteroide deshidrogenasa , respectivamente.
Metabolismo
La androsterona se sulfata en sulfato de androsterona y se glucuronida en glucurónido de androsterona y estos conjugados se excretan en la orina .
Química
Fuentes
Se ha demostrado que la androsterona se encuentra naturalmente en el polen de pino y es bien conocida en muchas especies animales .
Historia
La androsterona fue aislada por primera vez en 1931 por Adolf Friedrich Johann Butenandt y Kurt Tscherning . Destilaron más de 17.000 litros (3.700 gal imp; 4.500 gal EE.UU.) de orina masculina, de los cuales obtuvieron 50 miligramos (0,77 gr) de androsterona cristalina, que fue suficiente para encontrar que la fórmula química era muy similar a la estrona .
Ver también
- Vía de puerta trasera de andrógenos
- Lista de andrógenos / esteroides anabólicos
- Lista de neuroesteroides § Androstanos
- Lista de neuroesteroides § Feromonas y ferinas
