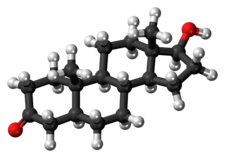
Dihidrotestosterona - Dihydrotestosterone

|
|
|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
(1 S , 3a S , 3b R , 5a S , 9a S , 9b S , 11a S ) -1-hidroxi-9a, 11a-dimethylhexadecahydro-7 H ciclopenta [ a ] fenantren-7-ona |
|
| Otros nombres
DHT; 5 \ alpha - dihidrotestosterona; 5α-DHT; Androstanolona; Stanolone; 5α-Androstan-17β-ol-3-ona
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Tarjeta de información ECHA |
100.007.554 |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 19 H 30 O 2 | |
| Masa molar | 290,447 g · mol −1 |
| Farmacología | |
| A14AA01 ( OMS ) | |
| Transdérmico ( gel ), en la mejilla , debajo de la lengua , inyección intramuscular (como ésteres ) | |
| Farmacocinética : | |
| Oral : muy bajo (debido al extenso metabolismo de primer paso ) | |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
La dihidrotestosterona ( DHT , 5α-dihidrotestosterona , 5α-DHT , androstanolona o estanolona ) es un esteroide y una hormona sexual androgénica endógena . La enzima 5α-reductasa cataliza la formación de DHT a partir de testosterona en ciertos tejidos, incluida la glándula prostática , las vesículas seminales , los epidídimos , la piel , los folículos pilosos , el hígado y el cerebro . Esta enzima media la reducción del doble enlace C4-5 de la testosterona. En relación con la testosterona, la DHT es considerablemente más potente como agonista del receptor de andrógenos (AR).
Además de su función como hormona natural, la DHT se ha utilizado como medicamento , por ejemplo, en el tratamiento de niveles bajos de testosterona en los hombres ; para obtener información sobre la DHT como medicamento, consulte el artículo sobre androstanolona .
Función biológica
La DHT es biológicamente importante para la diferenciación sexual de los genitales masculinos durante la embriogénesis , la maduración del pene y el escroto en la pubertad , el crecimiento del vello facial , corporal y púbico , y el desarrollo y mantenimiento de la glándula prostática y las vesículas seminales . Se produce a partir de la testosterona menos potente por la enzima 5α-reductasa en tejidos seleccionados, y es el andrógeno principal en los genitales, la glándula prostática , las vesículas seminales , la piel y los folículos pilosos .
La DHT emite señales principalmente de manera intracrina y paracrina en los tejidos en los que se produce, desempeñando solo un papel menor, si es que lo hay, como hormona endocrina circulante . Los niveles circulantes de DHT son 1/10 y 1/20 de los de testosterona en términos de concentraciones totales y libres, respectivamente, mientras que los niveles locales de DHT pueden ser hasta 10 veces superiores a los de testosterona en tejidos con alta expresión de 5α-reductasa como la próstata. glándula. Además, a diferencia de la testosterona, la DHT es inactivada por la 3α-hidroxiesteroide deshidrogenasa (3α-HSD) en el andrógeno muy débil 3α-androstanodiol en varios tejidos como el músculo , el tejido adiposo y el hígado, entre otros, y en relación con esto, la DHT ha sido informó que es un agente anabólico muy pobre cuando se administra exógenamente como medicamento.
| Testosterona | DHT |
|---|---|
| Espermatogénesis y fertilidad | Agrandamiento de la próstata y riesgo de cáncer de próstata |
| Desarrollo musculoesquelético masculino | Crecimiento del vello facial, axilar, púbico y corporal |
| Profundización de la voz | Recesión temporal del cuero cabelludo y patrón de caída del cabello |
| Aumento de la producción de sebo y acné. | |
| Aumento del deseo sexual y erecciones. |
Además de las funciones biológicas normales, la DHT también desempeña un papel causal importante en una serie de afecciones dependientes de andrógenos, incluidas afecciones del cabello como el hirsutismo (crecimiento excesivo del vello facial / corporal) y la pérdida de cabello de patrón (alopecia androgénica o calvicie de patrón) y enfermedades de la próstata como como hiperplasia prostática benigna (HPB) y cáncer de próstata . Los inhibidores de la 5α-reductasa , que previenen la síntesis de DHT, son eficaces en la prevención y el tratamiento de estas afecciones. Además, la DHT puede desempeñar una función en el reclutamiento y la función del transportador de aminoácidos del músculo esquelético.
Se ha descubierto que los metabolitos de la DHT actúan como neuroesteroides con su propia actividad biológica independiente de AR. El 3α-androstanodiol es un potente modulador alostérico positivo del receptor GABA A , mientras que el 3β-androstanodiol es un agonista potente y selectivo del subtipo de receptor de estrógeno (ER), ERβ . Estos metabolitos pueden desempeñar funciones importantes en los efectos centrales de la DHT y, por extensión, la testosterona, incluidos sus efectos antidepresivos , ansiolíticos , gratificantes / hedónicos , antiestrés y procognitivos .
Deficiencia de 5α-reductasa 2
Gran parte del papel biológico de la DHT se ha dilucidado en estudios de individuos con alteración de la actividad de la 5α-reductasa 2 como resultado de mutaciones en el gen SRD5A2 subyacente . La condición, conocida como deficiencia de 5α-reductasa 2 , tiene una variedad de presentaciones como apariciones atípicas de los genitales externos en los hombres.
Inhibidores de la 5α-reductasa
Los inhibidores de la 5α-reductasa como la finasterida y la dutasterida inhiben la 5α-reductasa tipo II y / u otras isoformas y pueden disminuir los niveles de DHT circulante entre un 65 y un 98%, dependiendo del inhibidor de la 5α-reductasa en cuestión. Como tal, de manera similar al caso de la deficiencia de 5α-reductasa tipo II, proporcionan conocimientos útiles en la elucidación de las funciones biológicas de la DHT. Se desarrollaron inhibidores de la 5α-reductasa y se utilizan principalmente para el tratamiento de la BPH. Los medicamentos pueden reducir significativamente el tamaño de la glándula prostática y aliviar los síntomas de la afección. El tratamiento a largo plazo con inhibidores de la 5α-reductasa también puede reducir significativamente el riesgo general de cáncer de próstata, aunque se ha observado un pequeño aumento simultáneo en el riesgo de ciertos tumores de alto grado. Además de las enfermedades de la próstata, posteriormente se han desarrollado e introducido inhibidores de la 5α-reductasa para el tratamiento de la caída del cabello de patrón en los hombres. Pueden prevenir una mayor progresión de la caída del cabello en la mayoría de los hombres con la afección y producir cierta recuperación del cabello en aproximadamente dos tercios de los hombres. Por otro lado, los inhibidores de la 5α-reductasa parecen ser menos efectivos para la pérdida de cabello de patrón en las mujeres, aunque todavía muestran cierta efectividad. Aparte de la pérdida de cabello de patrón, los medicamentos también son útiles en el tratamiento del hirsutismo y pueden reducir en gran medida el crecimiento del vello facial y corporal en mujeres con la afección.
Los inhibidores de la 5α-reductasa se toleran bien en general y muestran una baja incidencia de efectos adversos . La disfunción sexual , incluida la disfunción eréctil , la pérdida de la libido y la reducción del volumen de la eyaculación , puede ocurrir en 3.4 a 15.8% de los hombres tratados con finasterida o dutasterida. Puede observarse un pequeño aumento en el riesgo de síntomas afectivos que incluyen depresión , ansiedad y autolesiones . Tanto la disfunción sexual como los síntomas afectivos pueden deberse parcial o totalmente a la prevención de la síntesis de neuroesteroides como la alopregnanolona y no necesariamente a la inhibición de la producción de DHT. Se ha asociado un riesgo muy pequeño de ginecomastia con los inhibidores de la 5α-reductasa (1,2 a 3,5%). Según los informes de deficiencia de 5α-reductasa tipo II en hombres y la eficacia de los inhibidores de 5α-reductasa para el hirsutismo en mujeres, la reducción del crecimiento del vello corporal y / o facial es un posible efecto secundario potencial de estos medicamentos en hombres. Hay muy pocos estudios que evalúen los efectos secundarios de los inhibidores de la 5α-reductasa en mujeres. Sin embargo, debido al papel conocido de la DHT en la diferenciación sexual masculina, los inhibidores de la 5α-reductasa pueden causar defectos de nacimiento como genitales ambiguos en los fetos masculinos de mujeres embarazadas . Como tal, no se utilizan en mujeres durante el embarazo.
MK-386 es un inhibidor selectivo de la 5α-reductasa de tipo I que nunca se comercializó. Mientras que los inhibidores de la 5α-reductasa tipo II logran reducciones mucho mayores en la producción de DHT circulante, MK-386 disminuye los niveles de DHT circulante entre un 20 y un 30%. Por el contrario, se descubrió que disminuía los niveles de DHT en sebo en un 55% en los hombres frente a una modesta reducción de solo un 15% para la finasterida. Sin embargo, MK-386 no demostró una eficacia significativa en un estudio clínico posterior para el tratamiento del acné.
Actividad biológica
La DHT es un potente agonista del AR y, de hecho, es el ligando endógeno conocido más potente del receptor. Tiene una afinidad (K d ) de 0,25 a 0,5 nM por el AR humano, que es aproximadamente de 2 a 3 veces mayor que la de la testosterona (K d = 0,4 a 1,0 nM) y de 15 a 30 veces mayor que la de andrógenos suprarrenales . Además, la tasa de disociación de la DHT del AR es 5 veces más lenta que la de la testosterona. La CE 50 de DHT para la activación del AR es 0,13 nM, que es aproximadamente 5 veces más fuerte que la de la testosterona (CE 50 = 0,66 nM). En bioensayos , se ha encontrado que la DHT es de 2,5 a 10 veces más potente que la testosterona.
La vida media de eliminación de la DHT en el cuerpo (53 minutos) es más larga que la de la testosterona (34 minutos), y esto puede explicar parte de la diferencia en su potencia. Un estudio de DHT transdérmico y tratamiento con testosterona informó semividas terminales de 2,83 horas y 1,29 horas, respectivamente.
A diferencia de otros andrógenos como la testosterona, la enzima aromatasa no puede convertir la DHT en un estrógeno como el estradiol . Por lo tanto, se usa con frecuencia en entornos de investigación para distinguir entre los efectos de la testosterona causados por la unión al AR y los causados por la conversión de testosterona en estradiol y la posterior unión y activación de los RE. Aunque la DHT no se puede aromatizar, todavía se transforma en metabolitos con una actividad y una afinidad significativa por el ER. Estos son 3α-androstanodiol y 3β-androstanodiol, que son agonistas predominantes del ERβ.
Bioquímica

Biosíntesis
Vía primaria
La DHT es sintetizada irreversiblemente a partir de testosterona por la enzima 5α-reductasa . Esto ocurre en varios tejidos, incluidos los genitales ( pene , escroto , clítoris , labios mayores ), próstata , piel , folículos pilosos , hígado y cerebro . Alrededor del 5 al 7% de la testosterona sufre una reducción de 5α en DHT, y aproximadamente de 200 a 300 μg de DHT se sintetizan en el cuerpo por día. La mayor parte de la DHT se produce en tejidos periféricos como la piel y el hígado, mientras que la mayor parte de la DHT circulante se origina específicamente en el hígado. Los testículos y la próstata contribuyen relativamente poco a las concentraciones de DHT en circulación.
Hay dos isoformas principales de 5α-reductasa, SRD5A1 (tipo I) y SRD5A2 (tipo II), siendo esta última la isoenzima biológicamente más importante. También existe una tercera 5α-reductasa: SRD5A3 . SRD5A2 se expresa más en los genitales, la glándula prostática , los epidídimos , las vesículas seminales , la piel genital , los folículos pilosos faciales y torácicos y el hígado , mientras que se observa una menor expresión en ciertas áreas del cerebro , piel / folículos pilosos no genitales, testículos y los riñones . SRD5A1 se expresa más en los folículos pilosos / cutáneos no genitales, el hígado y ciertas áreas del cerebro, mientras que los niveles más bajos están presentes en la próstata, los epidídimos, las vesículas seminales, la piel genital, los testículos, las glándulas suprarrenales y los riñones. En la piel, la 5α-reductasa se expresa en las glándulas sebáceas , glándulas sudoríparas , células epidérmicas y folículos pilosos. Ambas isoenzimas se expresan en los folículos pilosos del cuero cabelludo , aunque SRD5A2 predomina en estas células. El subtipo SRD5A2 es la isoforma casi exclusiva expresada en la glándula prostática.
Camino de puerta trasera
La DHT en ciertas condiciones normales y patológicas se puede producir a través de una ruta que no involucre al intermedio de testosterona. Esta ruta se llama "camino de puerta trasera".
La ruta puede describirse como 17α-hidroxiprogesterona → 5α-pregnan-17α-ol-3,20-diona → 5α-pregnane-3α, 17α-diol-20-one → androsterona → 5α-androstano-3α, 17β-diol ( androstanodiol) → DHT.
Esta vía no siempre se considera en la evaluación clínica de pacientes con hiperandrogenismo . Ignorar esta vía puede conducir a errores de diagnóstico y confusión, cuando la vía biosintética de andrógenos convencional no puede explicar completamente las consecuencias observadas.
Distribución
La unión de DHT a proteínas plasmáticas es superior al 99%. En los hombres, aproximadamente el 0,88% de la DHT no está unida y, por lo tanto, está libre, mientras que en las mujeres premenopáusicas, alrededor del 0,47 a 0,48% está libre. En los hombres, la DHT se une en un 49,7% a la globulina transportadora de hormonas sexuales (SHBG), el 39,2% a la albúmina y el 0,22% a la globulina transportadora de corticosteroides (CBG), mientras que en las mujeres premenopáusicas, la DHT se une en un 78,1% a 78,4% a la SHBG. 21,0-21,3% a albúmina y 0,12% a CBG. Al final del embarazo, solo el 0,07% de la DHT está libre en las mujeres; El 97,8% está unido a SHBG, mientras que el 2,15% está unido a la albúmina y el 0,04% está unido a CBG. La DHT tiene una mayor afinidad por la SHBG que la testosterona, el estradiol o cualquier otra hormona esteroidea.
| Compuesto | Grupo | Nivel (nM) | Gratis (%) | SHBG (%) | CBG (%) | Albúmina (%) |
|---|---|---|---|---|---|---|
| Testosterona | Hombres adultos | 23,0 | 2.23 | 44,3 | 3,56 | 49,9 |
| Mujeres adultas | ||||||
| Fase folicular | 1.3 | 1,36 | 66,0 | 2,26 | 30,4 | |
| Fase lútea | 1.3 | 1,37 | 65,7 | 2,20 | 30,7 | |
| El embarazo | 4,7 | 0,23 | 95,4 | 0,82 | 3.6 | |
| Dihidrotestosterona | Hombres adultos | 1,70 | 0,88 | 49,7 | 0,22 | 39,2 |
| Mujeres adultas | ||||||
| Fase folicular | 0,65 | 0,47 | 78,4 | 0,12 | 21,0 | |
| Fase lútea | 0,65 | 0,48 | 78,1 | 0,12 | 21,3 | |
| El embarazo | 0,93 | 0,07 | 97,8 | 0,04 | 21,2 | |
| Fuentes: Ver plantilla. | ||||||
Metabolismo
|
|
La DHT se inactiva en el hígado y los tejidos extrahepáticos como la piel en 3α-androstanodiol y 3β-androstanodiol por las enzimas 3α-hidroxiesteroide deshidrogenasa y 3β-hidroxiesteroide deshidrogenasa , respectivamente. Estos metabolitos se convierten a su vez, respectivamente, en androsterona y epiandrosterona , luego se conjugan (mediante glucuronidación y / o sulfatación ), se liberan a la circulación y se excretan en la orina .
A diferencia de la testosterona, la DHT no se puede aromatizar en un estrógeno como el estradiol y, por esta razón, no tiene propensión a los efectos estrogénicos.
Excreción
La DHT se excreta en la orina como metabolitos , como los conjugados de 3α-androstanodiol y androsterona .
Niveles
Los niveles séricos de DHT son aproximadamente 10% de los de testosterona, pero los niveles en la glándula prostática son de 5 a 10 veces más altos que los de testosterona debido a una conversión de más del 90% de testosterona en DHT por la 5α-reductasa expresada localmente. Por esta razón, y además del hecho de que la DHT es mucho más potente como agonista AR que la testosterona, la DHT se considera el principal andrógeno de la glándula prostática.
Uso medico
La DHT está disponible en formulaciones farmacéuticas para uso médico como un andrógeno o esteroide anabólico-androgénico (AAS). Se utiliza principalmente en el tratamiento del hipogonadismo masculino . Cuando se usa como medicamento, la dihidrotestosterona se conoce como androstanolona ( DCI ) o como estanolona ( BAN ), y se vende bajo marcas como Andractim, entre otras. La disponibilidad de DHT farmacéutica es limitada; no está disponible en los Estados Unidos o Canadá , pero está disponible en algunos países europeos . Las formulaciones disponibles de DHT incluyen comprimidos bucales o sublinguales , geles tópicos y, como ésteres en aceite , inyectables como propionato de androstanolona y valerato de androstanolona .
Química
DHT, también conocido como 5α-androstan-17β-ol-3-one, es un esteroide androstano de origen natural con un grupo cetona en la posición C3 y un grupo hidroxilo en la posición C17β. Es el derivado de la testosterona en el que el doble enlace entre las posiciones C4 y C5 se ha reducido o hidrogenado .
Historia
La DHT fue sintetizada por primera vez por Adolf Butenandt y sus colegas en 1935. Se preparó mediante la hidrogenación de testosterona, que se había descubierto a principios de ese año. La DHT se introdujo para uso médico como AAS en 1953 y se observó que era más potente que la testosterona pero con una androgenicidad reducida. No se determinó que fuera una sustancia endógena hasta 1956, cuando se demostró que se formaba a partir de testosterona en homogeneizados de hígado de rata. Además, la importancia biológica de la DHT no se comprendió hasta principios de la década de 1960, cuando se descubrió que era producida por la 5α-reductasa a partir de la testosterona circulante en los tejidos diana como la glándula prostática y las vesículas seminales y se descubrió que era más potente que la testosterona en bioensayos. Las funciones biológicas de la DHT en humanos se definieron mucho más claramente con el descubrimiento y caracterización de la deficiencia de 5α-reductasa tipo II en 1974. La DHT fue la última hormona sexual importante, las otras son testosterona, estradiol y progesterona , por descubrir, y es único en el sentido de que es la única hormona sexual importante que funciona principalmente como una hormona intracrina y paracrina en lugar de como una hormona endocrina.

