Hormona esteroide - Steroid hormone
| Hormona esteroide | |
|---|---|
| Clase de droga | |

| |
| Identificadores de clase | |
| Sinónimos | Esteroide suprarrenal; Esteroide gonadal |
| Usar | Varios |
| Objetivo biológico | Receptores de hormonas esteroides |
| Clase química | Esteroides ; No esteroideo |
| En Wikidata | |
Una hormona esteroidea es un esteroide que actúa como hormona . Las hormonas esteroides se pueden agrupar en dos clases: corticosteroides (típicamente producidos en la corteza suprarrenal , por lo tanto corticoides ) y esteroides sexuales (producidos típicamente en las gónadas o placenta ). Dentro de esas dos clases hay cinco tipos según los receptores a los que se unen: glucocorticoides y mineralocorticoides (ambos corticosteroides) y andrógenos , estrógenos y progestágenos (esteroides sexuales). Los derivados de la vitamina D son un sexto sistema hormonal estrechamente relacionado con receptores homólogos. Tienen algunas de las características de los verdaderos esteroides como ligandos de receptores .
Las hormonas esteroides ayudan a controlar el metabolismo , la inflamación , las funciones inmunitarias , el equilibrio de agua y sal , el desarrollo de las características sexuales y la capacidad de resistir lesiones y enfermedades. El término esteroide describe tanto las hormonas producidas por el cuerpo como los medicamentos producidos artificialmente que duplican la acción de los esteroides naturales.
Síntesis

Las hormonas esteroides naturales generalmente se sintetizan a partir del colesterol en las gónadas y las glándulas suprarrenales . Estas formas de hormonas son lípidos . Pueden atravesar la membrana celular ya que son solubles en grasa y luego unirse a los receptores de hormonas esteroides (que pueden ser nucleares o citosólicos según la hormona esteroidea) para producir cambios dentro de la célula. Las hormonas esteroides generalmente se transportan en la sangre, unidas a proteínas transportadoras específicas , como la globulina transportadora de hormonas sexuales o la globulina transportadora de corticosteroides . Se producen más conversiones y catabolismo en el hígado, en otros tejidos "periféricos" y en los tejidos diana.
| Sexo | Hormona sexual | Fase reproductiva |
Tasa de producción de sangre |
Tasa de secreción gonadal |
Tasa de aclaramiento metabólico |
Rango de referencia (niveles séricos) | |
|---|---|---|---|---|---|---|---|
| Unidades SI | No SI unidades | ||||||
| Hombres | Androstenediona |
-
|
2,8 mg / día | 1,6 mg / día | 2200 L / día | 2.8–7.3 nmol / L | 80-210 ng / dL |
| Testosterona |
-
|
6,5 mg / día | 6,2 mg / día | 950 L / día | 6,9 a 34,7 nmol / L | 200–1000 ng / dL | |
| Estrona |
-
|
150 μg / día | 110 μg / día | 2050 L / día | 37 a 250 pmol / L | 10 a 70 pg / ml | |
| Estradiol |
-
|
60 μg / día | 50 μg / día | 1600 L / día | <37 a 210 pmol / L | 10 a 57 pg / ml | |
| Sulfato de estrona |
-
|
80 μg / día | Insignificante | 167 L / día | 600-2500 pmol / L | 200–900 pg / mL | |
| Mujeres | Androstenediona |
-
|
3,2 mg / día | 2,8 mg / día | 2000 L / día | 3,1-12,2 nmol / L | 89–350 ng / dL |
| Testosterona |
-
|
190 μg / día | 60 μg / día | 500 L / día | 0,7–2,8 nmol / L | 20 a 81 ng / dl | |
| Estrona | Fase folicular | 110 μg / día | 80 μg / día | 2200 L / día | 110 a 400 pmol / L | 30-110 pg / mL | |
| Fase lútea | 260 μg / día | 150 μg / día | 2200 L / día | 310–660 pmol / L | 80-180 pg / ml | ||
| Post menopausia | 40 μg / día | Insignificante | 1610 L / día | 22 a 230 pmol / L | 6 a 60 pg / ml | ||
| Estradiol | Fase folicular | 90 μg / día | 80 μg / día | 1200 L / día | <37–360 pmol / L | 10 a 98 pg / ml | |
| Fase lútea | 250 μg / día | 240 μg / día | 1200 L / día | 699-1250 pmol / L | 190–341 pg / mL | ||
| Post menopausia | 6 μg / día | Insignificante | 910 L / día | <37-140 pmol / L | 10 a 38 pg / ml | ||
| Sulfato de estrona | Fase folicular | 100 μg / día | Insignificante | 146 L / día | 700–3600 pmol / L | 250-1300 pg / mL | |
| Fase lútea | 180 μg / día | Insignificante | 146 L / día | 1100–7300 pmol / L | 400 a 2600 pg / ml | ||
| Progesterona | Fase folicular | 2 mg / día | 1,7 mg / día | 2100 L / día | 0,3-3 nmol / L | 0,1 a 0,9 ng / ml | |
| Fase lútea | 25 mg / día | 24 mg / día | 2100 L / día | 19–45 nmol / L | 6–14 ng / ml | ||
|
Notas y fuentes
Notas: "La concentración de un esteroide en la circulación está determinada por la velocidad a la que se secreta por las glándulas, la velocidad del metabolismo de los precursores o prehormonas en el esteroide y la velocidad a la que los tejidos lo extraen y metabolizan. La tasa de secreción de un esteroide se refiere a la secreción total del compuesto de una glándula por unidad de tiempo. Las tasas de secreción se han evaluado tomando muestras del efluente venoso de una glándula a lo largo del tiempo y restando la concentración de hormonas venosas arteriales y periféricas. La tasa de aclaramiento metabólico de un esteroide se define como el volumen de sangre que se ha eliminado completamente de la hormona por unidad de tiempo. La tasa de producción de una hormona esteroide se refiere a la entrada en la sangre del compuesto de todas las fuentes posibles, incluida la secreción de las glándulas y la conversión de prohormonas en el esteroide de interés. En estado estacionario, la cantidad de hormona que ingresa a la sangre de todas las fuentes será igual a la velocidad a la que se está clicando orejas (tasa de aclaramiento metabólico) multiplicado por la concentración sanguínea (tasa de producción = tasa de aclaramiento metabólico × concentración). Si hay poca contribución del metabolismo de las prohormonas al grupo circulante de esteroides, entonces la tasa de producción se aproximará a la tasa de secreción ". Fuentes: consulte la plantilla.
|
|||||||
Esteroides y esteroles sintéticos
También se han ideado una variedad de esteroides y esteroles sintéticos. La mayoría son esteroides, pero algunas moléculas no esteroides pueden interactuar con los receptores de esteroides debido a una similitud de forma. Algunos esteroides sintéticos son más débiles o más fuertes que los esteroides naturales cuyos receptores activan.
Algunos ejemplos de hormonas esteroides sintéticas:
- Glucocorticoides : alclometasona , prednisona , dexametasona , triamcinolona , cortisona
- Mineralocorticoide : fludrocortisona
- Vitamina D: dihidrotaquisterol
- Andrógenos: oxandrolona , oxabolona , nandrolona (también conocidos como esteroides anabólico-androgénicos o simplemente esteroides anabólicos )
- Estrógenos: dietilestilbestrol (DES) y etinilestradiol (EE)
- Progestinas: noretisterona , acetato de medroxiprogesterona , caproato de hidroxiprogesterona .
Algunos antagonistas de esteroides:
- Andrógeno: acetato de ciproterona
- Progestinas: mifepristona , gestrinona
Transporte
Las hormonas esteroides se transportan a través de la sangre uniéndose a proteínas transportadoras, proteínas séricas que las unen y aumentan la solubilidad de las hormonas en agua. Algunos ejemplos son la globulina transportadora de hormonas sexuales (SHBG), la globulina transportadora de corticosteroides y la albúmina . La mayoría de los estudios dicen que las hormonas solo pueden afectar a las células cuando no están unidas por proteínas séricas. Para ser activas, las hormonas esteroides deben liberarse de sus proteínas solubilizantes en sangre y unirse a receptores extracelulares o cruzar pasivamente la membrana celular y unirse a receptores nucleares . Esta idea se conoce como la hipótesis de la hormona libre. Esta idea se muestra en la Figura 1 a la derecha.
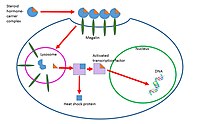
Un estudio ha descubierto que estos complejos de esteroides-portadores están unidos por la megalina , un receptor de membrana, y luego se introducen en las células mediante endocitosis . Una posible vía es que una vez dentro de la célula, estos complejos se llevan al lisosoma, donde la proteína transportadora se degrada y la hormona esteroidea se libera en el citoplasma de la célula diana. Luego, la hormona sigue una vía de acción genómica. Este proceso se muestra en la Figura 2 a la derecha. El papel de la endocitosis en el transporte de hormonas esteroides no se comprende bien y se está investigando más a fondo.
Para que las hormonas esteroides atraviesen la bicapa lipídica de las células, deben superar las barreras energéticas que evitarían su entrada o salida de la membrana. La energía libre de Gibbs es un concepto importante aquí. Estas hormonas, que se derivan todas del colesterol, tienen grupos funcionales hidrófilos en cada extremo y cadenas principales de carbono hidrófobas. Cuando las hormonas esteroides ingresan a las membranas, existen barreras de energía libre cuando los grupos funcionales ingresan al interior hidrofóbico de la membrana, pero es energéticamente favorable que el núcleo hidrofóbico de estas hormonas ingrese a las bicapas lipídicas. Estas barreras y pozos de energía se invierten para las hormonas que salen de las membranas. Las hormonas esteroides entran y salen fácilmente de la membrana en condiciones fisiológicas. Se ha demostrado experimentalmente que atraviesan las membranas a una velocidad de 20 μm / s, dependiendo de la hormona.
Aunque es energéticamente más favorable que las hormonas estén en la membrana que en el ECF o ICF, de hecho abandonan la membrana una vez que han entrado en ella. Esta es una consideración importante porque el colesterol, el precursor de todas las hormonas esteroides, no abandona la membrana una vez que se ha incrustado en su interior. La diferencia entre el colesterol y estas hormonas es que el colesterol se encuentra en un pozo de energía libre de Gibb negativo mucho más grande una vez dentro de la membrana, en comparación con estas hormonas. Esto se debe a que la cola alifática del colesterol tiene una interacción muy favorable con el interior de las bicapas lipídicas.
Mecanismos de acción y efectos.
Existen muchos mecanismos diferentes a través de los cuales las hormonas esteroides afectan sus células diana. Todas estas diferentes vías pueden clasificarse como que tienen un efecto genómico o un efecto no genómico. Las vías genómicas son lentas y alteran los niveles de transcripción de ciertas proteínas en la célula; las vías no genómicas son mucho más rápidas.
Vías genómicas
Los primeros mecanismos identificados de acción de las hormonas esteroides fueron los efectos genómicos. En esta vía, las hormonas libres pasan primero a través de la membrana celular porque son solubles en grasa. En el citoplasma, el esteroide puede sufrir o no una alteración mediada por enzimas , como reducción, hidroxilación o aromatización. Luego, el esteroide se une a un receptor específico de hormonas esteroides , también conocido como receptor nuclear , que es una metaloproteína grande. Tras la unión de esteroides, muchos tipos de receptores de esteroides se dimerizan : dos subunidades del receptor se unen para formar una unidad funcional de unión al ADN que puede ingresar al núcleo celular. Una vez en el núcleo, el complejo ligando esteroide-receptor se une a secuencias específicas de ADN e induce la transcripción de sus genes diana .
Vías no genómicas
Debido a que las vías no genómicas incluyen cualquier mecanismo que no sea un efecto genómico, existen varias vías no genómicas. Sin embargo, todas estas vías están mediadas por algún tipo de receptor de hormonas esteroides que se encuentra en la membrana plasmática. Se ha demostrado que los canales iónicos, los transportadores, los receptores acoplados a proteínas G (GPCR) y la fluidez de la membrana se ven afectados por las hormonas esteroides. De estas, las proteínas ligadas a GPCR son las más comunes. Para obtener más información sobre estas proteínas y vías, visite la página del receptor de hormonas esteroides .
Ver también
Referencias
Otras lecturas
- Brook CG (1999). "Mecanismo de la pubertad". Horm. Res . 51 Suppl 3 (3): 52–4. doi : 10.1159 / 000053162 . PMID 10592444 .
- Holmes SJ, Shalet SM (1996). "Papel de la hormona del crecimiento y los esteroides sexuales en el logro y mantenimiento de la masa ósea normal". Horm. Res . 45 (1–2): 86–93. doi : 10.1159 / 000184765 . PMID 8742125 .
- Ottolenghi C, Uda M, Crisponi L, Omari S, Cao A, Forabosco A, Schlessinger D (enero de 2007). "Determinación y estabilidad del sexo". BioEssays . 29 (1): 15-25. doi : 10.1002 / bies.20515 . PMID 17187356 .
- Couse JF, Korach KS (junio de 1998). "Explorando el papel de los esteroides sexuales a través de estudios de ratones deficientes en receptores" . J. Mol. Med . 76 (7): 497–511. doi : 10.1007 / s001090050244 . PMID 9660168 .
- McEwen BS (1992). "Hormonas esteroides: efecto sobre el desarrollo y la función del cerebro". Horm. Res . 37 Suppl 3 (3): 1–10. doi : 10.1159 / 000182393 . PMID 1330863 .
- Simons (agosto de 2008). "acciones de hormonas esteroides fisiológicas versus farmacológicas" . BioEssays . 30 (8): 744–56. doi : 10.1002 / bies.20792 . PMC 2742386 . PMID 18623071 .
- Han, Thang S .; Walker, Brian R .; Arlt, Wiebke; Ross, Richard J. (17 de diciembre de 2013). "Tratamiento y resultados de salud en adultos con hiperplasia suprarrenal congénita". Nature Reviews Endocrinología . 10 (2): 115-124. doi : 10.1038 / nrendo.2013.239 . PMID 24342885 Figura 2: Vía de la esteroidogénesis suprarrenal.CS1 maint: posdata ( enlace )