Ácido jasmónico - Jasmonic acid
|
|

|
|
| Nombres | |
|---|---|
|
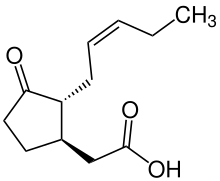
Nombre IUPAC preferido
Ácido [(1 R , 2 R ) -3-oxo-2 - [(2 Z ) -pent-2-en-1-il] ciclopentil] acético |
|
| Otros nombres
Ácido jasmónico
(-) - Ácido jasmónico JA, ( 1R, 2R ) -3-Oxo-2- ( 2Z ) -2-pentenil-ciclopentiletanoico {(1R, 2R) -3-Oxo-2 - [(2Z) - Ácido 2-penten-1-il] ciclopentil} acético |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 12 H 18 O 3 | |
| Masa molar | 210,27 g / mol |
| Densidad | 1,1 g / cm 3 |
| Punto de ebullición | 160 ° C (320 ° F; 433 K) a 0,7 mmHg |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El ácido jasmónico ( JA ) es un compuesto orgánico que se encuentra en varias plantas, incluido el jazmín . La molécula es un miembro de la clase de hormonas vegetales jasmonato . Se biosintetiza a partir del ácido linolénico por la vía octadecanoide . Fue aislado por primera vez en 1957 como el éster metílico del ácido jasmónico por el químico suizo Edouard Demole y sus colegas.
Biosíntesis
Su biosíntesis parte del ácido graso linolénico , que es oxigenado por la Lipoxigenasa (13-LOX), formando un peróxido. Este peróxido luego se cicla en presencia de alénóxido sintasa para formar un alenoóxido . Este óxido de aleno se reordena a medida que es catalizado por la enzima ciclasa de óxido de aleno para formar ácido 12-oxofitodienoico y sufre una serie de oxidaciones β a ácido 7-iso-jasmónico. En ausencia de enzima, este ácido iso-jasmónico se isomeriza a ácido jasmónico.
Función
La función principal de JA y sus diversos metabolitos es regular las respuestas de las plantas al estrés abiótico y biótico, así como el crecimiento y desarrollo de las plantas. Los procesos de crecimiento y desarrollo de las plantas regulados incluyen inhibición del crecimiento, senescencia , enrollamiento de zarcillos , desarrollo de flores y abscisión de hojas. JA también es responsable de la formación de tubérculos en papas y ñames. Tiene un papel importante en respuesta a las heridas de las plantas y la resistencia sistémica adquirida . El gen Dgl es responsable de mantener los niveles de JA durante las condiciones habituales en Zea mays , así como de la liberación preliminar de ácido jasmónico poco después de ser alimentado. Cuando las plantas son atacadas por insectos, responden liberando JA, que activa la expresión de inhibidores de proteasa , entre muchos otros compuestos de defensa anti-herbívoros. Estos inhibidores de proteasa evitan la actividad proteolítica de las proteasas digestivas o "proteínas salivales" de los insectos, impidiendo así que adquieran el nitrógeno necesario en la proteína para su propio crecimiento. JA también activa la expresión de polifenol oxidasa que promueve la producción de quinolinas . Estos pueden interferir con la producción de enzimas del insecto y disminuir el contenido nutricional de la planta ingerida.
JA puede tener un papel en el control de plagas. De hecho, JA ha sido considerado como un tratamiento de semillas para estimular las defensas naturales anti-plagas de las plantas que germinan a partir de las semillas tratadas. En esta aplicación, se pulverizan jasmonatos sobre plantas que ya han comenzado a crecer. Estas aplicaciones estimulan la producción de inhibidores de proteasa en la planta. Esta producción de inhibidor de proteasa puede proteger a la planta de los insectos, disminuyendo las tasas de infestación y el daño físico que sufren los herbívoros. Sin embargo, debido a su relación antagónica con el ácido salicílico (una señal importante en la defensa de patógenos) en algunas especies de plantas, puede resultar en una mayor susceptibilidad a agentes virales y otros patógenos. En Zea mays , el ácido salicílico y JA están mediados por NPR1 (no expresador de genes relacionados con la patogénesis1), que es esencial para evitar que los herbívoros exploten este sistema antagonista. Los gusanos cogolleros ( Spodoptera spp.), A través de mecanismos desconocidos, son capaces de incrementar la actividad de la vía del ácido salicílico en el maíz, resultando en la depresión de la síntesis de JA, pero gracias a la mediación de NPR1 , los niveles de JA no disminuyen en una cantidad significativa.
Derivados
El ácido jasmónico también se convierte en una variedad de derivados, incluido el éster metil jasmonato . Esta conversión es catalizada por la enzima carboxil metiltransferasa del ácido jasmónico. También se puede conjugar con aminoácidos en algunos contextos biológicos. La descarboxilación proporciona la fragancia relacionada jasmona .
Referencias
-
^
Demole, E .; Lederer, E .; Mercier, D. (1962). "Aislamiento y determinación de la estructura del jasmonato de metileno, componente odorizante característico de la esencia del jazmín" [Aislamiento y determinación de la estructura del jasmonato de metilo, el constituyente aromático [que es] característico del aceite esencial de jazmín]. Helvetica Chimica Acta (en francés). 45 : 675–685. doi : 10.1002 / hlca.19620450233 .
- Chapuis, Christian (diciembre de 2011). "La química y el legado creativo del jasmonato de metilo y la hediona" . Perfumista y saborista . 36 : 36–48.
- ^ Dewick, Paul (2009). Productos medicinales naturales: un enfoque biosintético . Reino Unido: John Wiley & Sons, Ltd. pp. 42 -53. ISBN 978-0-470-74168-9.
- ^ Delker, C .; Stenzel, I .; Hause, B .; Miersch, O .; Feussner, I .; Wasternack, C. (2006). "Biosíntesis de jasmonato en Arabidopsis thaliana - Enzimas, Productos, Regulación". Biología Vegetal . 8 (3): 297-306. doi : 10.1055 / s-2006-923935 . PMID 16807821 .
- ^ Gális, I .; Gaquerel, E .; Pandey, SP; Baldwin, INT (2009). "Mecanismos moleculares subyacentes a la memoria de la planta en respuestas de defensa mediadas por JA". Planta, célula y medio ambiente . 32 (6): 617–27. doi : 10.1111 / j.1365-3040.2008.01862.x . PMID 18657055 .
- ^ Lutz, Diana (2012). Revelada una parte clave del sistema de respuesta rápida de las plantas. Universidad de Washington en St. Louis. http://news.wustl.edu/news/Pages/23979.aspx
- ^ Zavala, JA; Patankar, AG; Gase, K .; Hui, D .; Baldwin, IT (2004). "La manipulación de la producción de inhibidores endógenos de tripsina proteinasa en Nicotiana attenuata demuestra su función como defensas antiherbívoras" . Fisiología vegetal . 134 (3): 1181-1190. doi : 10.1104 / pp.103.035634 . PMC 389942 . PMID 14976235 .
- ^ Los efectos de los tratamientos con bacterias y ácido jasmónico en insectos de canola . 2008.
- ^ "Éxito para el control de plagas de las plantas" . BBC News . 2008-10-07 . Consultado el 5 de mayo de 2010 .
- ^ Worrall, D .; Holroyd, GH; Moore, JP; Glowacz, M .; Croft, P .; Taylor, JE; Paul, ND; Roberts, MR (2012). "El tratamiento de semillas con activadores de defensa vegetal genera un cebado duradero de resistencia a plagas y patógenos" (PDF) . Nuevo fitólogo . 193 (3): 770–778. doi : 10.1111 / j.1469-8137.2011.03987.x . PMID 22142268 .
- ^ Granjero, EE; Johnson, RR; Ryan, CA (marzo de 1992). "Regulación de la expresión de genes inhibidores de proteinasa por jasmonato de metilo y ácido jasmónico" . Fisiología vegetal . 98 (3): 995–1002. doi : 10.1104 / pp.98.3.995 . ISSN 0032-0889 . PMC 1080300 . PMID 16668777 .
- ^ Fouad, Hany Ahmed; El-Gepaly, Hosam Mohamed Khalil Hammam; Fouad, Osama Ahmed (26 de agosto de 2016). "Nanosílice y ácido jasmónico como métodos alternativos para el control de Tuta absoluta (Meyrick) en cultivo de tomate en condiciones de campo". Archivos de Fitopatología y Protección Vegetal . 49 (13-14): 362-370. doi : 10.1080 / 03235408.2016.1219446 . ISSN 0323-5408 . S2CID 89119004 .
- ^ Lyons, R .; Modales, JM; Kazán, K. (2013). "Biosíntesis de jasmonato y señalización en monocotiledóneas: una descripción comparativa". Informes de células vegetales . 32 (6): 815–27. doi : 10.1007 / s00299-013-1400-y . PMID 23455708 . S2CID 10778582 .
- ↑ a b Ballaré, Carlos L. (2011). "Defensas inducidas por jasmonato: una historia de inteligencia, colaboradores y bribones". Tendencias en ciencia de las plantas . 16 (5): 249–57. doi : 10.1016 / j.tplants.2010.12.001 . PMID 21216178 .
- ^ Seo, HS; Song, JT; Cheong, JJ; Lee, YH; Lee, YW; Hwang, I .; Lee, JS; Choi, YD (10 de abril de 2001). "Carboxil metiltransferasa del ácido jasmónico: una enzima clave para las respuestas de las plantas reguladas por jasmonato" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 98 (8): 4788–4793. Código bibliográfico : 2001PNAS ... 98.4788S . doi : 10.1073 / pnas.081557298 . ISSN 0027-8424 . PMC 31912 . PMID 11287667 .
- Sankawa, Ushio; Barton, Derek HR; Nakanishi, Koji; Meth-Cohn, Otto, eds. (1999). Química integral de productos naturales: policétidos y otros metabolitos secundarios, incluidos los ácidos grasos y sus derivados . Pergamon Press. ISBN 978-0-08-043153-6.

