Tioéster - Thioester
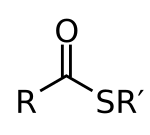
En química, los tioésteres son compuestos con el grupo funcional R – S – CO – R '. Son análogos a los ésteres de carboxilato con el azufre en el tioéster desempeñando el papel de oxígeno de enlace en el éster de carboxilato. Son el producto de la esterificación entre un ácido carboxílico y un tiol . En bioquímica , los tioésteres más conocidos son derivados de la coenzima A , por ejemplo, acetil-CoA .
Síntesis
La ruta más típica al tioéster implica la reacción de un cloruro de ácido con una sal de metal alcalino de un tiol:
- RSNa + R′COCl → R′COSR + NaCl
Otra ruta común implica el desplazamiento de haluros por la sal de metal alcalino de un ácido tiocarboxílico . Por ejemplo, los ésteres de tioacetato se preparan comúnmente mediante alquilación de tioacetato de potasio :
- CH 3 COSK + RX → CH 3 COSR + KX
Rara vez se practica la alquilación análoga de una sal de acetato. La alquilación se puede realizar utilizando bases de Mannich y el ácido tiocarboxílico:
- CH 3 COSH + R ′ 2 NCH 2 OH → CH 3 COSCH 2 NR ′ 2 + H 2 O
Los tioésteres se pueden preparar por condensación de tioles y ácidos carboxílicos en presencia de agentes deshidratantes:
- RSH + R′CO 2 H → RSC (O) R ′ + H 2 O
Un agente de deshidratación típico es DCC . También se han informado esfuerzos para mejorar la sostenibilidad de la síntesis de tioéster utilizando un reactivo de acoplamiento más seguro T3P y un disolvente más ecológico ciclopentanona . Los anhídridos de ácido y algunas lactonas también producen tioésteres tras el tratamiento con tioles en presencia de una base.
Los tioésteres se pueden preparar convenientemente a partir de alcoholes mediante la reacción de Mitsunobu , usando ácido tioacético .
También surgen por carbonilación de alquinos y alquenos en presencia de tioles.
Reacciones
Los tioésteres se hidrolizan a tioles y al ácido carboxílico:
- RC (O) SR '+ H 2 O → RCO 2 H + RSH
El centro de carbonilo en los tioésteres es más reactivo con los nucleófilos de amina para dar amidas :
En una reacción relacionada, pero utilizando un metal blando para capturar el tiolato, los tioésteres se convierten en ésteres. Los tioésteres proporcionan quimioselectividad útil en la síntesis de biomoléculas.
Una reacción exclusiva de los tioésteres es el acoplamiento de Fukuyama , en el que el tioéster se acopla con un haluro de organozinc mediante un catalizador de paladio para dar una cetona.

Bioquímica

Los tioésteres son productos intermedios comunes en muchas reacciones biosintéticas, incluida la formación y degradación de ácidos grasos y mevalonato , precursor de los esteroides. Los ejemplos incluyen malonil-CoA , acetoacetil-CoA , propionil-CoA , cinamoil-CoA y tioésteres de proteína transportadora de acilo (ACP). La acetogénesis procede mediante la formación de acetil-CoA . La biosíntesis de la lignina , que comprende una gran fracción de la biomasa terrestre de la Tierra, procede a través de un derivado tioéster del ácido cafeico . Estos tioésteres surgen de forma análoga a los preparados sintéticamente, con la diferencia de que el agente deshidratante es ATP. Además, los tioésteres juegan un papel importante en el marcado de proteínas con ubiquitina , que marca la proteína para su degradación.
La oxidación del átomo de azufre en los tioésteres (tiolactonas) se postula en la bioactivación de los profármacos antitrombóticos ticlopidina, clopidogrel y prasugrel.
Los tioésteres y el origen de la vida
Como se postula en un "mundo tioéster", los tioésteres son posibles precursores de la vida. Como explica Christian de Duve :
Es revelador que los tioésteres son intermedios obligatorios en varios procesos clave en los que el ATP se usa o se regenera. Los tioésteres participan en la síntesis de todos los ésteres , incluidos los que se encuentran en los lípidos complejos . También participan en la síntesis de otros componentes celulares, incluidos péptidos , ácidos grasos , esteroles , terpenos , porfirinas y otros. Además, los tioésteres se forman como intermediarios clave en varios procesos particularmente antiguos que dan como resultado el ensamblaje de ATP. En ambos casos, el tioéster está más cerca que el ATP del proceso que usa o produce energía. En otras palabras, los tioésteres podrían haber desempeñado el papel de ATP en un "mundo de tioésteres" inicialmente desprovisto de ATP. Eventualmente, [estos] tioésteres podrían haber servido para marcar el comienzo de ATP a través de su capacidad para apoyar la formación de enlaces entre grupos fosfato .
Sin embargo, debido al alto cambio de energía libre de la hidrólisis del tioéster y, en consecuencia, a sus bajas constantes de equilibrio, es poco probable que estos compuestos se hayan acumulado abióticamente en un grado significativo, especialmente en condiciones de ventilación hidrotermal.
Tionoésteres
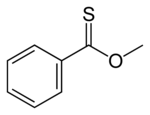
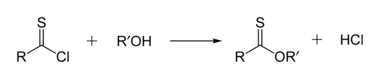
Los tionoésteres son isoméricos con los tioésteres. En un tionoéster, el azufre reemplaza al oxígeno del carbonilo en un éster. El tionobenzoato de metilo es C 6 H 5 C (S) OCH 3 . Estos compuestos se preparan típicamente mediante la reacción del cloruro de tioacilo con un alcohol.
También se pueden preparar mediante la reacción del reactivo de Lawesson con ésteres o mediante el tratamiento de sales de pinner con sulfuro de hidrógeno. Como alternativa, se pueden preparar varios tionoésteres mediante la transesterificación de un metil tionoéster existente con un alcohol en condiciones catalizadas por una base.