Metoximetanol - Methoxymethanol
|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
Metoximetanol |
|
| Otros nombres
Formaldehído metil hemiacetal
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 1900186 | |
| CHEBI | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.022.476 |
| Número CE | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 2 H 6 O 2 | |
| Masa molar | 62.068 g · mol −1 |
| Densidad | 0,948 |
| Peligros | |
| Pictogramas GHS |
  
|
| Palabra de señal GHS | Advertencia |
| H226 , H302 , H371 | |
| P210 , P233 , P240 , P241 , P242 , P243 , P260 , P264 , P270 , P280 , P301 + 312 , P303 + 361 + 353 , P309 + 311 , P330 , P370 + 378 , P403 + 235 , P405 , P501 | |
| punto de inflamabilidad | 39,9 ° C (103,8 ° F; 313,0 K) |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
| Referencias de Infobox | |
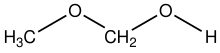
El metoximetanol es un compuesto químico que es tanto un éter como un alcohol , un hemiformal . La fórmula estructural se puede escribir como CH 3 OCH 2 OH. Ha sido descubierto en el espacio.
Formación
El metoximetanol se forma espontáneamente cuando se mezcla una solución acuosa de formaldehído y metanol . o cuando se burbujea formaldehído a través de metanol.
En el espacio, se puede formar metoximetanol cuando reaccionan los radicales de metanol (CH 2 OH o CH 3 O). Estos son productos de radiólisis que se obtienen cuando la luz ultravioleta o los rayos cósmicos inciden en el metanol congelado.
El metanol puede reaccionar con dióxido de carbono e hidrógeno a 80 ° C y algo de presión con un catalizador de rutenio o cobalto, para producir algo de metoximetanol.
Propiedades
Las diferentes conformaciones de la molécula son Gauche-gauce (Gg), Gauche-gauce '(Gg') y Trans-gauche (Tg).
