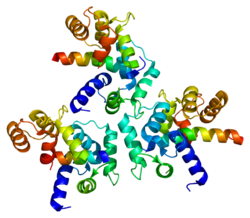
Ca v 1.3 -Cav1.3
Canal de calcio, dependiente de voltaje, tipo L, subunidad alfa 1D (también conocida como Ca v 1.3 ) es una proteína que en humanos está codificada por el gen CACNA1D . Los canales Ca v 1.3 pertenecen a la familia Ca v 1, que forman corrientes de calcio tipo L y son sensibles a la inhibición selectiva por dihidropiridinas (DHP).
Estructura y función
Los canales de calcio dependientes de voltaje (VDCC) son selectivamente permeables a los iones de calcio y median el movimiento de estos iones dentro y fuera de las células excitables. En el potencial de reposo, estos canales están cerrados, pero cuando el potencial de membrana se despolariza, estos canales se abren. La entrada de iones de calcio en la célula puede iniciar una gran variedad de procesos dependientes del calcio, que incluyen la contracción muscular , la expresión génica y la secreción . Los procesos dependientes del calcio se pueden detener reduciendo los niveles de calcio intracelular, lo que, por ejemplo, se puede lograr mediante bombas de calcio .
Los canales de calcio dependientes de voltaje son múltiples proteínas compuestas por subunidades α1, β, α2δ y γ. La subunidad principal es α1, que forma el poro de selectividad, el sensor de voltaje y el aparato de activación de los VDCC. En los canales Ca v 1.3, la subunidad α1 es α1D. Esta subunidad diferencia los canales Ca v 1.3 de otros miembros de la familia Ca v 1, como el Ca v 1.2 predominante y mejor estudiado , que tiene una subunidad α1C. La importancia de la subunidad α1 también significa que es el objetivo principal de los bloqueadores de los canales de calcio como las dihidropiridinas . Las restantes subunidades β, α2δ y γ tienen funciones auxiliares.
La subunidad α1 tiene cuatro dominios homólogos , cada uno con seis segmentos transmembrana. Dentro de cada dominio homólogo, el cuarto segmento transmembrana (S4) está cargado positivamente, a diferencia de los otros cinco segmentos hidrófobos . Esta característica permite que S4 funcione como sensor de voltaje. Las subunidades alfa-1D pertenecen a la familia Ca v 1, que se caracteriza por corrientes de calcio de tipo L. Específicamente, las subunidades α1D confieren activación de bajo voltaje e inactivación lenta de las corrientes de Ca 2+ , ideales para funciones fisiológicas particulares como la liberación de neurotransmisores en las células ciliadas internas de la cóclea .
Las propiedades biofísicas de los canales de Ca v 1.3 están estrechamente reguladas por un dominio modulador C-terminal (CTM), que afecta tanto a la dependencia del voltaje de la activación como a la inactivación dependiente de Ca 2+ . Ca v 1.3 tiene una baja afinidad por la DHP y se activa a potenciales de membrana por debajo del umbral, lo que los hace ideales para desempeñar un papel en el marcapasos cardíaco .
Regulación
Splicing alternativo
El empalme alternativo postranscripcional de Ca v 1.3 es un mecanismo regulador extenso y vital. El empalme alternativo puede afectar significativamente las propiedades de compuerta del canal. Comparable al empalme alternativo de los transcritos de Ca v 1.2, que confiere especificidad funcional, se ha descubierto recientemente que el empalme alternativo, particularmente en el extremo C-terminal, afecta las propiedades farmacológicas de Ca v 1.3. Sorprendentemente, se han informado diferencias de hasta 8 veces en la sensibilidad a la dihidropiridina entre isoformas empalmadas alternativamente.
Retroalimentación negativa
Los canales de Ca v 1.3 están regulados por retroalimentación negativa para lograr la homeostasis del Ca 2+ . Los iones de calcio son un segundo mensajero crítico , intrínseco a la transducción de señales intracelulares . Los niveles de calcio extracelular se aproximan a ser 12000 veces mayores que los niveles intracelulares. Durante los procesos dependientes del calcio, el nivel intracelular de calcio aumenta hasta 100 veces. Es de vital importancia regular este gradiente de calcio, sobre todo porque los niveles altos de calcio son tóxicos para la célula y pueden inducir la apoptosis .
La calmodulina unida a Ca 2+ (CaM) interactúa con Ca v 1.3 para inducir la inactivación dependiente del calcio (CDI). Recientemente, se ha demostrado que la edición de ARN de las transcripciones de Ca v 1.3 es esencial para CDI. Contrariamente a lo esperado, la edición de ARN no solo atenúa la unión de CaM, sino que debilita la unión previa de calmodulina libre de Ca 2+ (apoCaM) a los canales. El resultado es que CDI se puede sintonizar continuamente mediante cambios en los niveles de CaM.
Significación clínica
Audiencia
Los canales Ca v 1.3 se expresan ampliamente en humanos. En particular, su expresión predomina en las células ciliadas internas de la cóclea (IHC). Se ha demostrado a través de experimentos de pinzamiento de parche que Ca v 1.3 es esencial para el desarrollo normal de IHC y la transmisión sináptica . Por lo tanto, se requiere Ca v 1.3 para una audición adecuada.
Células cromafines
Ca v 1.3 se expresan densamente en células cromafines . La activación de bajo voltaje y la inactivación lenta de estos canales los hace ideales para controlar la excitabilidad en estas células. La secreción de catecolaminas de las células cromafines es particularmente sensible a las corrientes de tipo L, asociadas con Ca v 1.3. Las catecolaminas tienen muchos efectos sistémicos en múltiples órganos. Además, los canales de tipo L son responsables de la exocitosis en estas células.
Neurodegeneración
La enfermedad de Parkinson es la segunda enfermedad neurodegenerativa más común , en la que la muerte de las células productoras de dopamina en la sustancia negra del mesencéfalo conduce a una función motora deteriorada, quizás mejor caracterizada por temblores . La evidencia reciente sugiere que los canales de Ca v 1.3 Ca 2+ de tipo L contribuyen a la muerte de las neuronas dopaminérgicas en pacientes con enfermedad de Parkinson. La actividad basal de estas neuronas también depende de los canales de Ca 2+ de tipo L , como Ca v 1.3. La actividad de marcapasos continua impulsa los transitorios de calcio dendríticos y somáticos intracelulares permanentes, lo que parece hacer que las neuronas dopaminérgicas de la sustancia negra sean vulnerables a los factores estresantes que contribuyen a su muerte. Por tanto, la inhibición de los canales de tipo L, en particular Ca v 1.3, protege contra la patogénesis del Parkinson en algunos modelos animales. Un ensayo clínico de fase III ( STEADY-PD III ) que probó esta hipótesis en pacientes con Parkinson temprano no demostró eficacia para frenar la progresión del Parkinson.
La inhibición de Ca v 1.3 se puede lograr utilizando bloqueadores de los canales de calcio, como las dihidropiridinas (DHP). Estos medicamentos se utilizan desde hace décadas para tratar la hipertensión arterial y la angina de pecho. Esto se debe a sus potentes propiedades vasorrelajantes, que están mediadas por la inhibición de los canales de calcio de tipo L Ca v 1.2 en el músculo liso arterial. Por lo tanto, las reacciones hipotensivas (y el edema de la pierna) se consideran efectos secundarios limitantes de la dosis cuando se usan DHP para inhibir el canal Ca v 1.3 en el cerebro. Ante este problema, se ha intentado descubrir bloqueadores selectivos de canales de Ca v 1.3. Se ha afirmado que un candidato es un inhibidor potente y altamente selectivo de Ca v 1.3. Este compuesto, 1- (3-clorofenetil) -3-ciclopentilpirimidin-2,4,6- (1 H , 3 H , 5 H ) -triona se presentó por tanto como un candidato para el tratamiento futuro del Parkinson. Sin embargo, su selectividad y potencia no se pudo confirmar en dos estudios independientes de otros dos grupos. Uno de ellos incluso informó cambios en la compuerta inducidos por este fármaco, que indican efectos de activación del canal en lugar de bloqueo.
Cancer de prostata
La evidencia reciente de experimentos de inmunotinción muestra que CACNA1D se expresa altamente en cánceres de próstata en comparación con tejidos de próstata benignos. Bloquear los canales de tipo L o anular la expresión génica de CACNA1D suprimió significativamente el crecimiento celular en las células del cáncer de próstata. Es importante reconocer que esta asociación no representa un vínculo causal entre niveles altos de proteína α1D y cáncer de próstata. Se necesita más investigación para explorar el papel de la sobreexpresión del gen CACNA1D en el crecimiento de células de cáncer de próstata.
Aldosteronismo
Las mutaciones somáticas de novo en regiones conservadas dentro de la puerta de activación del canal de su subunidad α1 formadora de poros ( CACNA1D) provocan una producción excesiva de aldosterona en los adenomas productores de aldosterona (APA), lo que da como resultado aldosteronismo primario , que causa hipertensión arterial resistente al tratamiento . Estas mutaciones permiten una mayor afluencia de Ca 2+ a través de Cav1.3, que a su vez desencadena la producción de aldosterona dependiente de Ca 2+ . El número de mutaciones APA validadas crece constantemente. En casos raros, también se han encontrado mutaciones de APA como mutaciones de la línea germinal en personas con trastornos del desarrollo neurológico de diferente gravedad, incluido el trastorno del espectro autista.
Ver también
Referencias
Otras lecturas
- Williams ME, Feldman DH, McCue AF, Brenner R, Velicelebi G, Ellis SB, Harpold MM (enero de 1992). "Estructura y expresión funcional de las subunidades alfa 1, alfa 2 y beta de un nuevo subtipo de canal de calcio neuronal humano". Neurona . 8 (1): 71–84. doi : 10.1016 / 0896-6273 (92) 90109-Q . PMID 1309651 . S2CID 39341712 .
- Seino S, Chen L, Seino M, Blondel O, Takeda J, Johnson JH, Bell GI (enero de 1992). "Clonación de la subunidad alfa 1 de un canal de calcio dependiente de voltaje expresado en células beta pancreáticas" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 89 (2): 584–8. Código bibliográfico : 1992PNAS ... 89..584S . doi : 10.1073 / pnas.89.2.584 . PMC 48283 . PMID 1309948 .
- Seino S, Yamada Y, Espinosa R, Le Beau MM, Bell GI (agosto de 1992). "Asignación del gen que codifica la subunidad alfa 1 del canal de calcio neuroendocrino / de tipo cerebral (CACNL1A2) al cromosoma 3 humano, banda p14.3". Genómica . 13 (4): 1375–7. doi : 10.1016 / 0888-7543 (92) 90078-7 . PMID 1324226 .
- Chin HM, Kozak CA, Kim HL, Mock B, McBride OW (diciembre de 1991). "Un gen de la subunidad alfa 1 del canal de calcio de tipo L del cerebro (CCHL1A2) se asigna al cromosoma 14 del ratón y al cromosoma 3 humano" . Genómica (manuscrito enviado). 11 (4): 914–9. doi : 10.1016 / 0888-7543 (91) 90014-6 . PMID 1664412 .
- Mori Y, Friedrich T, Kim MS, Mikami A, Nakai J, Ruth P, Bosse E, Hofmann F, Flockerzi V, Furuichi T (abril de 1991). "Estructura primaria y expresión funcional del ADN complementario de un canal de calcio cerebral". Naturaleza . 350 (6317): 398–402. Código Bibliográfico : 1991Natur.350..398M . doi : 10.1038 / 350398a0 . PMID 1849233 . S2CID 4370532 .
- Yamada Y, Masuda K, Li Q, Ihara Y, Kubota A, Miura T, Nakamura K, Fujii Y, Seino S, Seino Y (mayo de 1995). "Las estructuras de los genes de la subunidad alfa 1 del canal de calcio humano (CACNL1A2) y la subunidad beta (CACNLB3)". Genómica . 27 (2): 312–9. doi : 10.1006 / geno.1995.1048 . PMID 7557998 .
- Puro DG, Hwang JJ, Kwon OJ, Chin H (abril de 1996). "Caracterización de un canal de calcio de tipo L expresado por células de Müller (gliales) retinianas humanas" . Investigación del cerebro. Investigación del cerebro molecular (manuscrito enviado). 37 (1–2): 41–8. doi : 10.1016 / 0169-328X (96) 80478-5 . PMID 8738134 .
- Yang SN, Larsson O, Bränström R, Bertorello AM, Leibiger B, Leibiger IB, Moede T, Köhler M, Meister B, Berggren PO (agosto de 1999). "La sintaxina 1 interactúa con el subtipo L (D) de los canales de Ca (2+) activados por voltaje en las células beta pancreáticas" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 96 (18): 10164–9. doi : 10.1073 / pnas.96.18.10164 . PMC 17860 . PMID 10468580 .
- Bell DC, Butcher AJ, Berrow NS, Page KM, Brust PF, Nesterova A, Stauderman KA, Seabrook GR, Nürnberg B, Dolphin AC (febrero de 2001). "Propiedades biofísicas, farmacología y modulación de las corrientes de calcio dependientes de voltaje de tipo L (alfa (1D), Ca (V) 1.3) neuronales humanas". Revista de neurofisiología . 85 (2): 816–27. doi : 10.1152 / jn.2001.85.2.816 . PMID 11160515 .
- Rosenthal R, Thieme H, Strauss O (abril de 2001). "El receptor 2 del factor de crecimiento de fibroblastos (FGFR2) en las neuronas del cerebro y las células epiteliales del pigmento de la retina actúan mediante la estimulación de los canales de tipo L neuroendocrinos (Ca (v) 1.3)". Revista FASEB . 15 (6): 970–7. doi : 10.1096 / fj.00-0188com . PMID 11292657 .
- Davare MA, Avdonin V, Hall DD, Peden EM, Burette A, Weinberg RJ, Horne MC, Hoshi T, Hell JW (julio de 2001). "Un complejo de señalización del receptor adrenérgico beta2 ensamblado con el canal Ca2 + Cav1.2". Ciencia . 293 (5527): 98–101. doi : 10.1126 / science.293.5527.98 . PMID 11441182 .
- Namkung Y, Skrypnyk N, Jeong MJ, Lee T, Lee MS, Kim HL, Chin H, Suh PG, Kim SS, Shin HS (octubre de 2001). "Requisito para la subunidad alfa (1D) del canal de Ca (2+) de tipo L en la generación de células beta pancreáticas posnatales" . La Revista de Investigación Clínica . 108 (7): 1015–22. doi : 10.1172 / JCI13310 . PMC 200955 . PMID 11581302 .
- Stokes L, Gordon J, Grafton G (mayo de 2004). "Canales de Ca2 + de tipo L no dependientes de voltaje en células T humanas: farmacología y caracterización molecular de las principales subunidades beta auxiliares y formadoras de poros alfa" . La revista de química biológica . 279 (19): 19566–73. doi : 10.1074 / jbc.M401481200 . PMID 14981074 .
- Qu Y, Baroudi G, Yue Y, Boutjdir M (junio de 2005). "Mecanismo molecular novedoso que implica el canal de calcio de tipo L alfa1D (Cav1.3) en la bradicardia sinusal asociada a autoinmunidad" . Circulación . 111 (23): 3034–41. doi : 10.1161 / CIRCULATIONAHA.104.517326 . PMID 15939813 .
- Baroudi G, Qu Y, Ramadan O, Chahine M, Boutjdir M (octubre de 2006). "La activación de la proteína quinasa C inhibe el canal de calcio Cav1.3 en el sitio de fosforilación de la serina 81 NH2-terminal". Revista estadounidense de fisiología. Fisiología cardíaca y circulatoria . 291 (4): H1614-22. doi : 10.1152 / ajpheart.00095.2006 . PMID 16973824 .
- Olsen JV, Blagoev B, Gnad F, Macek B, Kumar C, Mortensen P, Mann M (noviembre de 2006). "Dinámica de fosforilación global, in vivo y específica del sitio en redes de señalización" . Celular . 127 (3): 635–48. doi : 10.1016 / j.cell.2006.09.026 . PMID 17081983 . S2CID 7827573 .
enlaces externos
- CACNA1D + proteína, + humano en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- Descripción general de toda la información estructural disponible en la PDB para UniProt : Q01668 (subunidad alfa-1D del canal de calcio de tipo L dependiente del voltaje) en PDBe-KB .
Este artículo incorpora texto de la Biblioteca Nacional de Medicina de los Estados Unidos , que es de dominio público .