2,5-dimetilfurano - 2,5-Dimethylfuran

|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
2,5-dimetilfurano |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.009.923 |
| Número CE | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 6 H 8 O | |
| Masa molar | 96,13 |
| Apariencia | Líquido |
| Densidad | 0,8897 g / cm 3 |
| Punto de fusion | −62 ° C (−80 ° F; 211 K) |
| Punto de ebullición | 92 a 94 ° C (198 a 201 ° F; 365 a 367 K) |
| Insoluble | |
| -66,37 · 10 −6 cm 3 / mol | |
|
Índice de refracción ( n D )
|
1,44 - 1,442 |
| Peligros | |
| Principales peligros | Muy inflamable, nocivo |
| punto de inflamabilidad | −1 ° C (30 ° F; 272 K) |
| 285,85 ° C (546,53 ° F; 559,00 K) | |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El 2,5-dimetilfurano es un compuesto heterocíclico con la fórmula (CH 3 ) 2 C 4 H 2 O. Aunque a menudo se abrevia DMF , no debe confundirse con dimetilformamida . Un derivado del furano , este compuesto simple es un biocombustible potencial , derivado de la celulosa.
Producción
La fructosa se puede convertir en 2,5-dimetilfurano en un proceso catalítico de conversión de biomasa en líquido . La conversión de fructosa en DMF se realiza mediante hidroximetilfurfural .
La fructosa se obtiene a partir de la glucosa, un componente básico de la celulosa.
Potencial como biocombustible
El DMF tiene una serie de atractivos como biocombustible . Tiene una densidad de energía un 40% mayor que la del etanol , lo que lo hace comparable a la gasolina (gasolina). También es químicamente estable y, al ser insoluble en agua, no absorbe la humedad de la atmósfera. La evaporación del dimetilfurano durante el proceso de producción también requiere alrededor de un tercio menos de energía que la evaporación del etanol, aunque tiene un punto de ebullición unos 14 ° C más alto, a 92 ° C, en comparación con los 78 ° C del etanol.
La capacidad de producir dimetilfurano de manera eficiente y rápida a partir de fructosa, que se encuentra en frutas y algunas hortalizas de raíz , o de glucosa, que puede derivarse del almidón y la celulosa , todos ampliamente disponibles en la naturaleza, se suma a la atracción del dimetilfurano, aunque deben tenerse en cuenta cuestiones de seguridad examinado. El bioetanol y el biodiésel son actualmente los principales biocombustibles líquidos.
La relación estequiométrica de aire / combustible de dimetilfurano es de 10,72, en comparación con el etanol de 8,95 y la gasolina de 14,56. Esto significa que la quema de dimetilfurano requiere aproximadamente un 33% menos de aire que la misma cantidad de gasolina, pero aproximadamente un 20% más de aire que la misma cantidad de etanol.
El poder calorífico del dimetilfurano líquido es 33,7 MJ / kg, en comparación con 26,9 MJ / kg para el etanol y 43,2 MJ / kg para la gasolina. El índice de octano de investigación (RON) del dimetilfurano es 119. El calor latente de vaporización a 20 ° C es 31,91 kJ / mol. Pruebas recientes en un motor de gasolina de un solo cilindro encontraron que la eficiencia térmica de la combustión de dimetilfurano es similar a la de la gasolina.
Otros usos
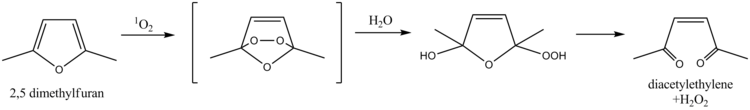
El 2,5-dimetilfurano sirve como depurador de oxígeno singlete , una propiedad que se ha aprovechado para la determinación de oxígeno singlete en aguas naturales. El mecanismo implica una reacción de Diels-Alder seguida de hidrólisis , que finalmente conduce a diacetiletileno y peróxido de hidrógeno como productos. Más recientemente, se ha utilizado alcohol furfurílico con el mismo propósito.
También se ha propuesto el 2,5-dimetilfurano como patrón interno para la espectroscopia de RMN . El 2,5-dimetilfurano tiene singletes en su espectro de RMN de 1 H en δ 2,2 y 5,8; los singletes dan integraciones confiables, mientras que las posiciones de los picos no interfieren con muchos analitos. El compuesto también tiene un punto de ebullición apropiado de 92 ° C que evita las pérdidas por evaporación, pero se elimina fácilmente.
Papel en la química de los alimentos
El 2,5-dimetilfurano se forma tras la degradación térmica de algunos azúcares y se ha identificado en cantidades mínimas como un componente de los azúcares caramelizados .
Toxicología
El 2,5-dimetilfurano juega un papel en el mecanismo de neurotoxicidad del hexano en humanos. Junto con hexano-2,5-diona y 4,5-dihidroxi-2-hexanona, es uno de los principales metabolitos del hexano .
El 2,5-dimetilfurano se ha identificado como uno de los componentes del humo del cigarro con baja toxicidad ciliar (capacidad de afectar negativamente a los cilios del tracto respiratorio que son responsables de eliminar las partículas extrañas). Su concentración en sangre se puede utilizar como biomarcador para fumar .
La comparación de las fichas de datos de seguridad muestra que la manipulación humana del 2,5-dimetilfurano es aproximadamente tan peligrosa como la manipulación de gasolina.
