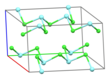
Cloruro de itrio (III) - Yttrium(III) chloride
 Parte de una capa en la estructura cristalina de YCl 3
|
|||
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombres IUPAC
Cloruro de itrio (III)
Tricloruro de itrio |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.030.716 |
||
| Número CE | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| YCl 3 | |||
| Masa molar | 195,265 g / mol | ||
| Apariencia | Blanco sólido | ||
| Densidad | 2,61 g / cm 3 | ||
| Punto de fusion | 721 ° C (1330 ° F; 994 K) | ||
| Punto de ebullición | 1.482 ° C (2.700 ° F; 1.755 K) | ||
| 751 g / L (20 ° C) | |||
| Solubilidad | 601 g / L de etanol (15 ° C) 606 g / L de piridina (15 ° C) |
||
| Estructura | |||
| Monoclínico , MS16 | |||
| C2 / m, No. 12 | |||
|
a = 0,692 nm, b = 1,194 nm, c = 0,644 nm
α = 90 °, β = 111 °, γ = 90 °
|
|||
|
Unidades de fórmula ( Z )
|
4 | ||
| Riesgos | |||
| Pictogramas GHS |
  
|
||
| Palabra de señal GHS | Peligro | ||
| H302 , H312 , H315 , H319 , H332 , H335 | |||
| P261 , P264 , P270 , P271 , P280 , P301 + 312 , P302 + 352 , P304 + 312 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P322 , P330 , P332 + 313 , P337 + 313 , P362 , P363 , P403 + 233 , P405 , P501 | |||
| punto de inflamabilidad | No es inflamable | ||
| Compuestos relacionados | |||
|
Otros aniones
|
Fluoruro de itrio (III) Bromuro de itrio (III) Yoduro de itrio (III) |
||
|
Otros cationes
|
Cloruro de escandio (III) Cloruro de lantano (III) Cloruro de actinio (III) |
||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
El cloruro de itrio (III) es un compuesto inorgánico de itrio y cloruro . Existe en dos formas, el hidrato (YCl 3 (H 2 O) 6 ) y una forma anhidra (YCl 3 ). Ambos son sólidos incoloros, altamente solubles en agua y delicuescentes .
Estructura
El YCl 3 sólido adopta una estructura cúbica con iones de cloruro e iones de itrio compactos que llenan un tercio de los orificios octaédricos y el octaedro de YCl 6 resultante comparte tres bordes con octaedros adyacentes, lo que le da una estructura en capas. Esta estructura es compartida por una variedad de compuestos, en particular AlCl 3 .
Preparación y reacciones
El YCl 3 a menudo se prepara por la " ruta del cloruro de amonio " , partiendo de Y 2 O 3 o cloruro u oxicloruro hidratado. o YCl 3 · 6H 2 O. Estos métodos producen (NH 4 ) 2 [YCl 5 ]:
- 10 NH 4 Cl + Y 2 O 3 → 2 (NH 4 ) 2 [YCl 5 ] + 6 NH 3 + 3 H 2 O
- YCl 3 · 6H 2 O + 2 NH 4 Cl → (NH 4 ) 2 [YCl 5 ] + 6 H 2 O
El pentacloruro se descompone térmicamente de acuerdo con la siguiente ecuación:
- (NH 4 ) 2 [YCl 5 ] → 2 NH 4 Cl + YCl 3
La reacción de termólisis procede a través de la intermediación de (NH 4 ) [Y 2 Cl 7 ].
El tratamiento de Y 2 O 3 con HCl acuoso produce el cloruro hidratado (YCl 3 · 6H 2 O). Cuando se calienta, esta sal produce oxicloruro de itrio en lugar de volver a la forma anhidra.