Dominio de homología de pleckstrina - Pleckstrin homology domain
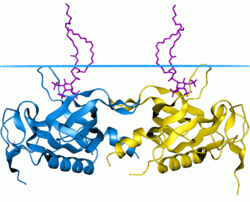 Dominio PH de la tirosina-proteína quinasa BTK
| |||||||||
| Identificadores | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Símbolo | PH | ||||||||
| Pfam | PF00169 | ||||||||
| Clan pfam | CL0266 | ||||||||
| InterPro | IPR001849 | ||||||||
| INTELIGENTE | PH | ||||||||
| PROSITE | PDOC50003 | ||||||||
| SCOP2 | 1dyn / SCOPe / SUPFAM | ||||||||
| Superfamilia OPM | 49 | ||||||||
| Proteína OPM | 1pls | ||||||||
| CDD | cd00821 | ||||||||
| |||||||||
El dominio de homología de pleckstrina ( dominio PH ) o ( PHIP ) es un dominio de proteína de aproximadamente 120 aminoácidos que se encuentra en una amplia gama de proteínas involucradas en la señalización intracelular o como constituyentes del citoesqueleto .
Este dominio puede unir lípidos de fosfatidilinositol dentro de las membranas biológicas (como fosfatidilinositol (3,4,5) -trisfosfato y fosfatidilinositol (4,5) -bisfosfato ), y proteínas como las subunidades βγ de las proteínas G heterotriméricas y la proteína quinasa C . A través de estas interacciones, los dominios de PH juegan un papel en el reclutamiento de proteínas en diferentes membranas , dirigiéndolas a los compartimentos celulares apropiados o permitiéndoles interactuar con otros componentes de las vías de transducción de señales .
Especificidad de unión a lípidos
Los dominios PH individuales poseen especificidades para fosfoinosítidos fosforilados en diferentes sitios dentro del anillo de inositol , por ejemplo, algunos se unen al fosfatidilinositol (4,5) -bisfosfato pero no al fosfatidilinositol (3,4,5) -trisfosfato o fosfatidilinositol (3,4) -bisfosfato , mientras que otros pueden poseer la afinidad necesaria. Esto es importante porque hace que el reclutamiento de diferentes proteínas que contienen dominios PH sean sensibles a las actividades de las enzimas que fosforilan o desfosforilan estos sitios en el anillo de inositol, como la fosfoinositido 3-quinasa o PTEN , respectivamente. Por tanto, tales enzimas ejercen una parte de su efecto sobre la función celular modulando la localización de proteínas de señalización aguas abajo que poseen dominios PH que son capaces de unirse a sus productos fosfolípidos.
Estructura
Se ha determinado la estructura 3D de varios dominios PH. Todos los casos conocidos tienen una estructura común que consta de dos láminas beta antiparalelas perpendiculares , seguidas de una hélice anfipática C-terminal . Los bucles que conectan las cadenas beta difieren enormemente en longitud, lo que hace que el dominio PH sea relativamente difícil de detectar y, al mismo tiempo, proporciona la fuente de la especificidad del dominio. El único residuo conservado entre los dominios PH es un solo triptófano ubicado dentro de la hélice alfa que sirve para nuclear el núcleo del dominio.
Proteínas que contienen dominio PH
Los dominios PH se pueden encontrar en muchas proteínas diferentes, como OSBP o ARF . El reclutamiento para el aparato de Golgi en este caso depende tanto de PtdIns como de ARF. Un gran número de dominios PH tienen poca afinidad por los fosfoinosítidos y se cree que funcionan como dominios de unión a proteínas. Una mirada a todo el genoma en Saccharomyces cerevisiae mostró que la mayoría de los 33 dominios PH de levadura son de hecho promiscuos en la unión a fosfoinosítidos, mientras que solo uno (Num1-PH) se comportó de manera altamente específica. Las proteínas que contienen dominios PH pertenecen a las siguientes familias:
- Pleckstrin , la proteína donde se detectó este dominio por primera vez, es el sustrato principal de la proteína quinasa C en las plaquetas. Pleckstrin contiene dos dominios PH. Las proteínas ARAP contienen cinco dominios PH.
- Proteínas quinasas específicas de serina / treonina tales como la familia Akt / Rac, la proteína quinasa D1 y la familia tripanosomal NrkA.
- Tirosina quinasas no receptoras pertenecientes a la subfamilia Btk / Itk / Tec.
- Sustrato del receptor de insulina 1 ( IRS-1 ).
- Reguladores de pequeñas proteínas G : 64 RhoGEF de la familia Dbl-like, y varias proteínas activadoras de GTPasa como las proteínas ABR, BCR o ARAP.
- Proteínas del citoesqueleto como dinamina (ver InterPro : IPR001401 ), proteína similar a la quinesina de Caenorhabditis elegans unc-104 (ver InterPro : IPR001752 ), espectrina de cadena beta, sintrofina (2 dominios PH) y proteína de migración nuclear de S. cerevisiae NUM1.
- Proteínas de unión a oxiesterol OSBP, S. cerevisiae OSH1 e YHR073w.
- Ceramida quinasa , una lípido quinasa que fosforila las ceramidas a ceramida-1-fosfato.
- Receptores quinasas de proteína G (GRK) de la subfamilia GRK2 (receptores quinasas beta-adrenérgicos): GRK2 y GRK3 .
Subfamilias
- Espectrina / pleckstrina-como InterPro : IPR001605
Ejemplos de
Los genes humanos que codifican proteínas que contienen este dominio incluyen:
- ABR , ADRBK1 , ADRBK2 , AFAP , AFAP1 , AFAP1L1 , AFAP1L2 , AKAP13 , AKT1 , AKT2 , Akt3 , ANLN , APBB1IP , APPL1 , APPL2 , ARHGAP10 , ARHGAP12 , ARHGAP15 , ARHGAP21 , ARHGAP22 , ARHGAP23 , ARHGAP24 , ARHGAP25 , ARHGAP26 , ARHGAP27 , ARHGAP9 , ARHGEF16 , ARHGEF18 , ARHGEF19 , ARHGEF2 , ARHGEF3 , ARHGEF4 , ARHGEF5 , ARHGEF6 , ARHGEF7 , ARHGEF9 , ASEF2 ,
- BMX , BTK ,
- C20orf42 , C9orf100 , CADPS , CADPS2 , CDC42BPA , CDC42BPB , CDC42BPG , CENTA1 , CENTA2 , CENTB1 , CENTB2 , CENTB5 , CENTD1 , CENTD2 , CENTD3 , CENTG1 , CENTG2 , CENTG3 , CERK , CIT , CNKSR1 , CNKSR2 , COL4A3BP , CTGLF1 , CTGLF2 , CTGLF3 , * CTGLF4 , CTGLF5 , CTGLF6 ,
- DAB2IP , DAPP1 , DDEF1 , DDEF2 , DdeFL1 , dEF6 , DEPDC2 , DGKD , DGKH , DGKK , DNM1 , DNM2 , DNM3 , DOCK10 , DOCK11 , DOCK9 , DOK1 , DOK2 , DOK3 , DOK4 , DOK5 , DOK6 , DTGCU2 ,
- EXOC8 ,
- FAM109A , FAM109B , FARP1 , FARP2 , FGD1 , FGD2 , FGD3 , FGD4 , FGD5 , FGD6 ,
- GAB1 , GAB2 , GAB3 , GAB4 , GRB10 , GRB14 , GRB7 ,
- IRS1 , IRS2 , IRS4 , ITK , ITSN1 , ITSN2 ,
- KALRN , KIF1A , KIF1B , KIF1Bbeta ,
- MCF2 , MCF2L , MCF2L2 , MRIP , MYO10 ,
- NET1 , NGEF ,
- OBPH1 , OBSCN , OPHN1 , OSBP , OSBP2 , OSBPL10 , OSBPL11 , OSBPL3 , OSBPL5 , OSBPL6 , OSBPL7 , OSBPL8 , OSBPL9 ,
- PHLDA2 , PHLDA3 , PHLDB1 , PHLDB2 , PHLPP , PIP3-E , plcd1 , plcd4 , plcg1 , plcg2 , PLCH1 , PLCH2 , PLCL1 , PLCL2 , PLD1 , PLD2 , PLEK , PLEK2 , PLEKHA1 , PLEKHA2 , PLEKHA3 , PLEKHA4 , PLEKHA5 , PLEKHA6 , PLEKHA7 , PLEKHA8 , PLEKHB1 , PLEKHB2 , PLEKHC1 , PLEKHF1 , PLEKHF2 , PLEKHG1 , PLEKHG2 , PLEKHG3 , PLEKHG4 , PLEKHG5 , PLEKHG6 , PLEKHH1 , PLEKHH2 , PLEKHH3 , PLEKHJ1 , PLEKHK1 , PLEKHM1 , PLEKHM2 , PLEKHO1 , PLEKHQ1 , PREX1 , PRKCN , PRKD1 , PRKD2 , PRKD3 , PSCD1 , PSCD2 , PSCD3 , PSCD4 , PSD , PSD2 , PSD3 , PSD4 , RALGPS1 , RALGPS2 , RAPH1 ,
- RASA1 , RASA2 , RASA3 , RASA4 , RASAL1 , RASGRF1 , RGNEF , ROCK1 , ROCK2 , RTKN ,
- SBF1 , SBF2 , SCAP2 , SGEF , sh2b , SH2B1 , SH2B2 , sh2b3 , SH3BP2 , SKAP1 , SKAP2 , SNTA1 , SNTB1 , SNTB2 , SOS1 , SOS2 , SPATA13 , SPNB4 , SPTBN1 , SPTBN2 , SPTBN4 , SPTBN5 , STAP1 , SWAP70 , SYNGAP1 ,
- TBC1D2 , TEC , TIAM1 , TRIO , TRIOBP , TYL ,
- URP1 , URP2 ,
- VAV-1 , VAV2 , Vav3 , VEPH1
Ver también
- Pleckstrin
- El dominio FYVE no relacionado se une al 3-fosfato de fosfatidilinositol y se ha encontrado en más de 60 proteínas.
- El dominio GRAM es un dominio proteico estructuralmente relacionado.
Referencias
enlaces externos
- Dominios de interacción de proteínas de Nash Lab - descripción del dominio PH
- UMich Orientación de proteínas en familias de membranas / superfamilia-51 - Orientaciones calculadas de dominios de PH en membranas
