Oxocarbono - Oxocarbon
Un oxocarbono u óxido de carbono es un compuesto químico que consta únicamente de carbono y oxígeno . Los oxocarbonos más simples y comunes son el monóxido de carbono (CO) y el dióxido de carbono (CO 2 ). Se conocen muchos otros óxidos de carbono estables (prácticamente si no termodinámicamente) o metaestables , pero rara vez se encuentran, como el subóxido de carbono (C 3 O 2 o O = C = C = C = O) y el anhídrido melítico (C 12 O 9 ).
|
|
|
|

|
||||
| CO de carbono monóxido |
CO 2 Dióxido de carbono |
Subóxido de
carbono C 3 O 2 |
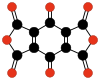
C 12 O 9 anhídrido
melítico |
Hoy en día se conocen muchos otros óxidos, la mayoría de ellos sintetizados desde la década de 1960. Algunos de estos nuevos óxidos son estables a temperatura ambiente. Algunos son metaestables o estables solo a temperaturas muy bajas, pero se descomponen en oxocarbonos más simples cuando se calientan. Muchos son inherentemente inestables y solo se pueden observar momentáneamente como intermedios en reacciones químicas o son tan reactivos que existen solo en fase gaseosa o solo se han detectado mediante aislamiento de matriz .
Existen óxido de grafeno y otros óxidos de carbono poliméricos estables con estructuras moleculares ilimitadas.
Visión general
El dióxido de carbono (CO 2 ) se encuentra ampliamente en la naturaleza y fue producido de manera incidental por los seres humanos desde tiempos prehistóricos, mediante la respiración, la combustión de sustancias que contienen carbono y la fermentación de alimentos como la cerveza y el pan . Fue reconocido gradualmente como una sustancia química, anteriormente llamada spiritus sylvestris ("espíritu del bosque") o "aire fijo", por varios químicos en los siglos XVII y XVIII.
El monóxido de carbono se puede producir en la combustión, también, y se utilizó (aunque no reconocido) desde la antigüedad para la fundición de hierro a partir de sus minerales . Al igual que el dióxido, fue descrito y estudiado en Occidente por varios alquimistas y químicos desde la Edad Media. Su verdadera composición fue descubierta por William Cruikshank en 1800.
El subóxido de carbono fue descubierto por Benjamin Brodie en 1873, pasando corriente eléctrica a través del dióxido de carbono.
El cuarto óxido "clásico", anhídrido melítico (C 12 O 9 ), aparentemente fue obtenido por Liebig y Wöhler en 1830 en su estudio de mellita ("piedra de miel") , pero fue caracterizado sólo en 1913 por Meyer y Steiner.
Brodie también descubrió en 1859 un quinto compuesto llamado óxido de grafito , que consta de carbono y oxígeno en proporciones que varían entre 2: 1 y 3: 1; pero la naturaleza y estructura molecular de esta sustancia permaneció desconocida hasta hace unos años, cuando pasó a llamarse óxido de grafeno y se convirtió en un tema de investigación en nanotecnología .
Ejemplos notables de óxidos inestables o metaestables que se detectaron solo en situaciones extremas son el radical monóxido de dicarbono (: C = C = O), trióxido de carbono (CO 3 ), tetróxido de carbono ( CO
4 ), pentóxido de carbono ( CO
5 ), hexóxido de carbono ( CO
6 ) y 1,2-dioxetanodiona (C 2 O 4 ). Algunos de estos óxidos de carbono reactivos se detectaron dentro de nubes moleculares en el medio interestelar mediante espectroscopía rotacional .
Se han estudiado muchos oxocarbonos hipotéticos mediante métodos teóricos, pero aún no se han detectado. Los ejemplos incluyen anhídrido oxálico (C 2 O 3 o O = (C 2 O) = O), etilendiona (C 2 O 2 o O = C = C = O) y otros polímeros lineales o cíclicos de monóxido de carbono (-CO- ) n ( policetonas ), y polímeros lineales o cíclicos de dióxido de carbono (-CO 2 -) n , tales como el dímero 1,3-dioxetanodiona (C 2 O 4 ).
|
|
|

|
|||
| C 2 O 3 anhídrido
oxálico |
C 2 O 2 Etileno diona |
C 2 O 4 1,3-Dioxetane- diona |
Estructura general
Normalmente, el carbono es tetravalente , mientras que el oxígeno es divalente , y en la mayoría de los oxocarbonos (como en la mayoría de los otros compuestos de carbono) cada átomo de carbono puede estar unido a otros cuatro átomos, mientras que el oxígeno puede estar unido como máximo a dos. Además, mientras que el carbono puede conectarse con otros carbonos para formar cadenas o redes arbitrariamente grandes, las cadenas de tres o más oxígenos rara vez se observan. Por tanto, los oxocarbonos eléctricamente neutros conocidos generalmente consisten en uno o más esqueletos de carbono (incluidas estructuras cíclicas y aromáticas ) conectados y terminados por grupos óxido (-O-, = O) o peróxido (-OO-).
Los átomos de carbono con enlaces insatisfechos se encuentran en algunos óxidos, como el dirradical C 2 O o: C = C = O; pero estos compuestos son generalmente demasiado reactivos para aislarse a granel. La pérdida o ganancia de electrones puede resultar en oxígeno negativo monovalente (- O -
), oxígeno trivalente positivo (≡ O +
), o carbono negativo trivalente (≡ C -
). Los dos últimos se encuentran en el monóxido de carbono, - C≡O + . El oxígeno negativo se encuentra en la mayoría de los aniones oxocarbonados .
Dióxidos de carbono lineales
Una familia de óxidos de carbono tiene la fórmula general C n O 2 , o O = (C =) n O, es decir, una cadena lineal de átomos de carbono, cubierta por átomos de oxígeno en ambos extremos. Los primeros miembros son
- CO 2 u O = C = O, el conocido dióxido de carbono .
- C 2 O 2 o O = C = C = O, la etilen diona extremadamente inestable .
- C 3 O 2 o O = C = C = C = O, el subóxido de carbono metaestable o dióxido de tricarbono.
- C 4 O 2 o O = C = C = C = C = O, dióxido de tetracarbono o 1,2,3-butatrieno-1,4-diona
- C 5 O 2 o O = C = C = C = C = C = O, dióxido de pentacarbono , estable en solución a temperatura ambiente. y puro hasta -90 ° C.
Algunos miembros superiores de esta familia se han detectado en trazas en experimentos de fase gaseosa a baja presión y / o matriz criogénica, específicamente para n = 7 yn = 17, 19 y 21.
Monóxidos de carbono lineales
Otra familia de oxocarbonos son los monóxidos de carbono lineales C n O. El primer miembro, el monóxido de carbono ordinario CO, parece ser el único que es prácticamente estable en estado puro a temperatura ambiente (aunque no es termodinámicamente estable a temperatura estándar y presión , ver reacción de Boudouard ). La fotólisis de los dióxidos de carbono lineales en una matriz criogénica conduce a la pérdida de CO, lo que da como resultado cantidades detectables de monóxidos pares, como C 2 O, C 4 O y C 6 O. Los miembros hasta n = 9 también se han obtenido por descarga eléctrica sobre C 3 O 2 gaseoso diluido en argón. Los primeros tres miembros se han detectado en el espacio interestelar.
Cuando n es par, se cree que las moléculas están en el estado triplete ( similar al cumuleno ), con los átomos conectados por dobles enlaces y un orbital vacío en el primer carbono, como en: C = C = O,: C = C = C = C = O, y, en general,: (C =) n = O. Cuando n es impar, se cree que la estructura del triplete resuena con un estado polar singlete ( tipo acetileno ) con una carga negativa en el extremo del carbono y una positiva en el extremo del oxígeno, como en - C≡C − C≡O + , - C≡C − C≡C − C≡O + y, en general, - (C≡C−) ( n −1) / 2 C≡O + . El propio monóxido de carbono sigue este patrón: se cree que su forma predominante es - C≡O + .
Policetonas cíclicas tipo radialeno
Otra familia de oxocarbonos que ha atraído especial atención son los oxocarbonos cíclicos de tipo radialeno C n O n o (CO) n . Ellos pueden ser considerados como polímeros cíclicos de monóxido de carbono, o n -fold cetonas de n -carbono cicloalcanos . El propio monóxido de carbono (CO) puede considerarse como el primer miembro. Los estudios teóricos indican que la etilen diona (C 2 O 2 o O = C = C = O) y la ciclopropanetriona C 3 O 3 no existen. Los siguientes tres miembros, C 4 O 4 , C 5 O 5 y C 6 O 6 , son teóricamente posibles, pero se espera que sean bastante inestables y, hasta ahora, solo se han sintetizado en pequeñas cantidades.
|
|

|

|

|

|
|||||
| (CO) 2 Etileno diona |
(CO) 3 Cyclopropane- triona |
(CO) 4 ciclobutano- tetrona |
(CO) 5 ciclopentano- pentona |
(CO) 6 ciclohexano- hexona |
Por otro lado, los aniones de estos oxocarbonos son bastante estables, y algunos de ellos se conocen desde el siglo XIX. Son
- C 2 O 2 2− , acetilendiolato (Weiss y Büchner, 1963),
- C 3 O 3 2− , deltate (Eggerding y West, 1976),
- C 4 O 4 2− , al cuadrado (Cohen y otros, 1959),
- C 5 O 5 2− , croconato (Gmelin, 1825) y
- C 6 O 6 2− , rodizonato (Heller, 1837).
El óxido cíclico C 6 O 6 también forma los aniones estables de tetrahidroxi-1,4-benzoquinona (C 6 O 6 4− ) y bencenohexol (C 6 O 6 6− ). La aromaticidad de estos aniones se ha estudiado utilizando métodos teóricos. .
Nuevos óxidos
Desde la década de 1960 se han sintetizado muchos óxidos estables o metaestables nuevos, como:
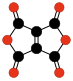
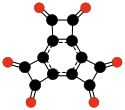
- C 10 O 8 , dianhídrido benzoquinonetetracarboxylic (Hammond, 1963).
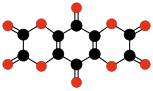
- C 6 O 6 , dianhídrido etilentetracarboxílico , un isómero estable de ciclohexanohexona (Sauer y otros, 1967).
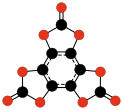
- C _ { 12} O _ { 12} o C _ { 6} (C _ { 2} O _ { 4} ) _ { 3} , trisoxalato de hexahidroxibenceno (Verter y Dominic, 1967); estable como solvato de tetrahidrofurano .
- C 10 O 10 o C 6 O 2 (C 2 O 4 ) 2 , bisoxalato de tetrahidroxi-1,4-benzoquinona (Verter y otros, 1968); estable como solvato de tetrahidrofurano.
- C 8 O 8 o C 6 O 2 (CO 3 ) 2 , tetrahidroxi-1,4-benzoquinona biscarbonato (Nallaiah, 1984); se descompone a aproximadamente 45–53 ° C.
- C 9 O 9 o C 6 (CO 3 ) 3 , triscarbonato de hexahidroxibenceno (Nallaiah, 1984); se descompone a aproximadamente 45–53 ° C.
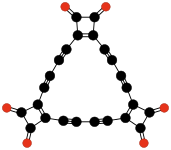
- C 24 O 6 , un trímero cíclico de la birradical 3,4-dialkynyl-3-cyclobutene1,2-diona -C = C- (C 4 O 2 ) -C = C- (Rubin y otros, 1990);
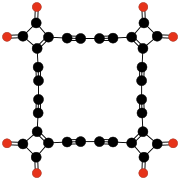
- C 32 O 8 , un tetrámero de 3,4-dialkynyl-3-cyclobutene1,2-diona (Rubin y otros, 1990);
- C 4 O 6 , dioxano tetracetona o anhídrido oxálico dimérico (Strazzolini y otros, 1998); estable en Et 2 O a -30 ° C, se descompone a 0 ° C.
- C 12 O 6 , hexaoxotriciclobutabenceno
Se han investigado teóricamente muchos parientes de estos óxidos y se espera que algunos sean estables, como otros ésteres de carbonato y oxalato de tetrahidroxi-1,2-benzoquinona y de los ácidos rodizónico, crocónico, escuárico y deltico.
Óxidos de carbono poliméricos
El subóxido de carbono se polimeriza espontáneamente a temperatura ambiente en un polímero de carbono-oxígeno , con una relación atómica carbono: oxígeno de 3: 2. Se cree que el polímero es una cadena lineal de anillos de lactona de seis miembros fusionados , con una cadena principal de carbono continua de enlaces simples y dobles alternos. Las mediciones físicas indican que el número medio de unidades por molécula es de aproximadamente 5-6, dependiendo de la temperatura de formación.

|
|
|

|
||||||
| Unidades terminales y repetidas de C 3 O 2 polimérico . | |||||||||

|

|
|

|
||||||
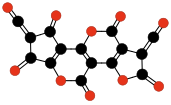
| Oligómeros de C 3 O 2 con 3 a 6 unidades. | |||||||||
El monóxido de carbono comprimido a 5 GPa en una celda de yunque de diamante produce un polímero rojizo algo similar con un contenido de oxígeno ligeramente mayor, que es metaestable en condiciones ambientales. Se cree que el CO se desproporciona en la celda a una mezcla de CO 2 y C 3 O 2 ; este último forma un polímero similar al descrito anteriormente (pero con una estructura más irregular), que atrapa parte del CO 2 en su matriz.
Otro polímero de carbono-oxígeno, con una relación C: O de 5: 1 o superior, es el óxido de grafito clásico y su versión de una sola hoja, el óxido de grafeno .
Ozónidos y óxidos de fullereno
Se conocen más de 20 óxidos y ozónidos de fullereno :
- C 60 O (2 isómeros)
- C 60 O 2 (6 isómeros)
- C 60 O 3 (3 isómeros)
- C 120 O
- C 120 O 4 (4 isómeros)
- C 70 O
- C 140 O
y otros.