Hexametilfosforamida - Hexamethylphosphoramide
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
Triamida hexametilfosfórica |
|
| Otros nombres
Hexametilfosforamida
Hexametapol HMPA Tris (dimetilamida) fosfórico (no recomendado) HMPT |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.010.595 |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 6 H 18 N 3 O P | |
| Masa molar | 179,20 g / mol |
| Apariencia | líquido transparente e incoloro |
| Olor | aromático, suave, amínico |
| Densidad | 1,03 g / cm 3 |
| Punto de fusion | 7,20 ° C (44,96 ° F; 280,35 K) |
| Punto de ebullición | 232,5 ° C (450,5 ° F; 505,6 K) CRC |
| miscible | |
| Presión de vapor | 0,03 mmHg (4,0 Pa) a 20 ° C |
| Peligros | |
| Principales peligros | Sospecha de carcinógeno |
| Ficha de datos de seguridad | MSDS de Oxford |
| punto de inflamabilidad | 104,4 ° C (219,9 ° F; 377,5 K) |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
|
PEL (permitido)
|
ninguno |
|
REL (recomendado)
|
California |
|
IDLH (peligro inmediato)
|
Ca [ND] |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
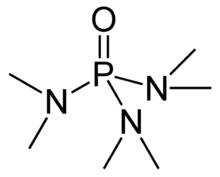
La hexametilfosforamida , a menudo abreviada como HMPA , es una fosforamida (una amida de ácido fosfórico ) con la fórmula [(CH 3 ) 2 N] 3 PO. Este líquido incoloro es un reactivo útil en síntesis orgánica .
Estructura y reactividad
HMPA es el óxido de la fosfina terciaria hexametilfosforosa triamida altamente básica (HMPT), P (NMe 2 ) 3 . Al igual que otros óxidos de fosfina (como el óxido de trifenilfosfina ), la molécula tiene un núcleo tetraédrico y un enlace P = O que está altamente polarizado, con una carga negativa significativa que reside en el átomo de oxígeno.
Los compuestos que contienen un enlace nitrógeno- fósforo típicamente son degradados por el ácido clorhídrico para formar una amina protonada y un fosfato.
Disuelve los metales alcalinos formando soluciones azules que son estables durante algunas horas. Los electrones solvatados están presentes en estas soluciones azules.
Aplicaciones
HMPA es un solvente especializado para polímeros , gases y compuestos organometálicos . Mejora la selectividad de las reacciones de litiación al romper los oligómeros de las bases de litio como el butillitio . Debido a que el HMPA solvata selectivamente los cationes, acelera las reacciones S N 2 que de otro modo serían más lentas al generar más aniones desnudos. Los centros básicos de nitrógeno en HMPA se coordinan fuertemente con Li + .
HMPA es un ligando en los reactivos útiles basados en complejos de peróxido de molibdeno , por ejemplo, MoO (O 2 ) 2 (HMPA) (H 2 O) se usa como oxidante en síntesis orgánica.
Reactivos alternativos
A menudo se puede utilizar dimetilsulfóxido en lugar de HMPA como codisolvente. Ambos son fuertes aceptores de enlaces de hidrógeno y sus átomos de oxígeno se unen a cationes metálicos . Otras alternativas al HMPA incluyen las N , N '-tetraalquilureas DMPU (dimetilpropilenurea) o DMI (1,3-dimetil-2-imidazolidinona). Se ha informado que la triamida del ácido tripirrolidinofosfórico (TPPA) es un buen reactivo sustituto del HMPA en reducciones con diyoduro de samario y como un aditivo de base de Lewis para muchas reacciones que involucran cetilos de samario .
Toxicidad
El HMPA es solo levemente tóxico, pero se ha demostrado que causa cáncer en ratas. El HMPA puede degradarse por la acción del ácido clorhídrico .
Referencias
enlaces externos
- "Hexametilfosforamida CAS No. 680-31-9" (PDF) . Informe sobre carcinógenos (12ª ed.). Programa Nacional de Toxicología, Departamento de Salud y Servicios Humanos. 2011.
- "Hexametilfosforamida" . Guía de bolsillo de NIOSH sobre peligros químicos . Centros para el Control y la Prevención de Enfermedades, Departamento de Salud y Servicios Humanos. 2011.
- Merck Index . 4761 (12ª ed.).
