Tricloruro de galio - Gallium trichloride
|
|

|
|
| Nombres | |
|---|---|
| Otros nombres
Cloruro de galio (III), triclorogalio, triclorogallano
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| Tarjeta de información ECHA |
100.033.268 |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
| Propiedades | |
|
GaCl 3 |
|
| Masa molar | 176.073 g / mol |
| Apariencia | cristales incoloros delicuescentes |
| Densidad | 2,47 g / cm 3 2,053 g / cm 3 en el punto de fusión |
| Punto de fusion | 77,9 ° C (172,2 ° F; 351,0 K) (anhidro) 44,4 ° C (hidratado) |
| Punto de ebullición | 201 ° C (394 ° F; 474 K) |
| muy soluble | |
| Solubilidad | soluble en benceno , CCl 4 , CS 2 |
| −63,0 · 10 −6 cm 3 / mol | |
| Peligros | |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | No es inflamable |
| Dosis o concentración letal (LD, LC): | |
|
LD 50 ( dosis media )
|
4700 mg / kg (rata, oral) |
| Compuestos relacionados | |
|
Otros aniones
|
Fluoruro de galio (III) Bromuro de galio (III) Yoduro de galio (III) |
|
Otros cationes
|
Cloruro de aluminio Cloruro de indio (III) Cloruro de talio (III) |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
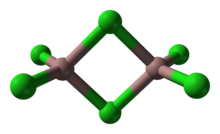
El tricloruro de galio es el compuesto químico con la fórmula GaCl 3 . El tricloruro de galio sólido existe como un dímero con la fórmula Ga 2 Cl 6 . Es incoloro y soluble en prácticamente todos los disolventes, incluso alcanos, lo que es realmente inusual para un haluro metálico. Es el principal precursor de la mayoría de los derivados del galio y un reactivo en síntesis orgánica .
Como ácido de Lewis , GaCl 3 es más suave que el tricloruro de aluminio . El galio (III) es más fácil de reducir que el Al (III), por lo que la química de los compuestos de galio reducido es más extensa que la del aluminio. Se conoce Ga 2 Cl 4 mientras que el Al 2 Cl 4 correspondiente no lo es. La química de coordinación de Ga (III) y Fe (III) es similar, y se han utilizado compuestos de galio (III) como análogos diamagnéticos de compuestos férricos.
Preparación
El tricloruro de galio se puede preparar a partir de los elementos, calentando el metal galio en una corriente de cloro y purificando el producto por sublimación al vacío.
- 2 Ga + 3 Cl 2 → 2 GaCl 3
También se puede preparar calentando óxido de galio con cloruro de tionilo :
- Ga 2 O 3 + 3 SOCl 2 → 2 GaCl 3 + 3 SO 2
El galio metálico reacciona lentamente con el ácido clorhídrico. Esta reacción produce gas hidrógeno lentamente.
Estructura
Como sólido, adopta una estructura bitetraédrica con dos cloruros puente. Su estructura se asemeja a la del tribromuro de aluminio . Por el contrario, las características de AlCl 3 e InCl 3 contienen 6 centros de metal coordinados. Como consecuencia de su naturaleza molecular y la baja energía reticular asociada , el tricloruro de galio tiene un punto de fusión más bajo que los trihaluros de aluminio e indio. La fórmula de Ga 2 Cl 6 a menudo se escribe como Ga 2 (μ-Cl) 2 Cl 4 . En la fase gaseosa, los dímeros se disocian en monómeros planos trigonales .
Complejos
El galio es el miembro más ligero del Grupo 13 que tiene una capa d completa (el galio tiene la configuración electrónica [ Ar ] 3 d 10 4 s 2 4 p 1 ) por debajo de los electrones de valencia que podrían participar en la unión d -π con ligandos. El bajo estado de oxidación de Ga en Ga (III) Cl 3 , junto con la baja electronegatividad y la alta polarización , permiten que GaCl 3 se comporte como un "ácido blando" en términos de la teoría HSAB . La fuerza de los enlaces entre los haluros de galio y los ligandos se ha estudiado extensamente. Lo que emerge es:
- GaCl 3 es un ácido de Lewis más débil que el AlCl 3 hacia los donantes de N y O, por ejemplo, piridina.
- GaCl 3 es un ácido de Lewis más fuerte que el AlCl 3 hacia los tioéteres, por ejemplo , sulfuro de dimetilo , Me 2 S
Con un ion cloruro como ligando , se produce el ion tetraédrico GaCl 4 - , no se puede formar la coordenada 6 GaCl 6 3− . Se conocen compuestos como KGa 2 Cl 7 que tienen un anión con puente de cloruro . En una mezcla fundida de KCl y GaCl 3 , existe el siguiente equilibrio:
- 2 GaCl 4 - ⇌ Ga 2 Cl 7 - + Cl -
Usos
Síntesis orgánica
El tricloruro de galio es un catalizador ácido de Lewis , como en la reacción de Friedel-Crafts , y también se usa en reacciones de carbogallación de compuestos con un triple enlace carbono-carbono. Es un precursor de los reactivos organogallium . También se utiliza como catalizador en muchas reacciones orgánicas.
Detección de neutrinos solares
Se utilizaron 110 toneladas de solución acuosa de tricloruro de galio en los experimentos GALLEX y GNO realizados en el Laboratori Nazionali del Gran Sasso en Italia para detectar neutrinos solares . En estos experimentos, el germanio -71 fue producido por interacciones de neutrinos con el isótopo galio-71 (que tiene una abundancia natural del 40%), y se midieron las subsecuentes desintegraciones beta del germanio-71.
Ver también
Referencias
- Greenwood, Norman N .; Earnshaw, Alan (1997). Química de los Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8 .
- "Galio" . Tabla periódica de WebElements .
- ^ Wells, AF (1984) Química inorgánica estructural, Oxford: Clarendon Press. ISBN 0-19-855370-6 .
- ^ a b Yamaguchi, Masahiko; Matsunaga, Shigeki; Shibasaki, Masakatsu; Michelet, Bastien; Bour, Christophe; Gandon, Vincent (2014), "Tricloruro de galio", Encyclopedia of Reagents for Organic Synthesis , John Wiley & Sons, Ltd, págs. 1–8, doi : 10.1002 / 047084289x.rn00118u.pub3 , ISBN 9780470842898
- ^ SC Wallwork IJWorral J.Chem. Soc 1965,1816
- ^ Kovar, RA "Tricloruro de galio" Síntesis inorgánica, 1977, volumen XVII, págs. 167-172. ISBN 0-07-044327-0
- ^ H.Hecht, G.Jander, H. Schlapmann Z. Anorg. Allgem. Chem. Vol.254, p.255 (1947)
- ^ JH von Barner Inorg Chem 1985 24 1686
- ^ David R. Lide, ed. Manual de Química y Física, 85ª edición , versión de Internet 2005. CRC Press, 2005.
enlaces externos
- "Guía de tratamiento de primeros auxilios de emergencia - tricloruro de galio" . Agencia de Protección Ambiental de Estados Unidos . Archivado desde el original el 12 de noviembre de 2004.

