Cianuro de zinc - Zinc cyanide
|
|
| Identificadores | |
|---|---|
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| Tarjeta de información ECHA |
100.008.331 |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| Zn (CN) 2 | |
| Masa molar | 117,444 g / mol |
| Apariencia | Blanco sólido |
| Densidad | 1.852 g / cm 3 , sólido |
| Punto de fusion | 800 ° C (1,470 ° F; 1,070 K) (se descompone) |
| 0,00005 g / 100 ml (20 ° C) | |
| Solubilidad | atacado por álcalis , KCN , amoniaco |
| −46,0 · 10 −6 cm 3 / mol | |
| Peligros | |
| no enlistado | |
| NFPA 704 (diamante de fuego) | |
| Dosis o concentración letal (LD, LC): | |
|
LD 50 ( dosis mediana )
|
100 mg / kg, rata (intraperitoneal) |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El cianuro de zinc es el compuesto inorgánico de fórmula Zn ( CN ) 2 . Es un sólido blanco que se utiliza principalmente para galvanoplastia de zinc pero también tiene aplicaciones más especializadas para la síntesis de compuestos orgánicos .
Estructura
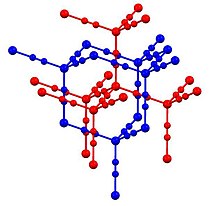
En Zn (CN) 2 , el zinc adopta el entorno de coordinación tetraédrico, todos unidos por ligandos de cianuro puente . La estructura consta de dos estructuras "interpenetradas" (azul y rojo en la imagen de arriba). Estos motivos a veces se denominan estructuras " diamondoides expandidas ". Algunas formas de SiO 2 adoptan una estructura similar, en la que los centros tetraédricos de Si están unidos por óxidos. El grupo cianuro muestra un desorden de cabeza a cola con cualquier átomo de zinc que tiene entre uno y cuatro vecinos de carbono, y el resto son átomos de nitrógeno. Muestra uno de los mayores coeficientes negativos de expansión térmica (superando al anterior poseedor del récord, tungstato de circonio ).
Propiedades químicas
Típico de un polímero inorgánico, el Zn (CN) 2 es insoluble en la mayoría de los disolventes. El sólido se disuelve, o más precisamente, se degrada mediante soluciones acuosas de ligandos básicos tales como hidróxido , amoníaco y cianuro adicional para dar complejos aniónicos.
Síntesis
El Zn (CN) 2 es fácil de preparar mediante la combinación de soluciones acuosas de iones de zinc y cianuro, por ejemplo, mediante la reacción de doble sustitución entre KCN y ZnSO 4 :
- ZnSO 4 + 2 KCN → Zn (CN) 2 + K 2 SO 4
Para aplicaciones comerciales, se hacen algunos esfuerzos para evitar las impurezas de haluros mediante el uso de sales de acetato de zinc:
- Zn (CH 3 COO) 2 + HCN → Zn (CN) 2 + 2 CH 3 COOH
El cianuro de zinc también se produce como subproducto de ciertos métodos de extracción de oro . Los procedimientos para aislar el oro del cianuro de oro acuoso a veces requieren la adición de zinc:
- 2 [Au (CN) 2 ] - + Zn → 2 Au + Zn (CN) 2 + 2 CN -
Aplicaciones
Galvanoplastia
La principal aplicación de Zn (CN) 2 es la galvanoplastia de zinc a partir de soluciones acuosas que contienen cianuro adicional.
Síntesis orgánica
El Zn (CN) 2 se usa para introducir el grupo formilo en compuestos aromáticos en la reacción de Gatterman, donde sirve como una alternativa conveniente, más segura y no gaseosa al HCN . Debido a que la reacción utiliza HCl , Zn (CN) 2 también suministra la reacción in situ con ZnCl 2 , un catalizador ácido de Lewis . Los ejemplos de Zn (CN) 2 que se utilizan de esta manera incluyen la síntesis de 2-hidroxi-1-naftaldehído y mesitaldehído.
El Zn (CN) 2 también se emplea como catalizador para la cianosililación de aldehídos y cetonas.
Referencias

