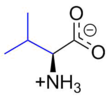
Valina - Valine
|
|||
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC
Valina
|
|||
| Otros nombres
Ácido 2-amino-3-metilbutanoico
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Tarjeta de información ECHA |
100.000.703 |
||
| Número CE | |||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
|
Tablero CompTox ( EPA )
|
|||
|
|||
| Propiedades | |||
| C 5 H 11 N O 2 | |||
| Masa molar | 117,148 g · mol −1 | ||
| Densidad | 1.316 g / cm 3 | ||
| Punto de fusion | 298 ° C (568 ° F; 571 K) (descomposición) | ||
| soluble | |||
| Acidez (p K a ) | 2,32 (carboxilo), 9,62 (amino) | ||
| -74,3 · 10 −6 cm 3 / mol | |||
| Página de datos complementarios | |||
|
Índice de refracción ( n ), constante dieléctrica (ε r ), etc. |
|||
|
Datos termodinámicos |
Comportamiento de fase sólido-líquido-gas |
||
| UV , IR , RMN , MS | |||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
La valina (símbolo Val o V ) es un α- aminoácido que se utiliza en la biosíntesis de proteínas. Contiene un α- grupo amino (que está en la protonado -NH 3 + forma en condiciones biológicas), un α- grupo de ácido carboxílico (que está en la -COO desprotonada - forma en condiciones biológicas), y una cadena lateral grupo isopropilo , lo que lo convierte en un aminoácido alifático no polar . Es esencial en el ser humano, lo que significa que el cuerpo no puede sintetizarlo: debe obtenerse de la dieta. Las fuentes dietéticas humanas son alimentos que contienen proteínas, como carnes, productos lácteos, productos de soya, frijoles y legumbres. Está codificado por todos los codones que comienzan con GU (GUU, GUC, GUA y GUG).
Historia y etimología
La valina fue aislada por primera vez de la caseína en 1901 por Hermann Emil Fischer . El nombre valina proviene del ácido valérico , que a su vez lleva el nombre de la planta valeriana debido a la presencia del ácido en las raíces de la planta.
Nomenclatura
Según la IUPAC , los átomos de carbono que forman valina se numeran secuencialmente comenzando desde 1 que denota el carbono carboxilo , mientras que 4 y 4 'denotan los dos metilcarbonos terminales .
Metabolismo
Fuente y biosíntesis
La valina, como otros aminoácidos de cadena ramificada, es sintetizada por plantas, pero no por animales. Por tanto, es un aminoácido esencial en los animales y debe estar presente en la dieta. Los seres humanos adultos necesitan alrededor de 4 mg / kg de peso corporal al día. Se sintetiza en plantas y bacterias a través de varios pasos a partir del ácido pirúvico . La parte inicial de la vía también conduce a la leucina . El α-cetoisovalerato intermedio sufre una aminación reductora con glutamato . Las enzimas involucradas en esta biosíntesis incluyen:
- Acetolactato sintasa (también conocida como acetohidroxiácido sintasa)
- Isomerorreductasa de acetohidroxiácido
- Dihidroxiácido deshidratasa
- Valina aminotransferasa
Degradación
Al igual que otros aminoácidos de cadena ramificada, el catabolismo de la valina comienza con la eliminación del grupo amino por transaminación , dando alfa-cetoisovalerato , un alfa- cetoácido , que se convierte en isobutiril-CoA mediante descarboxilación oxidativa por la cadena ramificada α -complejo cetoácido deshidrogenasa . Esto se oxida y se reordena aún más en succinil-CoA , que puede entrar en el ciclo del ácido cítrico .
Síntesis
La valina racémica se puede sintetizar mediante bromación de ácido isovalérico seguida de aminación del derivado α-bromo
- HO 2 CCH 2 CH (CH 3 ) 2 + Br 2 → HO 2 CCHBrCH (CH 3 ) 2 + HBr
- HO 2 CCHBrCH (CH 3 ) 2 + 2 NH 3 → HO 2 CCH (NH 2 ) CH (CH 3 ) 2 + NH 4 Br
Importancia médica
Resistencia a la insulina
La valina, al igual que otros aminoácidos de cadena ramificada, está asociada con la resistencia a la insulina: se observan niveles más altos de valina en la sangre de ratones, ratas y humanos diabéticos. Los ratones alimentados con una dieta de privación de valina durante un día han mejorado la sensibilidad a la insulina, y la alimentación con una dieta de privación de valina durante una semana reduce significativamente los niveles de glucosa en sangre. En ratones obesos y resistentes a la insulina inducidos por la dieta, una dieta con niveles reducidos de valina y otros aminoácidos de cadena ramificada da como resultado una adiposidad reducida y una sensibilidad a la insulina mejorada. El catabolito de valina 3-hidroxiisobutirato promueve la resistencia a la insulina del músculo esquelético en ratones al estimular la captación de ácidos grasos en el músculo y la acumulación de lípidos. En los seres humanos, una dieta restringida en proteínas reduce los niveles sanguíneos de valina y disminuye los niveles de glucosa en sangre en ayunas.
Células madre hematopoyéticas
La valina dietética es esencial para la autorrenovación de las células madre hematopoyéticas (HSC), como lo demuestran los experimentos en ratones. La restricción dietética de valina agota selectivamente las HSC repobladas a largo plazo en la médula ósea del ratón. Se logró un trasplante exitoso de células madre en ratones sin irradiación después de 3 semanas con una dieta restringida en valina. La supervivencia a largo plazo de los ratones trasplantados se logró cuando la valina se devolvió a la dieta gradualmente durante un período de 2 semanas para evitar el síndrome de realimentación .
Ver también
Referencias
enlaces externos