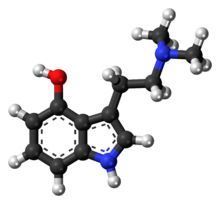
Psilocina - Psilocin
 | |
 | |
| Datos clinicos | |
|---|---|
| Otros nombres | 4-hidroxi- N , N -dimetiltriptamina |
| Vías de administración |
Oral, IV |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Metabolismo | Hepático |
| Vida media de eliminación | 1-3 horas |
| Excreción | Orina |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA |
100.007.543 |
| Datos químicos y físicos | |
| Fórmula | C 12 H 16 N 2 O |
| Masa molar | 204,273 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| Punto de fusion | 173 a 176 ° C (343 a 349 ° F) |
| |
| |
|
| |
Psilocina (también conocido como 4-HO-DMT , DMT 4-hidroxi , psilocina , psilocina , o psilotsin ) es un Sustituido triptamina alcaloide y una sustancia psicodélica serotoninérgica . Está presente en la mayoría de los hongos psicodélicos junto con su contraparte fosforilada , la psilocibina . La psilocina es una droga de la Lista I según la Convención sobre Sustancias Psicotrópicas . Los efectos de la psilocina que alteran la mente son muy variables, subjetivos y se asemejan a los del LSD y el DMT .
Química
La psilocina y su prima fosforilada, la psilocibina , fueron aisladas y nombradas por primera vez en 1958 por el químico suizo Albert Hofmann . Hofmann obtuvo los productos químicos de muestras cultivadas en laboratorio del hongo enteogénico Psilocybe mexicana . Hofmann también logró encontrar rutas sintéticas para estos productos químicos.
La psilocina se puede obtener por desfosforilación de la psilocibina natural en condiciones fuertemente ácidas o alcalinas ( hidrólisis ). Otra ruta sintética utiliza la síntesis de triptamina de Speeter-Anthony a partir de 4-hidroxiindol.
La psilocina es relativamente inestable en solución debido a su grupo fenólico hidroxi (-OH). En presencia de oxígeno , forma fácilmente productos de degradación de color negro azulado y oscuro. También se forman productos similares en condiciones ácidas en presencia de oxígeno e iones Fe 3+ ( reactivo de Keller ).
Análogos estructurales
Se conocen análogos de azufre con un reemplazo de benzotienilo así como con 4- SH -DMT. La 1-metilpsilocina es un agonista que prefiere el receptor 5-HT 2C funcionalmente . Se conoce la 4-fluoro- N , N -dimetiltriptamina . O- acetilpsilocina (4-AcO-DMT) es un análogo acetilado de psilocina. Además, el reemplazo de un grupo metilo en el nitrógeno dimetilado con un grupo isopropilo o etilo produce 4-HO-MIPT (4-hidroxi- N- metil- N -isopropiltriptamina) y 4-HO-MET (4-hidroxi- N -metilo - N -etiltriptamina), respectivamente.
Farmacología
La psilocina es el agente farmacológicamente activo en el cuerpo después de la ingestión de psilocibina o algunas especies de hongos psicodélicos.
La psilocibina se desfosforila rápidamente en el cuerpo a psilocina, que actúa como agonista o agonista parcial de 5-HT 2A , 5-HT 2C y 5-HT 1A . La psilocina exhibe selectividad funcional porque activa la fosfolipasa A2 en lugar de activar la fosfolipasa C como lo hace el ligando endógeno serotonina. La psilocina es estructuralmente similar a la serotonina (5-HT), y se diferencia solo por que el grupo hidroxilo está en la posición 4 en lugar de la 5 y los grupos dimetilo en el nitrógeno . Se cree que sus efectos provienen de su actividad agonista en los receptores de serotonina 5-HT 2A en la corteza prefrontal .
La psilocina no tiene un efecto significativo sobre los receptores de dopamina (a diferencia del LSD ) y solo afecta el sistema noradrenérgico en dosis muy altas.
La vida media de la psilocina varía de 1 a 3 horas.
Efectos conductuales y no conductuales

Sus efectos fisiológicos son similares a un estado de excitación simpática . Los efectos específicos observados después de la ingestión pueden incluir , entre otros, taquicardia , pupilas dilatadas , inquietud o excitación, euforia, ojos abiertos y cerrados (comunes en dosis medias a altas), sinestesia (por ejemplo, oír colores y ver sonidos), aumento de la temperatura corporal. , dolor de cabeza , sudoración y escalofríos y náuseas . La psilocina actúa como agonista o agonista parcial de 5-HT2A, 5-HT2C y 5-HT1A. Se afirma que los receptores regulan significativamente las imágenes, la toma de decisiones, el estado de ánimo, la disminución de la presión arterial y la frecuencia cardíaca.
Prácticamente no existe letalidad directa asociada con la psilocina. Prácticamente no hay síndrome de abstinencia cuando se suspende el uso crónico de este fármaco . Existe tolerancia cruzada entre psilocina, mescalina , LSD y otros agonistas de 5-HT 2A , 5-HT 2C y 5-HT 1A debido a la regulación a la baja de estos receptores.
Estatus legal
La Convención de las Naciones Unidas sobre Sustancias Sicotrópicas (adoptada en 1971) requiere que sus miembros prohíban la psilocibina, y las partes del tratado deben restringir el uso de la droga a la investigación médica y científica bajo condiciones estrictamente controladas.
Australia
La psilocina se considera una sustancia prohibida de la Lista 9 en Australia según el Estándar de Venenos (octubre de 2015). Una sustancia de la Lista 9 es una sustancia que puede ser objeto de abuso o mal uso, cuya fabricación, posesión, venta o uso debería estar prohibida por la ley, excepto cuando sea necesario para la investigación médica o científica, o con fines analíticos, de enseñanza o de formación con la aprobación del Commonwealth. y / o autoridades sanitarias estatales o territoriales.
Rusia
La psilocina y la psilocibina están prohibidas en Rusia como estupefacientes con una sanción penal por posesión de al menos 50 mg.
