Nanophyetus -Nanophyetus
| Nanophyetus | |
|---|---|
|
clasificación cientifica |
|
| Reino: | Animalia |
| Filo: | Platelmintos |
| Clase: | Rhabditophora |
| Pedido: | Plagiorchiida |
| Familia: | Troglotrematidae |
| Género: |
Nanophyetus Chapin, 1927 |
| Especies: |
N. salmincola
|
| Nombre binomial | |
|
Nanophyetus salmincola ( Chapin , 1926) Chapin, 1927
|
|
| Sinónimos | |
|
|
Nanophyetus salmincola es un parásito trematodo intestinal transmitido por los alimentos queprevalece en lacosta noroeste del Pacífico . La especie puede ser el trematodo endémico más común de los Estados Unidos.
El ciclo de vida de N. salmincola requiere tres huéspedes . El primer huésped intermedio es un caracol de arroyo Juga plicifera . El segundo huésped intermedio es un pez salmónido , aunque algunos peces no salmónidos también juegan un papel. Por último, el huésped definitivo suele ser un cánido, aunque muchos otros mamíferos también son huéspedes definitivos, incluidos los humanos. La transmisión de N. salmincola al huésped definitivo se produce tras la ingestión de peces infectados por el parásito.
El parásito es más conocido por su asociación con la " enfermedad de envenenamiento del salmón " que, si no se trata, es fatal para los perros y otros cánidos. Sin embargo, los cánidos se ven afectados por la bacteria Neorickettsia helminthoeca , para la cual N. salmincola actúa como vector y no por el parásito en sí.
En la literatura se encuentran muy pocos casos conocidos de infección humana adquirida naturalmente con N. salmincola , aunque es probable que muchos casos no se notifiquen, ya que la mayoría de las personas son asintomáticas o sintomáticas con síntomas inespecíficos como malestar gastrointestinal. La enfermedad causada por N. salmincola , o nanofetiasis , se puede prevenir fácilmente cocinando bien el pescado antes de consumirlo. No se conocen casos de infección humana por la bacteria Rickettsia transportada por N. salmincola .
Un parásito subespecífico, Nanophyetus schikhobalowi , es endémico de Siberia , donde se han informado casos humanos de nanofetiasis en la literatura científica desde 1931.
Descubrimiento
El primer registro de intoxicación por salmón (SPD) se informó en el noroeste de Oregon en 1814 cuando un escritor del Henry's Astoria Journal notó la muerte de perros después del consumo de salmón crudo . Al principio, los investigadores creían que el SPD era causado por sangre venenosa en el pescado ingerido. En 1911, se observaron pequeños quistes blancos en los riñones de salmones y truchas causantes de enfermedades, pero los quistes se identificaron erróneamente como amebas. En 1925 se encontraron finalmente pequeños trematodos en los intestinos de perros que murieron después de comer salmón infectado y los quistes presentes en el salmón se identificaron correctamente como etapas intermedias del trematodo. En un estudio de seguimiento experimental, los investigadores demostraron que el parásito del intestino delgado de hecho causó SPD en perros y que los quistes se convirtieron en el gusano adulto que se encuentra en el intestino.
El trematodo fue nombrado por primera vez por Chapin como Nanophyes salmincola en 1926, como miembro de la familia Heterophyidae. Tras un examen más detenido de la morfología, Chapin reasignó el trematodo a la familia Troglotrematidae y renombró el parásito Nanophyetus salmincola , ya que Nanophyes ya se había tomado. Continuaron las discusiones sobre la exactitud de la clasificación del parásito a medida que el trematodo recibió mayor atención científica y se examinó más a fondo su morfología y comportamiento. Finalmente, se acordó Nanophyetus salmincola , aunque Troglotrema salmincola sigue siendo un sinónimo.
En 1931, Skrjabin y Podjapolskaja describen un parásito similar, Nanophyetus schikhobalowi , que era endémico de Siberia Oriental. El argumento sobre si N. schikhobalowi y N. salmincola eran la misma especie o especies diferentes se repitió hasta 1966, cuando a las dos se les otorgó un estatus subespecífico para reflejar sus diferencias biológicas y geográficas, pero pocas diferencias morfológicas significativas. Desde su descubrimiento, se sabe que N. schikhobalowi infecta naturalmente a los seres humanos y las investigaciones revelan encuestas que indican tasas de infección en las aldeas siberianas endémicas de hasta el 98%.
Por el contrario, no se reconoció que N. salmincola fuera una fuente de infección hasta que un investigador se infectó deliberadamente a sí mismo en un experimento científico en 1958. Además de que Philip se infectó experimentalmente con N. salmincola norteamericana , los primeros casos de infección intestinal humana adquiridos de forma natural se observaron entre septiembre de 1974 y octubre de 1985. El estudio reveló 10 pacientes que presentaban muestras de heces positivas a N. salmincola y molestias gastrointestinales o eosinofilia en sangre periférica inexplicable. 7 pacientes recordaron la ingestión de pescado crudo o poco cocido. De los que no recibieron un tratamiento eficaz, los síntomas y / o los huevos en las heces persistieron durante 2 o más meses antes de resolverse espontáneamente. Se planteó la hipótesis de que el movimiento, la unión y la irritación de los gusanos adultos en la mucosa del intestino delgado era la causa probable de los síntomas gastrointestinales y la eosinofilia periférica.
Dos años después de que se notificaran los primeros 10 casos de infección humana por N. salmincola en 1987, Fritsche et al. informó diez casos adicionales de nanofetiasis humana. Cinco presentaban molestias gastrointestinales y los otros cinco presentaban eosinofilia periférica inexplicable. Nueve de cada diez recordaron haber comido pescado mal cocido. Esta vez, el prazicuantel fue el tratamiento eficaz de elección.
En 1990, se notificó el primer caso de infección humana por N. salmincola sin ingestión de pescado contaminado crudo o poco cocido. Un hombre se infectó a través de la contaminación de las manos mientras manipulaba salmón coho recién sacrificado y altamente infectado. El diagnóstico de nanofetiasis se realizó con base en malestar gastrointestinal, esinofilia en sangre periférica y muestra de heces positiva. El tratamiento con praziquantel fue eficaz.
Ninguno de los casos humanos de infección por la subespecie norteamericana o siberiana revela infección por Neorickettsia helminthoeca transportada dentro del trematodo, que fue descubierto en 1950. La infección por rickettsia ayuda a explicar el desenlace más fatal que aflige a los cánidos.
Presentación clínica en humanos
Tras la infección por N. salmincola , los seres humanos normalmente son asintomáticos. Si los síntomas están presentes, generalmente son inespecíficos y se confunden con una indicación de otros problemas gastrointestinales. Los síntomas incluyen "diarrea, eosinofilia en sangre periférica inexplicable, malestar abdominal, náuseas y vómitos, pérdida de peso y fatiga". Los huevos de N. salmincola aparecen en las heces aproximadamente una semana después de la ingestión de pescado infectado.
Patología en perros
La nanofisiasis en perros es mucho más grave que en humanos. Los científicos notaron hace casi 200 años que los perros que consumían pescado crudo a veces morían con bastante rapidez. Esta "intoxicación por salmón", aunque está asociada con el trematodo Nanophyetus salmincola, no es causada por el gusano. La enfermedad es causada por Neorickettsia helminthoeca , una bacteria rickettsial que usa N. salmincola como hospedante. Aunque solo los caninos son susceptibles a la enfermedad, los mapaches muestran una temperatura elevada e infección linfática después de ser infectados por la rickettsia, pero ambos desaparecen pronto. El período de incubación en los perros es de 5 a 7 días, aunque puede tardar hasta 33 días. Después del inicio, hay una fiebre aguda junto con anorexia, vómitos y disentería. La rickettsia ataca el sistema linfático del canino provocando agrandamiento y eventualmente hemorragia de muchos de los ganglios linfáticos. La enfermedad puede extenderse a otros tejidos como los leucocitos. La muerte ocurre de 10 a 14 días después de que aparecen los primeros signos.
Transmisión
Nanophyetus salmincola se transmite más comúnmente por la ingestión de salmón o trucha trucha arco iris crudos, poco cocidos o ahumados. Por lo general, se trata de la ingestión del músculo del pez, pero se han notificado casos en los que el agente sospechoso de transmisión fue la hueva de Steelhead. Los investigadores plantean la hipótesis, en peces con una carga de gusanos especialmente alta, que N. salmincola puede migrar a muchos de los tejidos de los peces, no solo al tejido muscular. En un caso de 1990, se diagnosticó nanofetiasis en un individuo que se cree que adquirió la enfermedad por simple manipulación de salmón recién sacrificado. Irónicamente, el individuo infectado era un investigador que estudiaba N.salmincola en salmones coho juveniles, y sin darse cuenta había iniciado la infección por contacto de la mano a la boca durante el estudio de 3 meses de duración.
Reservorio
Los reservorios de N. salmincola son mapaches, visones y zorrillos. Los reservorios son organismos que albergan parásitos dentro de sí mismos sin sufrir ningún signo de patología y propagan los parásitos a través de su comportamiento natural. Por ejemplo, los mapaches propagan naturalmente N. salmincola porque con frecuencia comen pescado y defecan huevos parásitos en el agua o cerca de ella, donde las etapas larvarias posteriores pueden continuar su ciclo de vida.
Vector
Los vectores son organismos que transmiten parásitos de un huésped a otro. Los caracoles de corriente Juga plicifera son vectores biológicos de una etapa larvaria de N. salmincola . Los salmónidos y algunos peces no salmónidos son vectores de las metacercarias de N. salmincola. Tanto los peces de agua dulce como los del océano pueden ser vectores parásitos. Los peces que actúan como segundos huéspedes intermediarios son diferentes especies de las familias Salmonidae, Cottidae y Cyprinidae. Entre los treinta y cuatro huéspedes secundarios naturales y experimentales que se encuentran en la literatura científica se encuentran la trucha asesina costera, la trucha arco iris, el salmón coho, el salmón chum y el salmón kokanee. Se producen más infecciones en los peces salmónidos que en los no salmónidos. En particular, los peces salmónidos de los géneros Salmo, Oncorhynchus y Salvelinus desempeñan un papel importante en el ciclo de vida de N. salmincola . El parásito en sí mismo también es un vector de Neorickettsia helminthoeca .
Anfitriones definitivos
Los huéspedes definitivos incluyen aves y mamíferos que se alimentan de pescado. Los huéspedes definitivos más comunes son el perro doméstico, el gato y el zorro rojo. Los seres humanos también son huéspedes definitivos de N. salmincola . Una larga lista de hospedadores definitivos experimentales incluye el hámster y la rata de madera. Un estudio experimental no logró infectar a dos ratas blancas y dos ratones blancos. Los trematodos existen a lo largo de todo el intestino delgado en animales más pequeños como los hámsteres, mientras que existen solo en el extremo superior del intestino delgado en animales más grandes como los perros.
Periodo de incubación
Después de la ingestión de pescado infectado con N. salmincola , se necesitan aproximadamente 1 semana para que aparezcan los síntomas, es decir, para que se detecten los huevos en las heces.
Morfología
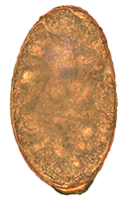
Los huevos de N. salmincola son de color marrón claro, ovoides y operculados en un extremo, con una pequeña proyección roma en el otro extremo. Miden 0.087 mm a 0.097 mm por 0.038 mm a 0.055 mm. Normalmente hay de 5 a 16 huevos en el útero y su pesadez les permite hundirse rápidamente en el agua.
N. salmincola es un trematodo digénico, lo que significa que es un gusano no segmentado que se aplana dorsoventralmente. Los gusanos adultos alternan la forma de "una esfera a una varilla roma larga". Los gusanos miden 0,8 a 1,1 mm de largo y 0,3 a 0,5 mm de ancho y son hermafroditas, y tienen órganos reproductores masculinos y femeninos en el mismo organismo. Los dos grandes testículos ovalados miden de 0,2 a 0,3 mm de largo y el ovario redondo tiene de 0,07 a 0,11 mm de diámetro. N. salmincola tiene una bolsa de cirro prominente u órgano hueco que rodea el órgano copulador masculino, pero no tiene vesícula seminal. Fiel a su carácter de trematodo, tiene una ventosa oral de 0,15 a 0,18 mm de diámetro y una ventosa ventral de 0,12 a 0,13 mm de diámetro. Las ventosas orales y ventrales se utilizan para agarrar y arrastrarse activamente por el tejido intestinal de su huésped, aunque el gusano no deja daños mecánicos importantes.
Ciclo vital
El adulto pone huevos dentro del hospedador vertebrado. El vertebrado distribuye los huevos en sus heces. La primera etapa larvaria, los miracidios, se desarrollan dentro de los huevos, eclosionan y se alejan nadando. Luego, los miracidios penetran en el primer hospedador intermedio, el caracol de corriente Juga plicifera . Después de un mayor desarrollo en el caracol de arroyo, la larva de N. salmincola se convierte en rediae, que da lugar a cercariae. Las cercarias emergen del caracol y penetran en el segundo hospedador intermedio, el pez salmónido (algunos no salmónidos). Los parásitos se convierten en metacercarias y se enquistan dentro de los riñones, músculos y aletas de los salmónidos. Los parásitos ingresan a su huésped final, incluidos los cánidos y los seres humanos, tras la ingestión de los peces infectados y se convierten en gusanos adultos que producen huevos que se transmiten a las heces del huésped.
Información detallada sobre las etapas del ciclo de vida
Huevos y miracidios: los huevos que pasan por las heces no están embrionados . Los estudios experimentales demuestran que los huevos recolectados a temperatura ambiente requieren de 75 días a 200 días para eclosionar. La tasa de eclosión de los miracidios de los huevos aumenta con la disminución de la temperatura y la mortalidad de los huevos aumenta con el aumento de la temperatura. Los miracidios completamente desarrollados dentro de los huevos se contraen y alargan repetidamente, y los miracidios recién emergidos nadan en "curvas características, largas y elegantes". Los miracidios parecen no tener atracción por albergar caracoles, chocando con los caracoles sin intentar penetrarlos e infectarlos.
Rediae: Las rediae son la segunda etapa larvaria del ciclo de vida de los trematodos, que se desarrolla a partir del miracidum y contiene células germinales que se convierten en cercarias. Las rediae se encuentran en el segundo hospedador intermedio, el caracol. Las redias pueden oscilar entre 0,45 mm y 3 mm, y las redias más grandes pueden contener hasta 76 cercarias. Rediae y cercariae se encuentran en todos los tejidos del caracol huésped, pero principalmente en las gónadas y la glándula digestiva. Rediae destruye las gónadas, invaden el hepatopáncreas, lo dañan por 1) aumento de la presión por crecimiento rápido, 2) ingestión activa por el parásitos, y 3) la disposición de desechos parasitarios. Además, los parásitos absorben glucógeno y lípidos del hepatopáncreas.
Cercarias: Las cercarias miden de 0,31 mm a 0,47 mm por 0,03 mm a 0,15 mm y viven hasta 48 horas en el agua. Tienen una tendencia a infectar caracoles que miden al menos 2,5 cm de longitud, aunque también se ha observado que los caracoles más pequeños arrojan cercarias. Las cercarias se desprenden intermitentemente por miles, ingresan a la cavidad del manto del caracol y salen a la deriva con la "corriente de agua exhausta en el lado derecho de la cabeza del caracol". Se encontró que las cercarias de los caracoles en agua salobre de baja salinidad sobrevivían más tiempo que los caracoles en agua dulce.
Una vez que se desprenden las cercarias del caracol, este se contrae repetidamente hasta que entra en contacto con un pez y penetra debajo de su piel en 30 segundos a 2 minutos. Las cercarias penetran más en el sistema sanguíneo portal renal, en el riñón y tejidos más profundos en la base de la cola. Los puntos de penetración son fácilmente visibles, ya que la piel, las aletas y las colas de los peces parecen estar muy erosionadas y dañadas. Las cercarias también pueden infectar indirectamente a los peces, si los peces se comen las cercarias por vía oral.
Metacercarias: Las cercarias pierden sus colas en el acto de penetración y se enquistan como metacercarias en casi cualquier tejido de los salmónidos. La nueva pared del quiste es delgada, transparente y se rompe fácilmente. Si la pared del quiste se rompe, las metacercarias salen y vuelven a enquistarse unas horas más tarde en una pared del quiste más grande y resistente. Si bien los quistes se pueden encontrar en todos los tejidos de los peces, la mayor parte del enquistamiento ocurre en los riñones y los músculos corporales de los peces salmónidos, y en las branquias y aletas de los peces no salmónidos. Las cercarias penetran menos profundamente en los peces no salmónidos que en los salmónidos. Los peces infectados experimentan una disminución en su actividad de natación y pérdida del equilibrio, y no es raro que los peces tengan entre 1000 y 2000 metacercarias en sus tejidos.
Es importante destacar que las metacercarias pueden destruirse cocinando o congelando el pescado infectado.
Caracol: El caracol huésped Juga plicifera prevalece en los arroyos de la costa y prefiere rocas grandes, puentes, tablas viejas y escombros en el fondo del lecho de los arroyos. Rara vez migra a aguas poco profundas. La infección de los caracoles es alta en comparación con el número de cercarias que arroja, ya que el desarrollo larvario continúa lentamente durante un largo período de tiempo. La evidencia de infección mixta varió entre los estudios, pero los caracoles con grandes cantidades de N. salmincola no fueron parasitados por otros trematodos. También se descubrió que las incidencias mensuales de infección en caracoles oscilaban entre el 9% y el 52% después de examinar más de 3000 caracoles cada mes durante 10 meses, y que las cercarias maduras infectaban a los caracoles de forma estacional. Las cercarias maduras tenían más probabilidades de infectar a los caracoles entre finales de abril y noviembre.
Neorickettsia helmintheoca Neorickettsia helmintheoca es el agente etiológico de la intoxicación por salmón, que se encuentra presente en todas las etapas del trematodo. Tiene un tamaño de 0,3 micrómetros y una tinción de Giemsa púrpura indica que es Gram negativo. Hasta ahora, solo los cánidos son susceptibles a la enfermedad por rickettsia y todavía no se sabe cómo la rickettsia abandona el vector trematodo y llega a los tejidos del huésped. Los experimentos muestran que la bacteria conduce a la necrosis de los folículos linfáticos, ulceración y hemorragia severa en su huésped.
Pruebas de diagnóstico
- Historia de comer pescado crudo
- Examen de heces en busca de huevos de N. salmincola
- Debido a que cada gusano adulto contiene solo unos pocos huevos, es probable que los pacientes con infecciones leves tengan pruebas de heces negativas. El uso de preparaciones teñidas con tricrómico en lugar de concentrados de formalina-acetato de etilo fue más sensible para identificar casos.
Manejo y terapia
Praziquantel, 20 mg / kg de peso corporal, tres veces al día. El praziquantel provoca la contracción inmovilizada del gusano, de modo que ya no puede agarrar las paredes intestinales y puede ser eliminado del cuerpo. Tres dosis de 2 g de niclosamida o dos dosis de 50 mg / kg de bitionol también han sido eficaces cuando no se disponía de praziquantel o se rechazaba el tratamiento. Sin embargo, una sola dosis de 2 g de niclosamina fue ineficaz, al igual que 100 mg de mebendazol por vía oral dos veces al día durante tres días. Si la diarrea se repite, es posible que también se necesiten suplementos generales para mantener el equilibrio de electrolitos y cumplir con los requisitos nutricionales.
Epidemiología
Nanophyetus salmincola se limita al rango geográfico de sus huéspedes intermediarios, principalmente el noroeste del Pacífico de EE. UU. Los caracoles de arroyo se encuentran al oeste de las Montañas Cascade en Oregon, al norte de la Península Olímpica en Washington y en parte del norte de California. Es "el trematodo sistémico más común en los Estados Unidos".
Estrategias de prevención y salud pública
- Cocine bien el pescado
- Congele el pescado durante al menos 24 horas.
- Pesque lejos de lugares conocidos como endémicos de caracoles (de lo contrario, asegúrese de cocinar el pescado completamente)
- Tome precauciones al manipular pescado (evite la transmisión de las metacercarias de la mano a la boca y tenga cuidado con la contaminación de las manos por peces muy infectados)
- Revise los peces periódicamente para detectar signos de infección, como quistes o sitios de irritación por la penetración de cercarariae (pertinente a empresas pesqueras, mercados de pescado y restaurantes)
- Informar las fuentes de peces infectados (cuerpos de agua, empresas pesqueras, restaurantes)
- Consuma pescado crudo solo de fuentes confiables, como restaurantes de renombre
- Utilice molusquicidas si se puede utilizar en la práctica en masas de agua más pequeñas.
- Mantenga a los perros alejados de los arroyos, asegurándose de que defecan lejos de los hábitats de los caracoles.