Enfermedad de Lyme - Lyme disease
| enfermedad de Lyme | |
|---|---|
| Otros nombres | Borreliosis de Lyme |
 | |
| Una garrapata de venado adulta (la mayoría de los casos de Lyme son causados por garrapatas ninfales más que por garrapatas adultas) | |
| Especialidad | Enfermedad infecciosa |
| Síntomas | Ampliación del área de enrojecimiento en el lugar de la picadura de una garrapata , fiebre , dolor de cabeza , cansancio |
| Complicaciones | Parálisis del nervio facial , artritis , meningitis. |
| Inicio habitual | Una semana después de un bocado |
| Causas | Borrelia transmitida por garrapatas |
| Método de diagnóstico | Basado en síntomas, exposición a garrapatas, análisis de sangre |
| Prevención | Prevención de picaduras de garrapatas (ropa de las extremidades, DEET ), doxiciclina |
| Medicamento | Doxiciclina , amoxicilina , ceftriaxona , cefuroxima |
| Frecuencia | ~ 476.000 por año en EE. UU. (2010 - 2018) |
La enfermedad de Lyme , también conocida como borreliosis de Lyme , es una enfermedad transmitida por vectores causada por la bacteria Borrelia que se transmite por garrapatas del género Ixodes . El signo más común de infección es una erupción roja en expansión , conocida como eritema migratorio , que aparece en el sitio de la picadura de la garrapata aproximadamente una semana después de que ocurrió. La erupción no suele causar picazón ni dolor. Aproximadamente del 70 al 80% de las personas infectadas desarrollan una erupción. El diagnóstico temprano puede resultar difícil. Otros síntomas tempranos pueden incluir fiebre, dolor de cabeza y cansancio . Si no se trata, los síntomas pueden incluir pérdida de la capacidad para mover uno o ambos lados de la cara , dolores en las articulaciones , dolores de cabeza intensos con rigidez en el cuello o palpitaciones del corazón , entre otros. Meses o años después, pueden ocurrir episodios repetidos de dolor e hinchazón en las articulaciones. Ocasionalmente, las personas desarrollan dolores punzantes u hormigueo en brazos y piernas. A pesar del tratamiento adecuado, alrededor del 10 al 20% de las personas desarrollan dolores en las articulaciones, problemas de memoria y cansancio durante al menos seis meses.
La enfermedad de Lyme se transmite a los humanos por la picadura de garrapatas infectadas del género Ixodes . En los Estados Unidos, las garrapatas preocupantes suelen ser del tipo Ixodes scapularis y deben permanecer adheridas durante al menos 36 horas antes de que la bacteria se propague. En Europa, las garrapatas Ixodes ricinus pueden propagar la bacteria más rápidamente. En América del Norte, la bacteria Borrelia burgdorferi , B. bissettiae , y B. mayonii causan la enfermedad de Lyme. En Europa y Asia, Borrelia afzelii , Borrelia garinii , B. spielmanii , y otras 4 especies también pueden causar la enfermedad. La enfermedad no parece ser transmisible entre personas, por otros animales o a través de los alimentos. El diagnóstico se basa en una combinación de síntomas, antecedentes de exposición a garrapatas y posiblemente pruebas de anticuerpos específicos en la sangre. Los análisis de sangre suelen ser negativos en las primeras etapas de la enfermedad. Las pruebas de garrapatas individuales no suelen ser útiles.
La prevención incluye los esfuerzos para prevenir las picaduras de garrapatas mediante el uso de ropa que cubra los brazos y las piernas, y el uso de DEET o repelentes de insectos a base de picaridina . El uso de pesticidas para reducir el número de garrapatas también puede ser eficaz. Las garrapatas se pueden eliminar con pinzas . Si la garrapata extraída estaba llena de sangre, se puede usar una sola dosis de doxiciclina para prevenir el desarrollo de una infección, pero generalmente no se recomienda ya que el desarrollo de una infección es poco común. Si se desarrolla una infección, varios antibióticos son eficaces, como doxiciclina, amoxicilina y cefuroxima . El tratamiento estándar suele durar dos o tres semanas. Algunas personas desarrollan fiebre y dolores musculares y articulares debido al tratamiento, que pueden durar uno o dos días. En aquellos que desarrollan síntomas persistentes, no se ha encontrado que la terapia con antibióticos a largo plazo sea útil.
La enfermedad de Lyme es la enfermedad más común transmitida por garrapatas en el hemisferio norte . Se estima que afecta a 300.000 personas al año en Estados Unidos y a 65.000 personas al año en Europa. Las infecciones son más comunes en la primavera y principios del verano. La enfermedad de Lyme fue diagnosticada como una condición separada por primera vez en 1975 en Lyme, Connecticut . Originalmente se confundió con la artritis reumatoide juvenil . La bacteria involucrada fue descrita por primera vez en 1981 por Willy Burgdorfer . Los síntomas crónicos que siguen al tratamiento están bien descritos y se conocen como "síndrome de la enfermedad de Lyme postratamiento" (SLTPD). PTLDS es diferente de la enfermedad de Lyme crónica , un término que ya no es respaldado por la comunidad científica y que diferentes grupos utilizan de diferentes maneras. Algunos proveedores de atención médica afirman que el SLPTD es causado por una infección persistente, pero no se cree que sea cierto porque no se puede encontrar evidencia de una infección persistente después del tratamiento estándar. Una vacuna para la enfermedad de Lyme se comercializó en los Estados Unidos entre 1998 y 2002, pero se retiró del mercado debido a las malas ventas. Se están realizando investigaciones para desarrollar nuevas vacunas.
Signos y síntomas

La enfermedad de Lyme puede afectar a múltiples sistemas corporales y producir una amplia gama de síntomas. No todas las personas con la enfermedad de Lyme tienen todos los síntomas, y muchos de los síntomas no son específicos de la enfermedad de Lyme, pero también pueden ocurrir con otras enfermedades.
El período de incubación desde la infección hasta la aparición de los síntomas suele ser de una a dos semanas, pero puede ser mucho más corto (días) o mucho más largo (meses o años). Los síntomas de Lyme ocurren con mayor frecuencia de mayo a septiembre en el hemisferio norte, porque la etapa ninfal de la garrapata es responsable de la mayoría de los casos. Existe una infección asintomática , pero ocurre en menos del 7% de las personas infectadas en los Estados Unidos. La infección asintomática puede ser mucho más común entre los infectados en Europa.
Infección localizada temprana
La infección localizada temprana puede ocurrir cuando la infección aún no se ha extendido por todo el cuerpo. Solo se ve afectado el sitio donde la infección entró en contacto por primera vez con la piel. El signo inicial de aproximadamente el 80% de las infecciones de Lyme es una erupción de eritema migratorio (EM) en el sitio de la picadura de una garrapata, a menudo cerca de los pliegues de la piel, como la axila , la ingle o la parte posterior de la rodilla , en el tronco , debajo de la ropa. correas o en el cabello, las orejas o el cuello de los niños. La mayoría de las personas que se infectan no recuerdan haber visto una garrapata o una picadura. El exantema aparece típicamente una o dos semanas (rango de 3 a 32 días) después de la picadura y se expande 2 a 3 cm por día hasta un diámetro de 5 a 70 cm (mediana 16 cm). La erupción suele ser circular u ovalada, roja o azulada y puede tener un centro elevado u oscuro. En aproximadamente el 79% de los casos en Europa, pero solo el 19% de los casos en áreas endémicas de los EE. UU., La erupción desaparece gradualmente desde el centro hacia los bordes, posiblemente formando un patrón de "ojo de buey". El sarpullido puede sentirse caliente, pero por lo general no produce picazón, rara vez es sensible o doloroso y tarda hasta cuatro semanas en resolverse si no se trata.
La erupción EM a menudo se acompaña de síntomas de una enfermedad similar a un virus, que incluyen fatiga, dolor de cabeza, dolores corporales, fiebre y escalofríos, pero generalmente no náuseas ni problemas de las vías respiratorias superiores. Estos síntomas también pueden aparecer sin una erupción o persistir después de que la erupción desaparece. Lyme puede progresar a etapas posteriores sin estos síntomas ni una erupción.
Las personas con fiebre alta durante más de dos días o cuyos otros síntomas de una enfermedad de tipo viral no mejoran a pesar del tratamiento con antibióticos para la enfermedad de Lyme, o que tienen niveles anormalmente bajos de glóbulos blancos o rojos o plaquetas en la sangre, deben ser investigadas para detectar posibles coinfección con otras enfermedades transmitidas por garrapatas , como ehrlichiosis y babesiosis .
Infección diseminada temprana
Días o semanas después del inicio de la infección local, la bacteria Borrelia puede diseminarse a través del sistema linfático o del torrente sanguíneo. En 10 a 20% de los casos no tratados, las erupciones EM se desarrollan en sitios de todo el cuerpo que no guardan relación con la picadura original de la garrapata. Los dolores musculares transitorios y los dolores articulares también son comunes.
En aproximadamente el 10-15% de las personas que no reciben tratamiento, Lyme causa problemas neurológicos conocidos como neuroborreliosis . La neuroborreliosis temprana aparece típicamente 4 a 6 semanas (rango 1 a 12 semanas) después de la picadura de garrapata e involucra alguna combinación de meningitis linfocítica, neuritis craneal, radiculopatía y / o mononeuritis múltiple. La meningitis linfocítica causa cambios característicos en el líquido cefalorraquídeo (LCR) y puede ir acompañada durante varias semanas de dolor de cabeza variable y, con menos frecuencia, signos de meningitis leves , como incapacidad para flexionar el cuello completamente e intolerancia a las luces brillantes , pero generalmente no o solo fiebre muy baja. Después de varios meses, la neuroborreliosis también puede presentar síntomas otorrinolaringológicos. Hasta un 76,5% de estos otorrinolaringológicos se presentan como acúfenos, el síntoma más común. Vértigo y mareos (53,7%) y pérdida de audición (16,7%) fueron los siguientes síntomas más comunes. En los niños, también puede ocurrir una pérdida parcial de la visión . La neuritis craneal es una inflamación de los nervios craneales . Cuando se debe a Lyme, generalmente causa parálisis facial que dificulta el parpadeo, la sonrisa y la masticación en uno o ambos lados de la cara. También puede causar visión doble intermitente . La radiculopatía de Lyme es una inflamación de las raíces nerviosas espinales que a menudo causa dolor y, con menor frecuencia , debilidad , entumecimiento o sensación alterada en las áreas del cuerpo servidas por los nervios conectados a las raíces afectadas , por ejemplo, extremidades o partes del tronco. . El dolor a menudo se describe como diferente a cualquier otro sentido anteriormente, insoportable, migratorio, peor por la noche, rara vez simétrico y, a menudo, acompañado de una alteración extrema del sueño. La mononeuritis múltiple es una inflamación que causa síntomas similares en uno o más nervios periféricos no relacionados. En raras ocasiones, neuroborreliosis temprano puede implicar la inflamación de la cerebro o la médula espinal , con síntomas tales como confusión, marcha anormal, movimientos oculares, o el habla , alteración del movimiento , alteración de la planificación de motor , o sacudiendo .
En América del Norte, la parálisis facial es la presentación típica de neuroborreliosis temprana, que ocurre en 5 a 10% de las personas no tratadas, en aproximadamente 75% de los casos acompañada de meningitis linfocítica. La radiculopatía de Lyme se informa con la mitad de frecuencia, pero muchos casos pueden pasar desapercibidos. En los adultos europeos, la presentación más común es una combinación de meningitis linfocítica y radiculopatía conocida como síndrome de Bannwarth , acompañada en un 36-89% de los casos de parálisis facial. En este síndrome, el dolor radicular tiende a comenzar en la misma región del cuerpo que el exantema de eritema migratorio inicial , si lo hubiera, y precede a una posible parálisis facial y otras alteraciones del movimiento . En casos extremos, puede producirse un deterioro permanente de la función motora o sensorial de las extremidades inferiores. En los niños europeos, las manifestaciones más frecuentes son la parálisis facial (en el 55%), otras neuritis craneales y la meningitis linfocítica (en el 27%).
En alrededor del 4% al 10% de los casos no tratados en los EE. UU. Y del 0,3% al 4% de los casos no tratados en Europa, por lo general entre junio y diciembre, aproximadamente un mes (rango de 4 días a 7 meses) después de la picadura de la garrapata, la infección puede causar problemas cardíacos. complicaciones conocidas como carditis de Lyme . Los síntomas pueden incluir palpitaciones del corazón (en el 69% de las personas), mareos , desmayos , dificultad para respirar y dolor en el pecho . También pueden estar presentes otros síntomas de la enfermedad de Lyme, como erupción EM , dolores en las articulaciones , parálisis facial , dolores de cabeza o dolor radicular . En algunas personas, sin embargo, la carditis puede ser la primera manifestación de la enfermedad de Lyme. La carditis de Lyme en el 19–87% de las personas impacta negativamente en el sistema de conducción eléctrica del corazón, causando un bloqueo auriculoventricular que a menudo se manifiesta como ritmos cardíacos que alternan en minutos entre anormalmente lentos y anormalmente rápidos. En el 10-15% de las personas, Lyme causa complicaciones miocárdicas como cardiomegalia , disfunción del ventrículo izquierdo o insuficiencia cardíaca congestiva.
Otra afección de la piel, que se encuentra en Europa pero no en América del Norte, es el linfocitoma borrelial , un bulto violáceo que se desarrolla en el lóbulo de la oreja, el pezón o el escroto .
Infección diseminada tardía
Después de varios meses, las personas no tratadas o tratadas inadecuadamente pueden desarrollar síntomas crónicos que afectan muchas partes del cuerpo, incluidas las articulaciones, los nervios, el cerebro, los ojos y el corazón.
La artritis de Lyme se presenta en hasta un 60% de las personas que no reciben tratamiento, y por lo general comienza aproximadamente seis meses después de la infección. Por lo general, afecta solo una o algunas articulaciones, a menudo una rodilla o posiblemente la cadera , otras articulaciones grandes o la articulación temporomandibular . Suele haber un gran derrame e hinchazón en las articulaciones , pero solo dolor leve o moderado. Sin tratamiento, la hinchazón y el dolor suelen desaparecer con el tiempo, pero vuelven periódicamente. Los quistes de Baker pueden formarse y romperse. En algunos casos, se produce erosión articular.
Los síntomas neurológicos crónicos ocurren en hasta el 5% de las personas que no reciben tratamiento. Es posible que se desarrolle una neuropatía periférica o polineuropatía , que cause sensaciones anormales como entumecimiento, hormigueo o ardor que comience en los pies o las manos y, con el tiempo, posiblemente suba por las extremidades. Una prueba puede mostrar una reducción de la sensación de vibraciones en los pies. Una persona afectada puede sentirse como si estuviera usando una media o un guante sin hacerlo realmente.
Un síndrome neurológico llamado encefalopatía de Lyme se asocia con dificultades sutiles de memoria y cognitivas, insomnio , una sensación general de malestar y cambios en la personalidad. Sin embargo, problemas como la depresión y la fibromialgia son tan comunes en las personas con enfermedad de Lyme como en la población general.
Lyme puede causar una encefalomielitis crónica que se asemeja a la esclerosis múltiple . Puede ser progresivo y puede implicar deterioro cognitivo, confusión mental, migrañas , problemas de equilibrio, debilidad en las piernas, marcha torpe, parálisis facial, problemas de vejiga, vértigo y dolor de espalda. En casos raros, la enfermedad de Lyme no tratada puede causar psicosis franca , que se ha diagnosticado erróneamente como esquizofrenia o trastorno bipolar . Pueden ocurrir ataques de pánico y ansiedad; además, se pueden observar conductas delirantes, incluyendo delirios somatomorfos , a veces acompañadas de un síndrome de despersonalización o desrealización, donde las personas comienzan a sentirse desapegadas de sí mismas o de la realidad.
La acrodermatitis crónica atrófica (ACA) es un trastorno cutáneo crónico que se observa principalmente en Europa entre los ancianos. La ACA comienza como una mancha azul rojiza de piel descolorida, a menudo en el dorso de las manos o los pies. La lesión se atrofia lentamente durante varias semanas o meses, y la piel se vuelve primero delgada y arrugada y luego, si no se trata, se seca por completo y no tiene pelo.
Porque


La enfermedad de Lyme es causada por espiroquetas , bacterias espirales del género Borrelia . Las espiroquetas están rodeadas de peptidoglicano y flagelos , junto con una membrana externa similar a las bacterias Gram negativas. Debido a su envoltura de doble membrana, las bacterias Borrelia a menudo se describen erróneamente como Gram negativas a pesar de las considerables diferencias en los componentes de su envoltura de las bacterias Gram-negativas. Las especies de Borrelia relacionadas con Lyme se conocen colectivamente como Borrelia burgdorferi sensu lato y muestran una gran diversidad genética .
B. burgdorferi sensu lato es un complejo de especies compuesto por 20 genoespecies aceptadas y tres propuestas. Se sabe que ocho especies causan la enfermedad de Lyme: B. mayonii (encontrada en América del Norte), B. burgdorferi sensu stricto , B. bissettiae (ambas encontradas en América del Norte y Europa), B. afzelii , B. garinii, B. spielmanii, y B. lusitaniae (todos encontrados en Eurasia ). Algunos estudios también han propuesto que B. valaisiana a veces puede infectar a los humanos, pero esta especie no parece ser una causa importante de enfermedad.
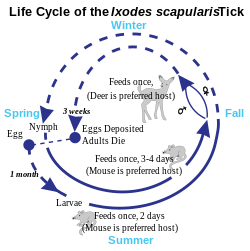
Ciclo de vida de las garrapatas
Hay tres etapas en el ciclo de vida de una garrapata. Larva, ninfa y adulto. Durante la etapa de ninfa, las garrapatas transmiten con mayor frecuencia la enfermedad de Lyme y suelen ser más activas a fines de la primavera y principios del verano en las regiones donde el clima es templado. Durante la etapa adulta, la transmisión de la enfermedad de Lyme es menos común debido al hecho de que es menos posible que las garrapatas adultas piquen a los humanos y porque tienden a ser de mayor tamaño y, por lo tanto, pueden verse y eliminarse fácilmente.
Transmisión
La enfermedad de Lyme se clasifica como zoonosis , ya que se transmite a los humanos desde un reservorio natural entre los pequeños mamíferos y las aves por medio de garrapatas que se alimentan de ambos conjuntos de huéspedes . Las garrapatas de cuerpo duro del género Ixodes son los vectores de la enfermedad de Lyme (también el vector de Babesia ). La mayoría de las infecciones son causadas por garrapatas en la etapa ninfal , porque son muy pequeñas y, por lo tanto, pueden alimentarse durante largos períodos de tiempo sin ser detectadas. Las garrapatas ninfa son generalmente del tamaño de una semilla de amapola y, a veces, tienen la cabeza oscura y el cuerpo translúcido. O las garrapatas ninfales pueden ser más oscuras. (Las garrapatas larvarias más jóvenes rara vez se infectan). Aunque los ciervos son los huéspedes preferidos de las garrapatas de ciervo adultas, y las poblaciones de garrapatas son mucho más bajas en ausencia de ciervos, las garrapatas generalmente no adquieren Borrelia de los ciervos, sino que las obtienen de las garrapatas pequeñas infectadas. mamíferos como el ratón de patas blancas y, ocasionalmente, aves. Las áreas donde Lyme es común se están expandiendo.
Dentro del intestino medio de la señal, la Borrelia ' s proteína de superficie exterior se une al receptor de garrapata para OspA A (OspA), conocido como TROSPA. Cuando la garrapata se alimenta, la Borrelia regula negativamente la OspA y regula positivamente la OspC, otra proteína de superficie. Después de que las bacterias migran desde el intestino medio a las glándulas salivales, OspC se une a Salp15, una proteína salival de garrapatas que parece tener efectos inmunosupresores que aumentan la infección. La infección exitosa del huésped mamífero depende de la expresión bacteriana de OspC.
Las picaduras de garrapatas a menudo pasan desapercibidas debido al pequeño tamaño de la garrapata en su etapa ninfal, así como a las secreciones de garrapatas que evitan que el huésped sienta picazón o dolor por la picadura. Sin embargo, la transmisión es bastante rara, con solo alrededor del 1.2 al 1.4 por ciento de las picaduras de garrapatas reconocidas que resultan en la enfermedad de Lyme.
En Europa, el vector principal es Ixodes ricinus , que también se llama garrapata de oveja o garrapata de ricino . En China, Ixodes persulcatus (la garrapata de la taiga) es probablemente el vector más importante. En América del Norte, la garrapata de patas negras o la garrapata del venado ( Ixodes scapularis ) es el principal vector en la costa este.
Es poco probable que la garrapata estrella solitaria ( Amblyomma americanum ), que se encuentra en todo el sureste de los Estados Unidos hasta el oeste de Texas , transmita las espiroquetas de la enfermedad de Lyme , aunque puede estar implicada en un síndrome relacionado llamado enfermedad eruptiva asociada a garrapatas del sur , que se asemeja a una forma leve de la enfermedad de Lyme.
En la costa oeste de los Estados Unidos , el vector principal es la garrapata de patas negras occidental ( Ixodes pacificus ). La tendencia de esta especie de garrapata a alimentarse predominantemente de especies hospedadoras como el lagarto de valla occidental que son resistentes a la infección por Borrelia parece disminuir la transmisión de la enfermedad de Lyme en Occidente.
La transmisión puede ocurrir a través de la placenta durante el embarazo y, como ocurre con otras enfermedades por espiroquetas, es posible que se produzcan resultados adversos en el embarazo con una infección no tratada; el tratamiento oportuno con antibióticos reduce o elimina este riesgo.
No existe evidencia científica que respalde la transmisión de la enfermedad de Lyme a través de transfusiones de sangre, contacto sexual o leche materna.
Coinfecciones transmitidas por garrapatas
Las garrapatas que transmiten B. burgdorferi a los humanos también pueden portar y transmitir varios otros parásitos, como Babesia microti y Anaplasma phagocytophilum , que causan las enfermedades babesiosis y anaplasmosis granulocítica humana (HGA), respectivamente. Entre las personas con enfermedad de Lyme temprana, dependiendo de su ubicación, del 2 al 12% también tendrá HGA y del 2 al 40% tendrá babesiosis. Las garrapatas en ciertas regiones, incluidas las tierras a lo largo del este del Mar Báltico, también transmiten virus que causan encefalitis transmitida por garrapatas .
Las coinfecciones complican los síntomas de Lyme, especialmente el diagnóstico y el tratamiento. Es posible que una garrapata lleve y transmita una de las coinfecciones y no Borrelia , lo que dificulta el diagnóstico y, a menudo, es difícil de alcanzar. Los Centros para el Control y la Prevención de Enfermedades estudiaron 100 garrapatas en zonas rurales de Nueva Jersey y encontraron que el 55% de las garrapatas estaban infectadas con al menos uno de los patógenos.
Fisiopatología
B. burgdorferi puede diseminarse por todo el cuerpo durante el curso de la enfermedad y se ha encontrado en la piel, el corazón, las articulaciones, el sistema nervioso periférico y el sistema nervioso central. Muchos de los signos y síntomas de la enfermedad de Lyme son consecuencia de la respuesta inmunitaria a la espiroqueta en esos tejidos.
B. burgdorferi se inyecta en la piel mediante la picadura de una garrapata Ixodes infectada . La saliva de las garrapatas, que acompaña a la espiroqueta en la piel durante el proceso de alimentación, contiene sustancias que alteran la respuesta inmunitaria en el lugar de la picadura. Esto proporciona un entorno protector donde la espiroqueta puede establecer una infección. Las espiroquetas se multiplican y migran hacia afuera dentro de la dermis . La respuesta inflamatoria del huésped a las bacterias en la piel causa la característica lesión EM circular. Sin embargo, los neutrófilos , que son necesarios para eliminar las espiroquetas de la piel, no aparecen en la cantidad necesaria en la lesión EM en desarrollo porque la saliva de la garrapata inhibe la función de los neutrófilos. Esto permite que la bacteria sobreviva y eventualmente se disemine por todo el cuerpo.
Días o semanas después de la picadura de la garrapata, las espiroquetas se diseminan a través del torrente sanguíneo a las articulaciones, el corazón, el sistema nervioso y sitios distantes de la piel, donde su presencia da lugar a una variedad de síntomas de la enfermedad diseminada. La propagación de B. burgdorferi se ve favorecida por la unión de la proteasa plasmina del huésped a la superficie de la espiroqueta.
Si no se trata, la bacteria puede persistir en el cuerpo durante meses o incluso años, a pesar de la producción de anticuerpos contra B. burgdorferi por parte del sistema inmunológico. Las espiroquetas pueden evitar la respuesta inmune al disminuir la expresión de proteínas de superficie que son el objetivo de los anticuerpos, la variación antigénica de la proteína de superficie VlsE, inactivando componentes inmunes clave como el complemento y escondiéndose en la matriz extracelular , que puede interferir con la función de inmunidad. factores.
En el cerebro, B. burgdorferi puede inducir a los astrocitos a sufrir astrogliosis (proliferación seguida de apoptosis ), lo que puede contribuir a la neurodisfunción. Las espiroquetas también pueden inducir a las células huésped a secretar ácido quinolínico , que estimula el receptor de NMDA en las células nerviosas, lo que puede explicar la fatiga y el malestar que se observa con la encefalopatía de Lyme . Además, la patología difusa de la sustancia blanca durante la encefalopatía de Lyme puede interrumpir las conexiones de la sustancia gris y podría explicar los déficits en la atención, la memoria, la capacidad visuoespacial, la cognición compleja y el estado emocional. La enfermedad de la sustancia blanca puede tener un mayor potencial de recuperación que la enfermedad de la sustancia gris, quizás porque la pérdida neuronal es menos común. Se ha observado resolución de las hiperintensidades de la sustancia blanca de la resonancia magnética después del tratamiento con antibióticos.
El triptófano , un precursor de la serotonina , parece estar reducido dentro del sistema nervioso central en una serie de enfermedades infecciosas que afectan al cerebro, incluida la de Lyme. Los investigadores están investigando si esta secreción de neurohormonas es la causa de los trastornos neuropsiquiátricos que se desarrollan en algunas personas con borreliosis.
Estudios inmunologicos
La exposición a la bacteria Borrelia durante la enfermedad de Lyme posiblemente cause una respuesta inflamatoria dañina y de larga duración , una forma de enfermedad autoinmune inducida por patógenos. La producción de esta reacción podría deberse a una forma de mimetismo molecular , en el que Borrelia evita ser asesinado por el sistema inmunológico al parecerse a partes normales de los tejidos del cuerpo.
Los síntomas crónicos de una reacción autoinmune podrían explicar por qué algunos síntomas persisten incluso después de que las espiroquetas han sido eliminadas del cuerpo. Esta hipótesis puede explicar por qué persiste la artritis crónica después de la terapia con antibióticos, similar a la fiebre reumática , pero su aplicación más amplia es controvertida.
Diagnóstico
La enfermedad de Lyme se diagnostica en función de los síntomas, hallazgos físicos objetivos (como eritema migratorio (EM), erupción cutánea, parálisis facial o artritis ), antecedentes de posible exposición a garrapatas infectadas y posiblemente pruebas de laboratorio . Las personas con síntomas de la enfermedad de Lyme temprana deben someterse a un examen de la piel de todo el cuerpo para detectar erupciones EM y preguntar si las erupciones de tipo EM se han manifestado en los últimos 1 o 2 meses. La presencia de una erupción EM y la exposición reciente a garrapatas (es decir, estar al aire libre en un hábitat probable de garrapatas donde Lyme es común , dentro de los 30 días posteriores a la aparición de la erupción) son suficientes para el diagnóstico de Lyme; no se necesita ni se recomienda confirmación de laboratorio. La mayoría de las personas que se infectan no recuerdan una garrapata o una picadura, y la erupción EM no tiene por qué verse como un ojo de buey (la mayoría de las erupciones EM en los EE. UU. No lo hacen) ni estar acompañada de otros síntomas. En los EE. UU., Lyme es más común en los estados de Nueva Inglaterra y el Atlántico medio y partes de Wisconsin y Minnesota , pero se está expandiendo a otras áreas. Varias áreas fronterizas de Canadá también tienen un alto riesgo de Lyme.
En ausencia de una erupción EM o antecedentes de exposición a garrapatas, el diagnóstico de Lyme depende de la confirmación del laboratorio. Las bacterias que causan la enfermedad de Lyme son difíciles de observar directamente en los tejidos corporales y también es difícil y requiere demasiado tiempo para crecer en el laboratorio. Las pruebas más utilizadas buscan en cambio la presencia de anticuerpos contra esas bacterias en la sangre. Un resultado positivo de una prueba de anticuerpos no prueba por sí solo una infección activa, pero puede confirmar una infección que se sospecha debido a síntomas, hallazgos objetivos y antecedentes de exposición a garrapatas en una persona. Debido a que hasta un 5-20% de la población normal tiene anticuerpos contra Lyme, las personas sin antecedentes y síntomas que sugieran la enfermedad de Lyme no deben someterse a pruebas de anticuerpos contra Lyme: un resultado positivo probablemente sería falso, lo que posiblemente provocaría un tratamiento innecesario.
En algunos casos, cuando la historia, los signos y los síntomas sugieren fuertemente una enfermedad de Lyme diseminada temprana, se puede iniciar un tratamiento empírico y reevaluarlo a medida que se disponga de los resultados de las pruebas de laboratorio.
Prueba de laboratorio
Las pruebas de anticuerpos en sangre mediante ELISA y Western blot es el método más utilizado para el diagnóstico de Lyme. Los Centros para el Control y la Prevención de Enfermedades (CDC) recomiendan un protocolo de dos niveles : primero se realiza la prueba ELISA sensible y, si es positiva o dudosa, se realiza la transferencia Western más específica . El sistema inmunológico tarda algún tiempo en producir anticuerpos en cantidad. Después de la aparición de la infección de Lyme, los anticuerpos de los tipos IgM e IgG por lo general se pueden detectar por primera vez, respectivamente, a las 2 a 4 semanas y a las 4 a 6 semanas, y alcanzan su punto máximo a las 6 a 8 semanas. Cuando aparece por primera vez una erupción EM, es posible que no haya anticuerpos detectables. Por lo tanto, se recomienda que no se realicen pruebas y que el diagnóstico se base en la presencia de erupción EM. Hasta 30 días después del inicio de la sospecha de infección de Lyme, la infección puede confirmarse mediante la detección de anticuerpos IgM o IgG; después de eso, se recomienda que solo se consideren los anticuerpos IgG. Un resultado positivo de IgM e IgG negativo después del primer mes de infección es generalmente indicativo de un resultado falso positivo. El número de anticuerpos IgM suele colapsar 4 a 6 meses después de la infección, mientras que los anticuerpos IgG pueden permanecer detectables durante años.
Se pueden usar otras pruebas en casos de neuroborreliosis. En Europa, la neuroborreliosis suele ser causada por Borrelia garinii y casi siempre implica pleocitosis linfocítica , es decir, las densidades de linfocitos (células que combaten infecciones) y proteínas en el líquido cefalorraquídeo (LCR) suelen aumentar hasta niveles característicamente anormales, mientras que el nivel de glucosa permanece normal. Además, el sistema inmunológico produce anticuerpos contra Lyme dentro del espacio intratecal, que contiene el LCR. Se requiere la demostración mediante punción lumbar y análisis del LCR de la pleocitosis y la producción de anticuerpos intratecal para el diagnóstico definitivo de neuroborreliosis en Europa (excepto en casos de neuropatía periférica asociada con acrodermatitis crónica atrófica , que generalmente es causada por Borrelia afzelii y confirmada por análisis de anticuerpos en sangre). En América del Norte, la neuroborreliosis es causada por Borrelia burgdorferi y puede no estar acompañada de los mismos signos de LCR; confirman un diagnóstico de neuroborreliosis del sistema nervioso central (SNC) si es positivo, pero no lo excluyen si es negativo. Las directrices estadounidenses consideran que el análisis del LCR es opcional cuando los síntomas parecen estar confinados al sistema nervioso periférico (SNP), por ejemplo, parálisis facial sin síntomas evidentes de meningitis. A diferencia de las pruebas de sangre y de anticuerpos intratecales, las pruebas de pleocitosis en LCR vuelven a la normalidad después de que finaliza la infección y, por lo tanto, pueden usarse como marcadores objetivos del éxito del tratamiento e informar las decisiones sobre si retirarse. En la infección que afecta al SNP, se pueden utilizar estudios de conducción nerviosa y electromiografía para monitorizar objetivamente la respuesta al tratamiento.
En la carditis de Lyme, los electrocardiogramas se utilizan para evidenciar anomalías en la conducción cardíaca, mientras que la ecocardiografía puede mostrar disfunción miocárdica . La biopsia y la confirmación de las células de Borrelia en el tejido miocárdico se pueden usar en casos específicos, pero generalmente no se realizan debido al riesgo del procedimiento.
También se han desarrollado pruebas de reacción en cadena de la polimerasa (PCR) para la enfermedad de Lyme para detectar el material genético ( ADN ) de la espiroqueta de la enfermedad de Lyme. El cultivo o PCR son los medios actuales para detectar la presencia del organismo, ya que los estudios serológicos solo evalúan anticuerpos de Borrelia . La PCR tiene la ventaja de ser mucho más rápida que el cultivo. Sin embargo, las pruebas de PCR son susceptibles de obtener resultados falsos positivos , por ejemplo, mediante la detección de restos de células muertas de Borrelia o la contaminación de la muestra. Incluso cuando se realiza correctamente, la PCR a menudo muestra resultados falsos negativos porque se pueden encontrar pocas células de Borrelia en la sangre y el líquido cefalorraquídeo (LCR) durante la infección. Por lo tanto, las pruebas de PCR se recomiendan solo en casos especiales, por ejemplo, el diagnóstico de artritis de Lyme, porque es una forma muy sensible de detectar el ADN de ospA en el líquido sinovial. Aunque la sensibilidad de la PCR en el LCR es baja, se puede considerar su uso cuando se sospecha que los resultados de la prueba de producción de anticuerpos intratecal son falsamente negativos, por ejemplo, en neuroborreliosis muy temprana (<6 semanas) o en personas inmunodeprimidas .
Existen varias otras formas de pruebas de laboratorio para la enfermedad de Lyme, algunas de las cuales no han sido validadas adecuadamente. Los antígenos OspA , vertidos por las bacterias Borrelia vivas en la orina, son una técnica prometedora que se está estudiando. Se está estudiando el uso de partículas de nanotrap para su detección y la OspA se ha relacionado con los síntomas activos de Lyme. Los títulos altos de anticuerpos de inmunoglobulina G (IgG) o inmunoglobulina M (IgM) contra los antígenos de Borrelia indican enfermedad, pero los títulos más bajos pueden ser engañosos, porque los anticuerpos IgM pueden permanecer después de la infección inicial y los anticuerpos IgG pueden permanecer durante años.
Los CDC no recomiendan las pruebas de antígeno en orina, las pruebas de PCR en orina, la tinción inmunofluorescente para las formas de B. burgdorferi con deficiencia de la pared celular y las pruebas de transformación de linfocitos.
Imagen
La neuroimagen es controvertida en cuanto a si proporciona patrones específicos exclusivos de la neuroborreliosis , pero puede ayudar en el diagnóstico diferencial y en la comprensión de la fisiopatología de la enfermedad. Aunque es controvertido, algunas pruebas muestran que ciertas pruebas de neuroimagen pueden proporcionar datos que son útiles en el diagnóstico de una persona. La resonancia magnética (MRI) y la tomografía computarizada por emisión de fotón único (SPECT) son dos de las pruebas que pueden identificar anomalías en el cerebro de una persona afectada por esta enfermedad. Los hallazgos de neuroimagen en una resonancia magnética incluyen lesiones en la sustancia blanca periventricular, así como ventrículos agrandados y atrofia cortical. Los hallazgos se consideran algo poco excepcionales porque se ha descubierto que las lesiones son reversibles después del tratamiento con antibióticos. Las imágenes producidas mediante SPECT muestran numerosas áreas en las que se suministra una cantidad insuficiente de sangre a la corteza y la sustancia blanca subcortical. Sin embargo, se sabe que las imágenes SPECT son inespecíficas porque muestran un patrón heterogéneo en las imágenes. Las anomalías observadas en las imágenes de SPECT son muy similares a las observadas en personas con vacuidades cerebrales y enfermedad de Creutzfeldt-Jakob , lo que las hace cuestionables.
Diagnóstico diferencial
Se ha informado que las clínicas comunitarias diagnostican erróneamente entre el 23 y el 28% de las erupciones por eritema migrans (EM) y el 83% de otras manifestaciones objetivas de la enfermedad de Lyme temprana. Las erupciones EM a menudo se diagnostican erróneamente como picaduras de araña , celulitis o herpes zóster . Muchos diagnósticos erróneos se atribuyen a la idea errónea generalizada de que las erupciones EM deberían verse como un ojo de buey. En realidad, las características distintivas clave de la erupción EM son la velocidad y el grado en que se expande, respectivamente hasta 2-3 cm / día y un diámetro de al menos 5 cm, y en el 50% de los casos más de 16 cm. La erupción se expande lejos de su centro, que puede o no tener un aspecto diferente o estar separado del resto de la erupción por un claro en forma de anillo. En comparación con las erupciones EM, las picaduras de arañas son más comunes en las extremidades, tienden a ser más dolorosas y pican o se inflaman, y algunas pueden causar necrosis (mancha de piel muerta de color azul oscuro que se hunde). La celulitis se desarrolla con mayor frecuencia alrededor de una herida o úlcera, rara vez es circular y es más probable que se hinche y se vuelva sensible. Las erupciones EM a menudo aparecen en sitios que son inusuales para la celulitis, como la axila, la ingle, el abdomen o la parte posterior de la rodilla. Al igual que Lyme, el herpes zóster a menudo comienza con dolor de cabeza, fiebre y fatiga, seguidos de dolor o entumecimiento. Sin embargo, a diferencia de Lyme, en el herpes zóster, estos síntomas suelen ir seguidos de la aparición de erupciones compuestas por múltiples ampollas pequeñas junto con un dermatoma nervioso , y el herpes zóster también puede confirmarse mediante pruebas rápidas de laboratorio.
La parálisis facial causada por la enfermedad de Lyme (LDFP) a menudo se diagnostica erróneamente como parálisis de Bell . Aunque la parálisis de Bell es el tipo más común de parálisis facial unilateral (aproximadamente el 70% de los casos), la LDFP puede representar aproximadamente el 25% de los casos de parálisis facial en áreas donde la enfermedad de Lyme es común. En comparación con LDFP, la parálisis de Bell afecta con mucha menos frecuencia a ambos lados de la cara. Aunque LDFP y la parálisis de Bell tienen síntomas similares y evolucionan de manera similar si no se tratan, el tratamiento con corticosteroides es beneficioso para la parálisis de Bell, mientras que es perjudicial para la LDFP. Se debe evaluar el historial reciente de exposición a un posible hábitat de garrapatas durante los meses más cálidos, erupción EM, síntomas de tipo viral como dolor de cabeza y fiebre y / o parálisis en ambos lados de la cara para determinar la probabilidad de LDFP; si es más que mínima, debe iniciarse una terapia empírica con antibióticos, sin corticosteroides, y reevaluarse al completar las pruebas de laboratorio para la enfermedad de Lyme.
A diferencia de la meningitis viral , la meningitis linfocítica de Lyme tiende a no causar fiebre, dura más y reaparece. La meningitis linfocítica también se caracteriza por posiblemente coexistir con erupción EM , parálisis facial u obstrucción de la visión parcial y tener un porcentaje mucho menor de leucocitos polimorfonucleares en el LCR .
La radiculopatía de Lyme que afecta a las extremidades a menudo se diagnostica erróneamente como una radiculopatía causada por la compresión de la raíz nerviosa, como la ciática . Aunque la mayoría de los casos de radiculopatía son compresivos y se resuelven con tratamiento conservador (p. Ej., Reposo) dentro de 4 a 6 semanas, las pautas para el manejo de la radiculopatía recomiendan evaluar primero los riesgos de otras posibles causas que, aunque menos frecuentes, requieren un diagnóstico y tratamiento inmediatos, incluidas infecciones como como Lyme y el herpes zóster. Un historial de actividades al aire libre en hábitats probables de garrapatas en los últimos 3 meses posiblemente seguidos de una erupción o síntomas similares a los virales, y dolor de cabeza actual, otros síntomas de meningitis linfocítica o parálisis facial llevarían a sospechar la enfermedad de Lyme y recomendarían pruebas serológicas y serológicas. pruebas de punción lumbar para confirmación.
La radiculopatía de Lyme que afecta el tronco puede diagnosticarse erróneamente como una miríada de otras afecciones, como diverticulitis y síndrome coronario agudo . El diagnóstico de la enfermedad de Lyme en etapa tardía a menudo se complica por una apariencia multifacética y síntomas inespecíficos, lo que llevó a un revisor a llamar a Lyme el nuevo "gran imitador". La enfermedad de Lyme puede diagnosticarse erróneamente como esclerosis múltiple , artritis reumatoide , fibromialgia , síndrome de fatiga crónica , lupus , enfermedad de Crohn , VIH u otras enfermedades autoinmunes y neurodegenerativas . Como todas las personas con infección en etapa avanzada tendrán una prueba de anticuerpos positiva, los análisis de sangre simples pueden excluir la enfermedad de Lyme como una posible causa de los síntomas de una persona.
Prevención
Las picaduras de garrapatas se pueden prevenir evitando o reduciendo el tiempo en hábitats probables de garrapatas y tomando precauciones al entrar y salir de uno.
La mayoría de las infecciones humanas de Lyme son causadas por picaduras de ninfa de Ixodes entre abril y septiembre. Las garrapatas prefieren lugares húmedos y sombreados en bosques , arbustos, pastos altos y hojarasca o montones de madera. Las densidades de garrapatas tienden a ser más altas en los bosques, seguidas de los bordes sin mantenimiento entre los bosques y el césped (aproximadamente la mitad de alto), las plantas ornamentales y la cubierta vegetal perenne (aproximadamente una cuarta parte) y el césped (aproximadamente 30 veces menos). Las larvas y ninfas de Ixodes tienden a ser abundantes también donde anidan los ratones, como muros de piedra y troncos de madera. Las larvas y ninfas de Ixodes esperan típicamente huéspedes potenciales ("búsqueda") en hojas o pastos cerca del suelo con las patas delanteras extendidas; cuando un huésped roza sus extremidades, la garrapata se aferra rápidamente y trepa al huésped en busca de un lugar en la piel para morder. En el noreste de los Estados Unidos, se estima que el 69% de las picaduras de garrapatas ocurren en residencias, el 11% en escuelas o campamentos, el 9% en parques o áreas recreativas, el 4% en el trabajo, el 3% durante la caza y el 4% en otras áreas. Las actividades asociadas con las picaduras de garrapatas alrededor de las residencias incluyen trabajo en el jardín, limpieza de matorrales, jardinería, jugar en el patio y dejar entrar a los perros o gatos que deambulan afuera en áreas boscosas o con césped. En los parques, las picaduras de garrapatas a menudo ocurren durante una excursión o un campamento. Caminar sobre un césped cortado o el centro de un sendero sin tocar la vegetación adyacente es menos riesgoso que gatear o sentarse sobre un tronco o una pared de piedra. No se debe permitir que las mascotas deambulen libremente en hábitats probables de garrapatas.
Como precaución, los CDC recomiendan remojar o rociar la ropa, los zapatos y el equipo de campamento, como tiendas de campaña, mochilas y sacos de dormir, con una solución de permetrina al 0.5% y colgarlos para que se sequen antes de usarlos. La permetrina es inodoro y seguro para los humanos, pero altamente tóxico para las garrapatas. Después de gatear sobre la tela tratada con permetrina durante tan solo 10 a 20 segundos, las ninfas de las garrapatas se irritan y se caen o mueren. Los zapatos y calcetines cerrados tratados con permetrina reducen en 74 veces el número de picaduras de ninfas que hacen el primer contacto con un zapato de una persona que también usa pantalones cortos tratados (debido a que las ninfas generalmente buscan cerca del suelo, este es un escenario de contacto típico). Se puede lograr una mejor protección metiendo pantalones tratados con permetrina dentro de los calcetines tratados y una camisa de manga larga tratada dentro de los pantalones para minimizar los espacios a través de los cuales una garrapata podría alcanzar la piel del usuario. La ropa de colores claros puede hacer que sea más fácil ver las garrapatas y quitarlas antes de que piquen. Se ha descubierto que los uniformes militares y para trabajadores al aire libre tratados con permetrina reducen el número de casos de mordeduras en un 80–95%. La protección con permetrina dura varias semanas de uso y lavados en artículos tratados por el cliente y hasta 70 lavados para artículos tratados en fábrica. La permetrina no debe usarse en piel humana, ropa interior o gatos.
La EPA recomienda varios repelentes de garrapatas para su uso en la piel expuesta, incluidos DEET , picaridina , IR3535 (un derivado del aminoácido beta-alanina), aceite de eucalipto de limón (OLE, un compuesto natural) y el ingrediente activo de OLE para-mentanodiol ( PMD) . A diferencia de la permetrina, los repelentes repelen pero no matan a las garrapatas, protegen solo durante varias horas después de la aplicación y pueden eliminarse con el sudor o el agua. El repelente más popular es el DEET en EE. UU. Y la picaridina en Europa. A diferencia del DEET, la picaridina es inodoro y es menos probable que irrite la piel o dañe la tela o los plásticos. Los repelentes con mayor concentración pueden durar más tiempo pero no son más efectivos; contra las garrapatas, la picaridina al 20% puede funcionar durante 8 horas en comparación con el 55-98,11% de DEET durante 5-6 horas o el 30-40% de OLE durante 6 horas. Los repelentes no deben usarse debajo de la ropa, en ojos, boca, heridas o cortes, o en bebés menores de 2 meses (3 años para OLE o PMD). Si se usa protector solar , se debe aplicar repelente encima. Los repelentes no deben rociarse directamente en la cara, sino que deben rociarse en una mano y luego frotarse en la cara.
Después de entrar al interior, se debe revisar la ropa, el equipo y las mascotas para detectar garrapatas. La ropa se puede poner en una secadora caliente durante 10 minutos para matar las garrapatas (no basta con lavarla o en la secadora caliente). Ducharse lo antes posible, buscar garrapatas en todo el cuerpo y eliminarlas reduce el riesgo de infección. Las ninfas de garrapatas no alimentadas son del tamaño de una semilla de amapola, pero uno o dos días después de morder y adherirse a una persona, parecen una pequeña ampolla de sangre . Las siguientes áreas deben revisarse con especial atención: axilas, entre piernas, parte posterior de la rodilla, ombligo, tronco y en las orejas, el cuello y el cabello de los niños.
Eliminación de garrapatas
Las garrapatas adheridas deben eliminarse de inmediato. El riesgo de infección aumenta con el tiempo de inserción, pero en Norteamérica el riesgo de enfermedad de Lyme es pequeño si la garrapata se quita dentro de las 36 horas. Los CDC recomiendan insertar una pinza de punta fina entre la piel y la garrapata, sujetarla con mucha firmeza y tirar de la pinza cerrada directamente lejos de la piel sin retorcer, sacudir, apretar o aplastar la garrapata. Después de quitar la garrapata, si es posible, debe quitarse cualquier parte de la garrapata que quede en la piel con una pinza limpia. Luego, la herida y las manos deben limpiarse con alcohol o agua y jabón. La garrapata puede desecharse colocándola en un recipiente con alcohol, una bolsa sellada, cinta adhesiva o tirándola por el inodoro. La persona mordida debe anotar dónde y cuándo ocurrió la picadura para que pueda informar a un médico si la persona presenta un sarpullido o síntomas similares a los de la gripe en las siguientes semanas. Los CDC recomiendan no usar los dedos, esmalte de uñas, vaselina o calor en la garrapata para tratar de quitarla.
En Australia, donde prevalece la garrapata de parálisis australiana , la Sociedad Australasia de Inmunología Clínica y Alergia recomienda no usar pinzas para quitar las garrapatas, porque si la persona es alérgica, podría producirse anafilaxia . En cambio, se debe rociar un producto sobre la garrapata para que se congele y luego se caiga. Un médico usaría nitrógeno líquido, pero en su lugar se pueden usar productos disponibles de los químicos para congelar las verrugas. Otro método originario de Australia consiste en utilizar unos 20 cm de hilo dental o hilo de pescar para atar lentamente un nudo entre la piel y la garrapata y luego separarlo de la piel.
Antibióticos preventivos
El riesgo de transmisión infecciosa aumenta con la duración del apego de la garrapata. Requiere entre 36 y 48 horas de adhesión para la bacteria que hace que Lyme viaje desde el interior de la garrapata hasta su saliva. Si una garrapata de venado que es lo suficientemente probable que sea portadora de Borrelia se encuentra adherida a una persona y se retira, y si la garrapata ha estado adherida durante 36 horas o está ingurgitada, una sola dosis de doxiciclina administrada dentro de las 72 horas posteriores a la extracción puede reducir la riesgo de enfermedad de Lyme. Por lo general, no se recomienda para todas las personas mordidas, ya que el desarrollo de la infección es poco común: unas 50 personas mordidas tendrían que ser tratadas de esta manera para prevenir un caso de eritema migratorio (es decir, la erupción típica que se encuentra en aproximadamente el 70-80% de las personas infectadas). ).
Paisajismo de jardín
Varias prácticas de jardinería pueden reducir el riesgo de picaduras de garrapatas en patios residenciales. El césped debe mantenerse cortado, la hojarasca y las malas hierbas deben eliminarse y debe evitarse el uso de cubiertas vegetales . Los bosques , arbustos, paredes de piedra y pilas de madera deben estar separados del césped por una barrera de roca o astillas de madera de 3 pies de ancho. Sin vegetación en la barrera, las garrapatas tenderán a no cruzarla; También se pueden rociar acaricidas para matar las garrapatas. Una zona a prueba de garrapatas expuesta al sol al menos a 9 pies de la barrera debe concentrar la actividad humana en el patio, incluidos los patios, áreas de juego y jardinería. Se pueden utilizar materiales como tarimas de madera, hormigón, ladrillos, grava o astillas de madera en el suelo debajo de los patios y áreas de juego para disuadir a las garrapatas allí. Se puede agregar una cerca de 8 pies de altura para mantener a los venados alejados de la zona segura contra las garrapatas.
Exposición ocupacional
Los trabajadores al aire libre corren el riesgo de contraer la enfermedad de Lyme si trabajan en lugares con garrapatas infectadas. Esto incluye construcción, paisajismo, silvicultura, limpieza de matorrales, agrimensura, agricultura, trabajos en ferrocarriles, trabajos en campos petroleros, trabajos en líneas de servicios públicos, manejo de parques o vida silvestre. Los trabajadores estadounidenses en los estados del noreste y centro-norte tienen mayor riesgo de exposición a garrapatas infectadas. Las garrapatas también pueden transmitir otras enfermedades transmitidas por garrapatas a los trabajadores en estas y otras regiones del país. Es probable que los lugares de trabajo con bosques, arbustos, hierba alta o hojarasca tengan más garrapatas. Los trabajadores al aire libre deben tener más cuidado de protegerse a fines de la primavera y el verano, cuando las garrapatas jóvenes están más activas.
Animales anfitriones
La enfermedad de Lyme y otras enfermedades transmitidas por garrapatas de los ciervos a veces se pueden reducir reduciendo en gran medida la población de ciervos de la que dependen las garrapatas adultas para alimentarse y reproducirse. Los casos de enfermedad de Lyme disminuyeron después de la erradicación de ciervos en una isla, Monhegan, Maine , y después del control de ciervos en Mumford Cove, Connecticut. Vale la pena señalar que la eliminación de los ciervos puede provocar un aumento temporal de la densidad de garrapatas.
Por ejemplo, en los EE. UU., La reducción de la población de ciervos a niveles de 8 a 10 por milla cuadrada (de los niveles actuales de 60 o más ciervos por milla cuadrada en las áreas del país con las tasas más altas de enfermedad de Lyme) puede reducir el número de garrapatas. y reducir la propagación de Lyme y otras enfermedades transmitidas por garrapatas. Sin embargo, una reducción tan drástica puede ser muy difícil de implementar en muchas áreas, y densidades bajas a moderadas de venados u otros grandes mamíferos hospedadores pueden continuar alimentando suficientes garrapatas adultas para mantener las densidades larvarias en niveles altos. El control veterinario de rutina de las garrapatas de los animales domésticos , incluido el ganado, mediante el uso de acaricidas puede contribuir a reducir la exposición de los seres humanos a las garrapatas.
En Europa, los reservorios conocidos de Borrelia burgdorferi eran 9 pequeños mamíferos, 7 mamíferos medianos y 16 especies de aves (incluidos paseriformes, aves marinas y faisanes). Estos animales parecen transmitir espiroquetas a las garrapatas y, por tanto, participan en la circulación natural de B. burgdorferi en Europa. El ratón doméstico también es sospechoso, así como otras especies de pequeños roedores, especialmente en Europa del Este y Rusia. "La especie reservorio que contiene la mayoría de patógenos es el corzo europeo Capreolus capreolus ;" no parece servir como reservorio importante de B. burgdorferi ", pensaron Jaenson & al. (1992) (hospedante incompetente de B. burgdorferi y TBE virus) pero es importante para la alimentación de las garrapatas, como ciervo y jabalí ( Sus scrofa ), en las que se identificaron una especie de Rickettsia y tres de Borrelia ", con alto riesgo de coinfección en corzos. Sin embargo, en la década de 2000, en el corzo de Europa " se identificaron dos especies de Rickettsia y dos especies de Borrelia ".
Vacunación
SmithKline Beecham desarrolló una vacuna recombinante contra la enfermedad de Lyme, basada en la proteína A de la superficie externa (ospA) de B. burgdorferi . En ensayos clínicos en los que participaron más de 10.000 personas, se descubrió que la vacuna, denominada LYMErix, confiere inmunidad protectora a Borrelia en el 76% de los adultos y el 100% de los niños, con efectos adversos sólo leves o moderados y transitorios . LYMErix fue aprobado sobre la base de estos ensayos por la Administración de Alimentos y Medicamentos (FDA) el 21 de diciembre de 1998.
Después de la aprobación de la vacuna , su entrada en la práctica clínica fue lenta por una variedad de razones, incluido su costo, que a menudo no era reembolsado por las compañías de seguros. Posteriormente, cientos de receptores de la vacuna informaron que habían desarrollado efectos secundarios autoinmunitarios y de otro tipo. Con el apoyo de algunos grupos de defensa, se presentaron varias demandas colectivas contra GlaxoSmithKline , alegando que la vacuna había causado estos problemas de salud. Estas afirmaciones fueron investigadas por la FDA y los Centros para el Control de Enfermedades, que no encontraron conexión entre la vacuna y las quejas autoinmunes.
A pesar de la falta de pruebas de que las quejas fueron causadas por la vacuna, las ventas se desplomaron y GlaxoSmithKline retiró LYMErix del mercado estadounidense en febrero de 2002, en un contexto de cobertura mediática negativa y temores de los efectos secundarios de la vacuna. El destino de LYMErix se describió en la literatura médica como una "advertencia"; un editorial de Nature citó la retirada de LYMErix como un caso en el que "temores públicos infundados ejercen presiones sobre los desarrolladores de vacunas que van más allá de las consideraciones de seguridad razonables". El desarrollador original de la vacuna OspA en el Instituto Max Planck dijo a Nature : "Esto solo muestra lo irracional que puede ser el mundo ... No había ninguna justificación científica para que se retirara la primera vacuna OspA LYMErix".
Se han formulado y aprobado vacunas para la prevención de la enfermedad de Lyme en perros. Actualmente, se encuentran disponibles tres vacunas contra la enfermedad de Lyme. LymeVax, formulado por Fort Dodge Laboratories, contiene espiroquetas muertas intactas que exponen al huésped al organismo. Galaxy Lyme, la vacuna de Intervet -Schering-Plough , se dirige a las proteínas OspC y OspA . Los anticuerpos de OspC matan a cualquiera de las bacterias que no hayan sido eliminadas por los anticuerpos de OspA. Canine Recombinant Lyme, formulado por Merial , genera anticuerpos contra la proteína OspA, por lo que una garrapata que se alimenta de un perro vacunado extrae sangre llena de anticuerpos anti-OspA, que matan las espiroquetas en el intestino de la garrapata antes de que se transmitan al perro.
En 2017, la Administración de Alimentos y Medicamentos de EE. UU. Concedió la designación de vía rápida a una vacuna candidata a vacuna basada en subunidades de proteína hexavalente (OspA), VLA15, desarrollada por Valneva, lo que permitirá realizar más estudios.
Tratamiento
Los antibióticos son el tratamiento principal. El enfoque específico para su uso depende del individuo afectado y la etapa de la enfermedad. Para la mayoría de las personas con infección localizada temprana, se recomienda ampliamente la administración oral de doxiciclina como primera opción, ya que es eficaz no solo contra la bacteria Borrelia, sino también contra una variedad de otras enfermedades transmitidas por garrapatas. Las personas que toman doxiciclina deben evitar la exposición al sol debido al mayor riesgo de quemaduras solares . La doxiciclina está contraindicada en niños menores de ocho años y en mujeres embarazadas o en período de lactancia; las alternativas a la doxiciclina son amoxicilina , cefuroxima axetilo y azitromicina . La azitromicina se recomienda solo en caso de intolerancia a los otros antibióticos. El tratamiento estándar para la celulitis , la cefalexina , no es útil para la enfermedad de Lyme. Cuando no está claro si una erupción es causada por Lyme o celulitis, la IDSA recomienda el tratamiento con cefuroxima o amoxicilina / ácido clavulánico , ya que son efectivos contra ambas infecciones. Los individuos con infección de Lyme diseminada temprana o tardía pueden tener enfermedad cardíaca sintomática, artritis de Lyme o síntomas neurológicos como parálisis facial , radiculopatía , meningitis o neuropatía periférica . Se recomienda la administración intravenosa de ceftriaxona como primera opción en estos casos; La cefotaxima y la doxiciclina están disponibles como alternativas.
Los regímenes de tratamiento para la enfermedad de Lyme oscilan entre 14 días en la enfermedad localizada temprana, 14 a 21 días en la enfermedad diseminada temprana y 14 a 28 días en la enfermedad diseminada tardía. Las complicaciones neurológicas de la enfermedad de Lyme pueden tratarse con doxiciclina, ya que se puede tomar por vía oral y tiene un costo menor, aunque en América del Norte la evidencia de eficacia es solo indirecta. En caso de falla, las guías recomiendan el retratamiento con ceftriaxona inyectable . Varios meses después del tratamiento para la artritis de Lyme, si la inflamación de las articulaciones persiste o regresa, se puede considerar una segunda ronda de antibióticos; Se prefieren los antibióticos intravenosos para el retratamiento en caso de mala respuesta a los antibióticos orales. Fuera de eso, no se recomienda un régimen prolongado de antibióticos que dure más de 28 días ya que no hay evidencia que demuestre que sea efectivo. Los niveles de anticuerpos IgM e IgG pueden estar elevados durante años incluso después de un tratamiento exitoso con antibióticos. Como los niveles de anticuerpos no son indicativos del éxito del tratamiento, no se recomienda realizar pruebas para detectarlos.
La parálisis facial puede resolverse sin tratamiento; sin embargo, se recomienda el tratamiento con antibióticos para detener otras complicaciones de Lyme. No se recomiendan los corticosteroides cuando la parálisis facial es causada por la enfermedad de Lyme. En aquellos con parálisis facial, se recomienda el uso frecuente de lágrimas artificiales mientras están despiertos, junto con ungüento y un parche o tapar el ojo para cerrarlo cuando duerme.
Aproximadamente un tercio de las personas con carditis de Lyme necesitan un marcapasos temporal hasta que se resuelva la anomalía de la conducción cardíaca y el 21% debe ser hospitalizado. La carditis de Lyme no debe tratarse con corticosteroides.
Las personas con artritis de Lyme deben limitar su nivel de actividad física para evitar dañar las articulaciones afectadas y, en caso de cojera, deben usar muletas. El dolor asociado con la enfermedad de Lyme puede tratarse con medicamentos antiinflamatorios no esteroides (AINE). No se recomiendan las inyecciones de corticosteroides en las articulaciones para la artritis de Lyme que se está tratando con antibióticos. Se dice que las personas con artritis de Lyme tratadas con antibióticos intravenosos o dos meses de antibióticos orales que continúan con inflamación de las articulaciones dos meses después del tratamiento y tienen una prueba de PCR negativa para ADN de Borrelia en el líquido sinovial tienen artritis de Lyme resistente a los antibióticos; esto es más común después de la infección por ciertas cepas de Borrelia en personas con ciertas características genéticas e inmunológicas. La artritis de Lyme resistente a los antibióticos puede tratarse sintomáticamente con AINE, fármacos antirreumáticos modificadores de la enfermedad (FARME) o sinovectomía artroscópica . Se recomienda fisioterapia para adultos después de la resolución de la artritis de Lyme.
Se debe advertir a las personas que reciben tratamiento que es posible una reinfección y cómo prevenirla .
Pronóstico
El primer signo típico de la enfermedad de Lyme, la erupción de eritema migratorio (EM), se resuelve en varias semanas incluso sin tratamiento. Sin embargo, en las personas que no reciben tratamiento, la infección a menudo se disemina al sistema nervioso, el corazón o las articulaciones, posiblemente causando daño permanente a los tejidos corporales.
Las personas que reciben el tratamiento antibiótico recomendado varios días después de la aparición de una erupción EM inicial tienen las mejores perspectivas. La recuperación puede no ser total o inmediata. El porcentaje de personas que logran una recuperación completa en los Estados Unidos aumenta de aproximadamente 64 a 71% al final del tratamiento para la erupción EM a aproximadamente 84 a 90% después de 30 meses; en Europa se registran porcentajes más elevados. El fracaso del tratamiento, es decir, la persistencia del origen o la aparición de nuevos signos de la enfermedad, ocurre solo en unas pocas personas. Las personas restantes se consideran curadas, pero continúan experimentando síntomas subjetivos, por ejemplo, dolores articulares o musculares o fatiga . Estos síntomas suelen ser leves y no incapacitantes.
Las personas tratadas solo después de las manifestaciones del sistema nervioso de la enfermedad pueden terminar con déficits neurológicos objetivos, además de síntomas subjetivos. En Europa, un promedio de 32 a 33 meses después de los síntomas iniciales de Lyme en personas tratadas principalmente con 200 mg de doxiciclina durante 14 a 21 días, el porcentaje de personas con síntomas persistentes fue mucho mayor entre los diagnosticados con neuroborreliosis (50%) que entre aquellos con solo una erupción EM (16%). En otro estudio europeo, 5 años después del tratamiento para la neuroborreliosis, los síntomas persistentes fueron menos comunes entre los niños (15%) que entre los adultos (30%), y en estos últimos fue menos común entre los tratados dentro de los 30 días del primer síntoma (16% ) que entre los tratados más tarde (39%); entre aquellos con síntomas persistentes, el 54% tenía restringidas sus actividades diarias y el 19% estaba de baja por enfermedad o incapacitado.
Algunos datos sugieren que alrededor del 90% de las parálisis faciales de Lyme tratadas con antibióticos se recuperan por completo una mediana de 24 días después de aparecer y la mayoría del resto se recupera con solo una anomalía leve. Sin embargo, en Europa, el 41% de las personas tratadas por parálisis facial tenían otros síntomas persistentes en el seguimiento hasta 6 meses después, incluido el 28% con entumecimiento o sensación alterada y el 14% con fatiga o problemas de concentración . Las parálisis en ambos lados de la cara se asocian con un tiempo de recuperación peor y más prolongado. Los datos históricos sugieren que las personas con parálisis faciales no tratadas se recuperan casi al mismo ritmo, pero el 88% posteriormente tiene artritis de Lyme. Otra investigación muestra que la sincinesia (movimiento involuntario de un músculo facial cuando otro se mueve voluntariamente) puede volverse evidente solo 6-12 meses después de que la parálisis facial parece resolverse, ya que los nervios dañados vuelven a crecer ya veces se conectan a músculos incorrectos. La sinquinesis está asociada con el uso de corticosteroides . En el seguimiento a más largo plazo, del 16 al 23% de las parálisis faciales de Lyme no se recuperan por completo.
En Europa, alrededor de una cuarta parte de las personas con síndrome de Bannwarth ( radiculopatía de Lyme y meningitis linfocítica ) tratadas con ceftriaxona intravenosa durante 14 días, un promedio de 30 días después de los primeros síntomas, tuvieron que volver a tratarse 3 a 6 meses después debido a una respuesta clínica insatisfactoria o un objetivo continuo. marcadores de infección en líquido cefalorraquídeo ; después de 12 meses, el 64% se recuperó por completo, el 31% tenía síntomas leves o infrecuentes no discapacitantes que no requerían el uso regular de analgésicos, y el 5% tenía síntomas que eran discapacitantes o requerían un uso sustancial de analgésicos. Los síntomas persistentes no discapacitantes más comunes fueron dolor de cabeza, fatiga , alteración de la sensibilidad , dolores articulares , alteraciones de la memoria , malestar , dolor radicular , alteraciones del sueño , dolores musculares y alteraciones de la concentración . Los síntomas incapacitantes persistentes incluyeron parálisis facial y otros movimientos alterados .
La recuperación de la neuroborreliosis tardía tiende a ser más prolongada y menos completa que la de la neuroborreliosis temprana, probablemente debido a un daño neurológico irreversible.
Aproximadamente la mitad de las personas con carditis de Lyme progresan hasta un bloqueo cardíaco completo , pero generalmente se resuelve en una semana. Otras anomalías de la conducción cardíaca de Lyme se resuelven típicamente en 6 semanas. Aproximadamente el 94% de las personas se recuperan por completo, pero el 5% necesita un marcapasos permanente y el 1% termina con un bloqueo cardíaco persistente (el porcentaje real puede ser mayor debido a casos no reconocidos). Las complicaciones del miocardio de Lyme suelen ser leves y autolimitadas. Sin embargo, en algunos casos, la carditis de Lyme puede ser fatal.
Los tratamientos con antibióticos recomendados son efectivos en aproximadamente el 90% de los casos de artritis de Lyme, aunque la inflamación puede tardar varios meses en resolverse y a menudo es necesaria una segunda ronda de antibióticos. La artritis de Lyme resistente a los antibióticos también se resuelve con el tiempo, por lo general en 9 a 14 meses (rango de 4 meses a 4 años); Los DMARD o la sinovectomía pueden acelerar la recuperación.
La reinfección no es infrecuente. En un estudio de EE. UU., Del 6 al 11% de las personas tratadas por una erupción EM tuvieron otra erupción EM dentro de los 30 meses. La segunda erupción generalmente se debe a una infección por una cepa de Borrelia diferente .
Se dice que las personas que tienen síntomas subjetivos inespecíficos, como fatiga, dolores articulares y musculares, o dificultades cognitivas durante más de seis meses después del tratamiento recomendado para la enfermedad de Lyme, tienen síndrome de la enfermedad de Lyme postratamiento (PTLDS, por sus siglas en inglés). A partir de 2016, se desconocía la razón de los síntomas persistentes; la afección generalmente se trata de manera similar a la fibromialgia o al síndrome de fatiga crónica .
Epidemiología
La enfermedad de Lyme ocurre con regularidad en las regiones templadas del hemisferio norte .
África
En el norte de África, se ha identificado B. burgdorferi sensu lato en Marruecos , Argelia , Egipto y Túnez .
Actualmente se desconoce la enfermedad de Lyme en África subsahariana, pero la evidencia indica que puede ocurrir en humanos en esta región. La abundancia de huéspedes y garrapatas vectores favorecería el establecimiento de la infección de Lyme en África. En África oriental, se han notificado dos casos de enfermedad de Lyme en Kenia .
Asia
Las garrapatas infestadas por B. burgdorferi sensu lato se encuentran con mayor frecuencia en Japón, así como en el noroeste de China, Nepal , Tailandia y el extremo oriental de Rusia. Borrelia también se ha aislado en Mongolia .
Europa
En Europa, la enfermedad de Lyme es causada por la infección con una o más genoespecies europeas patógenas de la espiroqueta B. burgdorferi sensu lato , transmitida principalmente por la garrapata Ixodes ricinus . Los casos de garrapatas infectadas por B. burgdorferi sensu lato se encuentran predominantemente en Europa central, particularmente en Eslovenia y Austria , pero se han aislado en casi todos los países del continente. El número de casos en el sur de Europa, como Italia y Portugal, es mucho menor. Los casos diagnosticados en algunos países occidentales, como Islandia, están aumentando.
Reino Unido
En el Reino Unido, el número de casos confirmados por laboratorio de la enfermedad de Lyme ha aumentado constantemente desde que se introdujo la notificación voluntaria en 1986, cuando se registraron 68 casos en el Reino Unido y la República de Irlanda combinados. En el Reino Unido hubo 23 casos confirmados en 1988 y 19 en 1990, pero 973 en 2009 y 953 en 2010. Las cifras provisionales para los primeros 3 trimestres de 2011 muestran un aumento del 26% con respecto al mismo período de 2010.
Sin embargo, se cree que el número real de casos es significativamente mayor que el sugerido por las cifras anteriores, y la Agencia de Protección de la Salud del Reino Unido estima que hay entre 2.000 y 3.000 casos por año (con un promedio de alrededor del 15% de los casos). infecciones adquiridas en el extranjero), mientras que el Dr. Darrel Ho-Yen, Director del Laboratorio de Referencia de Toxoplasma de Escocia y del Servicio Nacional de Pruebas de Enfermedad de Lyme, cree que el número de casos confirmados debe multiplicarse por 10 "para tener en cuenta los casos diagnosticados erróneamente, las pruebas dan falsas resultados, pacientes que no fueron evaluados, personas que están infectadas pero que no muestran síntomas, fallas en la notificación e individuos infectados que no consultan a un médico ".
A pesar de que la enfermedad de Lyme (infección por Borrelia burgdorferi) es una enfermedad de declaración obligatoria en Escocia desde enero de 1990 y, por lo tanto, debe notificarse sobre la base de la sospecha clínica, se cree que muchos médicos de cabecera desconocen el requisito. Los informes obligatorios, limitados únicamente a los resultados de las pruebas de laboratorio, se introdujeron en todo el Reino Unido en octubre de 2010, de conformidad con las Regulaciones (Notificación) de Protección de la Salud de 2010.
Aunque hay un mayor número de casos de enfermedad de Lyme en New Forest , Salisbury Plain , Exmoor , South Downs , partes de Wiltshire y Berkshire , Thetford Forest y la costa oeste y las islas de Escocia, las garrapatas infectadas están muy extendidas e incluso pueden ser encontrado en los parques de Londres. Un informe de 1989 encontró que el 25% de los trabajadores forestales en New Forest eran seropositivos , al igual que entre el 2% y el 4-5% de la población local general del área.
Las pruebas en perros de compañía realizadas en todo el país en 2009 indicaron que alrededor del 2,5% de las garrapatas en el Reino Unido pueden estar infectadas, considerablemente más de lo que se pensaba anteriormente. Se cree que el calentamiento global puede conducir a un aumento de la actividad de las garrapatas en el futuro, así como a un aumento en la cantidad de tiempo que las personas pasan en los parques públicos, aumentando así el riesgo de infección.
Norteamérica
Muchos estudios en América del Norte han examinado los correlatos ecológicos y ambientales del número de personas afectadas por la enfermedad de Lyme. Un estudio de 2005 que utilizó modelos de idoneidad climática de I. scapularis proyectó que el cambio climático causaría un aumento general del 213% en el hábitat adecuado para vectores para el año 2080, con expansiones hacia el norte en Canadá, mayor idoneidad en el centro de EE. UU. Y disminución de hábitats y vectores adecuados. retracción en el sur de EE. UU. Una revisión de estudios publicados en 2008 concluyó que la presencia de bosques o áreas boscosas era la única variable que elevaba constantemente el riesgo de enfermedad de Lyme, mientras que otras variables ambientales mostraron poca o ninguna concordancia entre los estudios. Los autores argumentaron que los factores que influyen en la densidad de garrapatas y el riesgo humano entre sitios aún no se comprenden bien, y que los estudios futuros deben realizarse durante períodos de tiempo más prolongados, estandarizarse más en todas las regiones e incorporar el conocimiento existente de la ecología regional de la enfermedad de Lyme .
Canadá
Debido al cambio climático, la variedad de garrapatas capaces de transmitir la enfermedad de Lyme se ha expandido desde un área limitada de Ontario para incluir áreas del sur de Quebec, Manitoba, norte de Ontario, sur de New Brunswick, suroeste de Nueva Escocia y partes limitadas de Saskatchewan y Alberta, como así como Columbia Británica. Se han notificado casos tan al este como la isla de Terranova. Una predicción basada en modelos de Leighton et al. (2012) sugiere que el rango de la garrapata I. scapularis se expandirá en Canadá en 46 km / año durante la próxima década, con el calentamiento de las temperaturas como el principal impulsor del aumento de la velocidad de propagación.
México
Un estudio de 2007 sugiere que las infecciones por Borrelia burgdorferi son endémicas en México, de cuatro casos reportados entre 1999 y 2000.
Estados Unidos
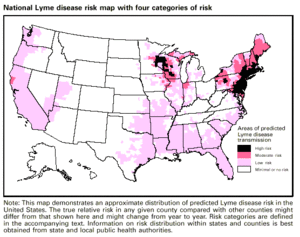
Cada año, se informan a los CDC aproximadamente 30,000 casos nuevos; sin embargo, es probable que este número esté subestimado. El CDC está realizando actualmente una investigación sobre la evaluación y el diagnóstico de la enfermedad y los resultados preliminares sugieren que el número de nuevos casos ronda los 300.000.
La enfermedad de Lyme es la enfermedad transmitida por garrapatas más común en América del Norte y Europa, y una de las enfermedades infecciosas de más rápido crecimiento en los Estados Unidos. De los casos notificados a los CDC de los Estados Unidos, la proporción de infección por la enfermedad de Lyme es de 7,9 casos por cada 100.000 personas. En los diez estados donde la enfermedad de Lyme es más común, el promedio fue de 31,6 casos por cada 100.000 personas para el año 2005.
Aunque la enfermedad de Lyme se ha informado en todos los estados, alrededor del 99% de todos los casos notificados se limitan a solo cinco áreas geográficas (Nueva Inglaterra, Atlántico Medio, Centro Este-Norte, Atlántico Sur y Centro Norte-Oeste). Las nuevas pautas de definición de casos de CDC Lyme de 2011 se utilizan para determinar los casos confirmados de vigilancia de los CDC.
A partir de enero de 2008, los CDC otorgan el mismo peso a la evidencia de laboratorio 1 de un cultivo positivo para B. burgdorferi ; 2) prueba de dos niveles ( detección de ELISA y confirmación de transferencia de Western ); o 3 ) Western blot de IgG de un solo nivel (infección antigua). Anteriormente, los CDC solo incluían evidencia de laboratorio basada en (1) y (2) en su definición de caso de vigilancia. La definición de caso ahora incluye el uso de Western blot sin una prueba previa de ELISA.
El número de casos notificados de la enfermedad ha ido en aumento, al igual que las regiones endémicas de América del Norte. Por ejemplo, anteriormente se pensaba que B. burgdorferi sensu lato se veía obstaculizada en su capacidad para mantenerse en un ciclo enzoótico en California, porque se suponía que la gran población de lagartos diluiría el número de personas afectadas por B. burgdorferi en las poblaciones locales de garrapatas. ; desde entonces, esto se ha puesto en duda, ya que algunas pruebas han sugerido que los lagartos pueden infectarse.
A excepción de un estudio en Europa, muchos de los datos que implican a las lagartijas se basan en la detección del ADN de la espiroqueta y no han demostrado que las lagartijas puedan infectar a las garrapatas que se alimentan de ellas. Como algunos experimentos sugieren que los lagartos son refractarios a la infección por Borrelia , parece probable que su participación en el ciclo enzoótico sea más compleja y específica de la especie.
Mientras que B. burgdorferi se asocia más con garrapatas hospedadas por venado cola blanca y ratones patas blancas , Borrelia afzelii se detecta con mayor frecuencia en garrapatas vectores que se alimentan de roedores, y Borrelia garinii y Borrelia valaisiana parecen estar asociadas con aves. Tanto los roedores como las aves son reservorios competentes de B. burgdorferi sensu stricto . La resistencia de una genoespecie de espiroquetas de la enfermedad de Lyme a las actividades bacteriolíticas de la vía alternativa del complemento de varias especies hospedadoras puede determinar su asociación con el hospedador reservorio.
Pueden existir varias condiciones similares pero aparentemente distintas, causadas por varias especies o subespecies de Borrelia en América del Norte. Una afección regionalmente restringida que puede estar relacionada con la infección por Borrelia es la erupción cutánea asociada a garrapatas del sur (STARI), también conocida como enfermedad de Masters. Amblyomma americanum , conocida comúnmente como garrapata estrella solitaria, es reconocida como el vector principal de STARI. En algunas partes de la distribución geográfica de STARI, la enfermedad de Lyme es bastante rara (p. Ej., Arkansas), por lo que las personas en estas regiones que experimentan síntomas similares a los de Lyme, especialmente si siguen una picadura de una garrapata estrella solitaria, deben considerar STARI como un posibilidad. Por lo general, es una afección más leve que la de Lyme y generalmente responde bien al tratamiento con antibióticos.
En los últimos años ha habido de 5 a 10 casos al año de una enfermedad similar a la de Lyme en Montana. Ocurre principalmente en los bolsillos a lo largo del río Yellowstone en el centro de Montana. Las personas han desarrollado una erupción en forma de ojo de buey rojo alrededor de la picadura de una garrapata seguida de semanas de fatiga y fiebre.
Los efectos de la enfermedad de Lyme son comparables entre hombres y mujeres. Una amplia gama de grupos de edad se ve afectada, aunque el número de casos es mayor entre los jóvenes de 10 a 19 años. Por razones desconocidas, la enfermedad de Lyme es siete veces más común entre los asiáticos.
Sudamerica
En América del Sur, el reconocimiento y la aparición de enfermedades transmitidas por garrapatas está aumentando. En Brasil, se identificó una enfermedad similar a Lyme conocida como síndrome de Baggio-Yoshinari , causada por microorganismos que no pertenecen al complejo B. burgdorferi sensu lato y transmitida por garrapatas de los géneros Amblyomma y Rhipicephalus . El primer caso notificado de BYS en Brasil se produjo en 1992 en Cotia , São Paulo.
Historia
La historia evolutiva de la genética de Borrelia burgdorferi ha sido objeto de estudios recientes. Un estudio ha encontrado que antes de la reforestación que acompañó al abandono de granjas poscoloniales en Nueva Inglaterra y la migración masiva hacia el medio oeste que ocurrió a principios del siglo XIX, la enfermedad de Lyme estuvo presente durante miles de años en América y se había extendido a lo largo de con sus hospedadores de garrapatas desde el noreste hasta el medio oeste.
John Josselyn, quien visitó Nueva Inglaterra en 1638 y nuevamente entre 1663 y 1670, escribió que "hay un número infinito de garrapatas que cuelgan de los arbustos en verano que se adhieren a la ropa del hombre y se deslizan en sus pantalones, comiéndose en poco tiempo en el carne de hombre. He visto las medias de los que han pasado por el bosque cubiertas con ellas ".
Esto también es confirmado por los escritos de Peter Kalm , un botánico sueco que fue enviado a América por Linneo , y quien encontró que los bosques de Nueva York "abundan" con garrapatas cuando lo visitó en 1749. Cuando el viaje de Kalm fue recordado 100 años después, los bosques habían desaparecido y la bacteria de Lyme probablemente se había aislado en unos pocos focos a lo largo de la costa noreste, Wisconsin y Minnesota.
Quizás la primera descripción detallada de lo que ahora se conoce como enfermedad de Lyme apareció en los escritos de John Walker después de una visita a la isla de Jura (Deer Island) en la costa oeste de Escocia en 1764. Da una buena descripción de ambos síntomas. de la enfermedad de Lyme (con "dolor intenso [en] el interior de las extremidades") y del propio vector de la garrapata, que describe como un "gusano" con un cuerpo "de color rojizo y de forma comprimida con una fila de pies a cada lado "que" penetra la piel ". Mucha gente de esta zona de Gran Bretaña emigró a Norteamérica entre 1717 y finales del siglo XVIII.
El examen de las muestras conservadas del museo ha encontrado ADN de Borrelia en una garrapata Ixodes ricinus infectada de Alemania que data de 1884, y de un ratón infectado de Cape Cod que murió en 1894. La autopsia de 2010 de Ötzi the Iceman , un animal de 5.300 años momia vieja , reveló la presencia de la secuencia de ADN de Borrelia burgdorferi convirtiéndolo en el primer ser humano conocido con la enfermedad de Lyme.
Los primeros estudios europeos de lo que ahora se conoce como enfermedad de Lyme describieron sus manifestaciones cutáneas. El primer estudio data de 1883 en Breslau , Alemania (ahora Wrocław , Polonia ), donde el médico Alfred Buchwald describió a un hombre que había sufrido durante 16 años un trastorno degenerativo de la piel que ahora se conoce como acrodermatitis crónica atrófica .
En una conferencia de investigación de 1909, el dermatólogo sueco Arvid Afzelius presentó un estudio sobre una lesión en forma de anillo en expansión que había observado en una mujer mayor después de la picadura de una garrapata de oveja. Llamó a la lesión eritema migratorio . La afección de la piel que ahora se conoce como linfocitoma borrelial se describió por primera vez en 1911.
La historia moderna de la comprensión médica de la enfermedad, incluida su causa, diagnóstico y tratamiento, ha sido difícil.
Los problemas neurológicos que siguen a las picaduras de garrapatas se reconocieron a partir de la década de 1920. Los médicos franceses Garin y Bujadoux describieron a un granjero con una radiculitis sensorial dolorosa acompañada de meningitis leve después de una picadura de garrapata. También se observó un gran sarpullido en forma de anillo, aunque los médicos no lo relacionaron con la meningoradiculitis. En 1930, el dermatólogo sueco Sven Hellerström fue el primero en proponer la EM y los síntomas neurológicos posteriores a una picadura de garrapata estaban relacionados. En la década de 1940, el neurólogo alemán Alfred Bannwarth describió varios casos de meningitis linfocítica crónica y polirradiculoneuritis, algunos de los cuales se acompañaban de lesiones cutáneas eritematosas.
Carl Lennhoff, que trabajaba en el Instituto Karolinska en Suecia, creía que muchas enfermedades de la piel eran causadas por espiroquetas. En 1948, utilizó una tinción especial para observar microscópicamente lo que creía que eran espiroquetas en varios tipos de lesiones cutáneas, incluida la EM. Aunque más tarde se demostró que sus conclusiones eran erróneas, se despertó el interés en el estudio de las espiroquetas. En 1949, Nils Thyresson, quien también trabajó en el Instituto Karolinska, fue el primero en tratar ACA con penicilina. En la década de 1950, la relación entre la picadura de garrapata, el linfocitoma, la EM y el síndrome de Bannwarth fue reconocida en toda Europa, lo que llevó al uso generalizado de la penicilina para el tratamiento en Europa.
En 1970, un dermatólogo en Wisconsin llamado Rudolph Scrimenti reconoció una lesión EM en una persona después de recordar un artículo de Hellerström que había sido reimpreso en una revista científica estadounidense en 1950. Este fue el primer caso documentado de EM en los Estados Unidos. Basado en la literatura europea, trató a la persona con penicilina.
El síndrome completo que ahora se conoce como enfermedad de Lyme no se reconoció hasta que se identificó un grupo de casos que originalmente se pensaba que eran artritis reumatoide juvenil en tres ciudades del sureste de Connecticut en 1975, incluidas las ciudades de Lyme y Old Lyme , que dieron a la enfermedad su nombre popular. Esto fue investigado por los médicos David Snydman y Allen Steere del Servicio de Inteligencia Epidémica , y por otros de la Universidad de Yale , incluido Stephen Malawista , a quien se le atribuye el co-descubrimiento de la enfermedad. El reconocimiento de que la gente en los Estados Unidos tenía EM llevó al reconocimiento de que la "artritis de Lyme" era una manifestación de la misma enfermedad transmitida por garrapatas conocida en Europa.
Antes de 1976, los elementos de la infección por B. burgdorferi sensu lato se llamaban o conocían como meningopolineuritis transmitida por garrapatas, síndrome de Garin-Bujadoux, síndrome de Bannwarth, enfermedad de Afzelius, rodilla de Montauk o fiebre por garrapata de oveja. Desde 1976, la enfermedad se conoce con mayor frecuencia como enfermedad de Lyme, borreliosis de Lyme o simplemente borreliosis.
En 1980, Steere, et al. , comenzó a probar regímenes de antibióticos en adultos con enfermedad de Lyme. Ese mismo año, el epidemiólogo del Departamento de Salud del Estado de Nueva York, Jorge Benach, le entregó a Willy Burgdorfer , investigador del Laboratorio Biológico de las Montañas Rocosas , colecciones de I. dammini [ scapularis ] de Shelter Island, Nueva York, un área conocida como endémica de Lyme como parte de una investigación en curso sobre la fiebre maculosa de las Montañas Rocosas. Al examinar las garrapatas en busca de rickettsias, Burgdorfer notó "espiroquetas mal teñidas, bastante largas e irregularmente enrolladas". Un examen más detallado reveló espiroquetas en el 60% de las garrapatas. Burgdorfer atribuyó a su familiaridad con la literatura europea su conocimiento de que las espiroquetas podrían ser la "causa largamente buscada de la ECM y la enfermedad de Lyme". Benach le suministró más garrapatas de Shelter Island y sueros de personas diagnosticadas con la enfermedad de Lyme. El investigador del Centro de Ciencias de la Salud de la Universidad de Texas, Alan Barbour, "ofreció su experiencia para cultivar y caracterizar inmunoquímicamente el organismo". Burgdorfer confirmó posteriormente su descubrimiento aislando, de personas con la enfermedad de Lyme, espiroquetas idénticas a las que se encuentran en las garrapatas. En junio de 1982, publicó sus hallazgos en Science , y la espiroqueta fue nombrada Borrelia burgdorferi en su honor.
Después de la identificación de B. burgdorferi como agente causante de la enfermedad de Lyme, se seleccionaron antibióticos para la prueba, guiados por sensibilidades antibióticas in vitro , incluidos antibióticos de tetraciclina , amoxicilina , cefuroxima axetilo , penicilina intravenosa e intramuscular y ceftriaxona intravenosa . El mecanismo de transmisión de las garrapatas también fue objeto de mucha discusión. Las espiroquetas de B. burgdorferi se identificaron en la saliva de las garrapatas en 1987, lo que confirma la hipótesis de que la transmisión se produce a través de las glándulas salivales de las garrapatas.
sociedad y Cultura
La urbanización y otros factores antropogénicos pueden estar implicados en la propagación de la enfermedad de Lyme a los humanos. En muchas áreas, la expansión de vecindarios suburbanos ha llevado a la deforestación gradual de las áreas boscosas circundantes y a un mayor contacto fronterizo entre humanos y áreas densas de garrapatas. La expansión humana también ha dado lugar a una reducción de los depredadores que cazan ciervos, así como ratones, ardillas listadas y otros pequeños roedores, los principales reservorios de la enfermedad de Lyme. Como consecuencia del mayor contacto humano con el huésped y el vector , la probabilidad de transmisión de la enfermedad ha aumentado considerablemente. Los investigadores están investigando posibles vínculos entre el calentamiento global y la propagación de enfermedades transmitidas por vectores, incluida la enfermedad de Lyme.
Controversia
El término "enfermedad de Lyme crónica" es controvertido y no está reconocido en la literatura médica, y la mayoría de las autoridades médicas desaconsejan el tratamiento con antibióticos a largo plazo para la enfermedad de Lyme. Los estudios han demostrado que la mayoría de las personas diagnosticadas con "enfermedad de Lyme crónica" no tienen evidencia objetiva de infección previa o actual con B. burgdorferi o son personas que deben clasificarse como personas con síndrome de enfermedad de Lyme postratamiento (PTLDS), que se define como Síntomas inespecíficos continuos o recurrentes (como fatiga, dolor musculoesquelético y quejas cognitivas) en una persona previamente tratada por la enfermedad de Lyme.
El documental de 2008 Under Our Skin es conocido por promover teorías de conspiración sobre la "enfermedad de Lyme crónica".
Otros animales
Mascotas
La prevención de la enfermedad de Lyme es un paso importante para mantener seguros a los perros en áreas endémicas. Se dispone de educación preventiva y una serie de medidas preventivas. Primero, para los dueños de perros que viven cerca o que a menudo frecuentan áreas infestadas de garrapatas, la vacunación de rutina de sus perros es un paso importante.
Otra medida preventiva crucial es el uso de acaricidas persistentes, como repelentes tópicos o pesticidas que contienen triazapentadienos ( Amitraz ), fenilpirazoles ( Fipronil ) o permetrina ( piretroides ). Estos acaricidas se dirigen principalmente a las etapas adultas de las garrapatas portadoras de Lyme y reducen la cantidad de garrapatas reproductivamente activas en el medio ambiente. Las formulaciones de estos ingredientes están disponibles en una variedad de formas tópicas, que incluyen manchas, aerosoles, polvos, collares impregnados, soluciones y champús.
El examen de un perro en busca de garrapatas después de estar en un área infestada de garrapatas es una medida de precaución importante para prevenir la enfermedad de Lyme. Los puntos clave para examinar incluyen la cabeza, el cuello y las orejas.
En los perros, un pronóstico grave a largo plazo puede resultar en enfermedad glomerular, que es una categoría de daño renal que puede causar enfermedad renal crónica. Los perros también pueden experimentar una enfermedad articular crónica si la enfermedad no se trata. Sin embargo, la mayoría de los casos de enfermedad de Lyme en perros resultan en una recuperación completa con, y a veces sin, tratamiento con antibióticos. En casos raros, la enfermedad de Lyme puede ser fatal tanto para humanos como para perros.
Referencia
![]() Este artículo incorpora material de dominio público del documento de los Centros para el Control y la Prevención de Enfermedades : "Síndrome de la enfermedad de Lyme posterior al tratamiento" .
Este artículo incorpora material de dominio público del documento de los Centros para el Control y la Prevención de Enfermedades : "Síndrome de la enfermedad de Lyme posterior al tratamiento" .
Otras lecturas
- Ostfeld, Richard (2012). Enfermedad de Lyme: la ecología de un sistema complejo . Nueva York: Oxford University Press . ISBN 978-0199928477.
- Barbour, Alan G. (2015). Enfermedad de Lyme: por qué se propaga, cómo te enferma y qué hacer al respecto . Baltimore. ISBN 9781421417219.
- Halperin, John Jay, ed. (2018). Enfermedad de Lyme: un enfoque basado en la evidencia (2ª ed.). Wallingford, Oxfordshire, Reino Unido: CABI. ISBN 1786392070.
- Radolf, Justin D .; Samuels, D. Scott, eds. (2021). Enfermedad de Lyme y espiroquetas de fiebre recurrente: genómica, biología molecular, interacciones con el huésped y patogénesis de la enfermedad . Poole, Reino Unido: Caister. ISBN 1913652610.
enlaces externos
- Organizaciones de la enfermedad de Lyme en Curlie
- CDC - Enfermedad de Lyme
- Pruebas de la enfermedad de Lyme: pruebas de laboratorio en línea
- NIH - Enfermedad de Lyme
- Pautas NICE - Enfermedad de Lyme
| Clasificación | |
|---|---|
| Recursos externos |
|