Ecuación de Hill (bioquímica) - Hill equation (biochemistry)
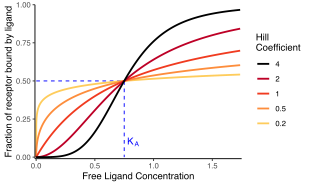
En bioquímica y farmacología , la ecuación de Hill se refiere a dos ecuaciones estrechamente relacionadas que reflejan la unión de ligandos a macromoléculas, en función de la concentración de ligando . Un ligando es "una sustancia que forma un complejo con una biomolécula para cumplir un propósito biológico" ( definición de ligando ), y una macromolécula es una molécula muy grande, como una proteína, con una estructura compleja de componentes ( definición de macromolécula ). La unión proteína-ligando típicamente cambia la estructura de la proteína diana, cambiando así su función en una célula.
La distinción entre las dos ecuaciones de Hill es si miden la ocupación o la respuesta . La ecuación de Hill-Langmuir refleja la ocupación de macromoléculas: la fracción que está saturada o unida por el ligando . Esta ecuación es formalmente equivalente a la isoterma de Langmuir . Por el contrario, la ecuación de Hill propiamente dicha refleja la respuesta celular o tisular al ligando: la producción fisiológica del sistema, como la contracción muscular.
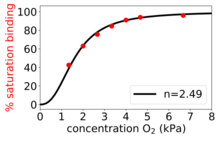
La ecuación de Hill-Langmuir fue formulada originalmente por Archibald Hill en 1910 para describir la curva sigmoidea de unión al O 2 de la hemoglobina .
La unión de un ligando a una macromolécula a menudo se mejora si ya hay otros ligandos presentes en la misma macromolécula (esto se conoce como unión cooperativa ). La ecuación de Hill-Langmuir es útil para determinar el grado de cooperación de los ligandos que se unen a la enzima o al receptor. El coeficiente de Hill proporciona una forma de cuantificar el grado de interacción entre los sitios de unión del ligando.
La ecuación de Hill (para la respuesta) es importante en la construcción de curvas dosis-respuesta .
Proporción de receptores unidos a ligandos
La ecuación de Hill-Langmuir es un caso especial de hipérbola rectangular y se expresa comúnmente de las siguientes formas.
- ,
dónde:
- es la fracción de la concentración de proteína receptora que está unida al ligando ,
- es la concentración total de ligando ,
- es la constante de disociación aparente derivada de la ley de acción de masas ,
- es la concentración de ligando que produce la mitad de la ocupación,
- es el coeficiente de Hill.
Constantes
En farmacología, a menudo se escribe como , donde es el ligando, equivalente a L, y es el receptor. se puede expresar en términos de la cantidad total de receptor y las concentraciones del receptor unido a ligando: . es igual a la relación entre la tasa de disociación del complejo ligando-receptor y su tasa de asociación ( ). Kd es la constante de equilibrio para la disociación. se define de modo que , esto también se conoce como la constante de disociación microscópica y es la concentración de ligando que ocupa la mitad de los sitios de unión. En la literatura reciente, esta constante a veces se denomina .
Ecuación de Gaddum
La ecuación de Gaddum es una generalización adicional de la ecuación de Hill, que incorpora la presencia de un antagonista competitivo reversible. La ecuación de Gaddum se deriva de manera similar a la ecuación de Hill pero con 2 equilibrios: el ligando con el receptor y el antagonista con el receptor. Por tanto, la ecuación de Gaddum tiene 2 constantes: las constantes de equilibrio del ligando y la del antagonista
Parcela de colina
El gráfico de Hill es el reordenamiento de la ecuación de Hill-Langmuir en una línea recta.
Tomando el recíproco de ambos lados de la ecuación de Hill-Langmuir, la reordenación, e invirtiendo de nuevo rendimientos: . Tomar el logaritmo de ambos lados de la ecuación conduce a una formulación alternativa de la ecuación de Hill-Langmuir:
- .
Esta última forma de la ecuación de Hill-Langmuir es ventajosa porque una gráfica de versus produce una gráfica lineal , que se llama gráfica de Hill. Debido a que la pendiente de una gráfica de Hill es igual al coeficiente de Hill para la interacción bioquímica, la pendiente se denota por . Una pendiente mayor que uno indica así una unión cooperativa positiva entre el receptor y el ligando, mientras que una pendiente menor que uno indica unión cooperativa negativamente.
Las transformaciones de ecuaciones en formas lineales como esta eran muy útiles antes del uso generalizado de las computadoras, ya que permitían a los investigadores determinar parámetros ajustando líneas a los datos. Sin embargo, estas transformaciones afectan la propagación del error, y esto puede resultar en una ponderación indebida del error en los puntos de datos cercanos a 0 o 1. Esto afecta los parámetros de las líneas de regresión lineal ajustadas a los datos. Además, el uso de computadoras permite un análisis más robusto que involucra regresión no lineal .
Respuesta del tejido
Debe hacerse una distinción entre la cuantificación de los fármacos que se unen a los receptores y los fármacos que producen respuestas. Puede que no exista necesariamente una relación lineal entre los dos valores. En contraste con la definición anterior de este artículo de la ecuación de Hill-Langmuir, la IUPHAR define la ecuación de Hill en términos de la respuesta del tejido , como
donde es la concentración del fármaco y es la concentración del fármaco que produce una respuesta máxima del 50%. Las constantes de disociación (en la sección anterior) se relacionan con la unión del ligando, mientras que reflejan la respuesta del tejido.
Esta forma de la ecuación puede reflejar las respuestas de tejido / célula / población a los fármacos y puede usarse para generar curvas de respuesta a la dosis . La relación entre y EC50 puede ser bastante compleja ya que una respuesta biológica será la suma de una miríada de factores; un fármaco tendrá un efecto biológico diferente si hay más receptores presentes, independientemente de su afinidad.
El modelo de Del-Castillo Katz se utiliza para relacionar la ecuación de Hill-Langmuir con la activación del receptor al incluir un segundo equilibrio del receptor unido al ligando con una forma activada del receptor unido al ligando.
El análisis estadístico de la respuesta en función del estímulo puede realizarse mediante métodos de regresión como el modelo probit o el modelo logit , u otros métodos como el método de Spearman-Karber . Los modelos empíricos basados en regresión no lineal suelen preferirse al uso de alguna transformación de los datos que linealiza la relación dosis-respuesta.
Coeficiente de colina
El coeficiente de Hill es una medida de ultrasensibilidad (es decir, qué tan inclinada es la curva de respuesta).
El coeficiente de Hill, o puede describir la cooperatividad (o posiblemente otras propiedades bioquímicas, según el contexto en el que se utilice la ecuación de Hill-Langmuir). Cuando sea apropiado, el valor del coeficiente de Hill describe la cooperatividad de la unión del ligando de la siguiente manera:
- . Unión positivamente cooperativa : una vez que una molécula de ligando se une a la enzima, aumenta su afinidad por otras moléculas de ligando. Por ejemplo, el coeficiente de Hill de la unión del oxígeno a la hemoglobina (un ejemplo de cooperatividad positiva) se encuentra dentro del rango de 1,7 a 3,2.
- . Unión negativamente cooperativa : una vez que una molécula de ligando se une a la enzima, su afinidad por otras moléculas de ligando disminuye.
- . Unión no cooperativa (completamente independiente) : la afinidad de la enzima por una molécula de ligando no depende de si otras moléculas de ligando ya están unidas o no. Cuando n = 1, obtenemos un modelo que puede ser modelado por cinética de Michaelis-Menten , en el cual , la constante de Michaelis-Menten .
El coeficiente de Hill se puede calcular en términos de potencia como:
- .
donde y son los valores de entrada necesarios para producir el 10% y el 90% de la respuesta máxima, respectivamente.
Derivación de la cinética de acción de masas
La ecuación de Hill-Langmuir se deriva de manera similar a la ecuación de Michaelis Menten pero incorpora el coeficiente de Hill. Considere una proteína ( ), como la hemoglobina o un receptor de proteína, con sitios de unión para ligandos ( ). La unión de los ligandos a la proteína se puede representar mediante la expresión de equilibrio químico:
- ,
donde (velocidad de avance, o la velocidad de asociación del complejo proteína-ligando) y (velocidad inversa, o la velocidad de disociación del complejo) son las constantes de velocidad de reacción para la asociación de los ligandos a la proteína y su disociación de la proteína, respectivamente. De la ley de acción de masas , que a su vez puede derivarse de los principios de la teoría de colisiones , la constante de disociación aparente , una constante de equilibrio, viene dada por:
- .
Al mismo tiempo, la relación entre la concentración de receptor ocupado y la concentración total de receptor viene dada por:
- .
Al usar la expresión obtenida anteriormente para la constante de disociación, podemos reemplazar con para obtener una expresión simplificada para :
- ,
que es una formulación común de la ecuación de Hill.
Suponiendo que el receptor de proteína estaba inicialmente completamente libre (no unido) a una concentración , luego en cualquier momento, y . En consecuencia, la ecuación de Hill-Langmuir también se escribe comúnmente como una expresión para la concentración de proteína unida:
- .
Todas estas formulaciones asumen que la proteína tiene sitios a los que se pueden unir los ligandos. En la práctica, sin embargo, el coeficiente de Hill rara vez proporciona una aproximación precisa del número de sitios de unión del ligando en una proteína. En consecuencia, se ha observado que el coeficiente de Hill debería interpretarse en cambio como un "coeficiente de interacción" que describe la cooperatividad entre los sitios de unión del ligando.
Aplicaciones
Las ecuaciones de Hill y Hill-Langmuir se utilizan ampliamente en farmacología para cuantificar los parámetros funcionales de un fármaco y también se utilizan en otras áreas de la bioquímica.
La ecuación de Hill se puede utilizar para describir las relaciones dosis-respuesta, por ejemplo , probabilidad de apertura del canal iónico (P-abierto) frente a la concentración de ligando.
Regulación de la transcripción de genes
La ecuación de Hill-Langmuir se puede aplicar para modelar la velocidad a la que se produce un producto génico cuando su gen original está siendo regulado por factores de transcripción (p. Ej., Activadores y / o represores ). Hacerlo es apropiado cuando un gen está regulado por múltiples sitios de unión para factores de transcripción, en cuyo caso los factores de transcripción pueden unirse al ADN de manera cooperativa.
Si la producción de proteína del gen X está regulada ( activada ) por un factor de transcripción Y , entonces la tasa de producción de proteína X puede modelarse como una ecuación diferencial en términos de la concentración de proteína Y activada :
- ,
donde k es la tasa de transcripción máxima de gen X .
Del mismo modo, si la producción de proteína del gen Y está regulada a la baja ( reprimida ) por un factor de transcripción Z , entonces la tasa de producción de proteína Y puede modelarse como una ecuación diferencial en términos de la concentración de proteína Z activada :
- ,
donde k es la tasa de transcripción máxima de gen Y .
Limitaciones
Debido a su suposición de que las moléculas de ligando se unen a un receptor simultáneamente, la ecuación de Hill-Langmuir ha sido criticada como un modelo físicamente irreal. Además, el coeficiente de Hill no debe considerarse una aproximación fiable del número de sitios de unión de ligandos cooperativos en un receptor, excepto cuando la unión del primer y los siguientes ligandos da como resultado una cooperatividad positiva extrema.
A diferencia de los modelos más complejos, la ecuación relativamente simple de Hill-Langmuir proporciona poca información sobre los mecanismos fisiológicos subyacentes de las interacciones proteína-ligando. Esta simplicidad, sin embargo, es lo que hace que la ecuación de Hill-Langmuir sea un modelo empírico útil, ya que su uso requiere poco conocimiento a priori sobre las propiedades de la proteína o del ligando que se está estudiando. No obstante, se han propuesto otros modelos más complejos de vinculación cooperativa. Para obtener más información y ejemplos de dichos modelos, consulte Enlace cooperativo .
La medida de sensibilidad global como el coeficiente de Hill no caracteriza los comportamientos locales de las curvas en forma de s. En cambio, estas características están bien capturadas por la medida del coeficiente de respuesta.
Existe un vínculo entre el coeficiente de Hill y el coeficiente de respuesta, como sigue. Altszyler y col. (2017) han demostrado que estas medidas de ultrasensibilidad pueden vincularse.
Ver también
- Parcela de Bjerrum
- Enlace cooperativo
- Curva de Gompertz
- Modelo de adsorción de Langmuir
- Función logística
- Cinética de Michaelis-Menten
- Ecuación monod
Notas
Referencias
Otras lecturas
- Diccionario médico ilustrado de Dorland
- Coval, ML (diciembre de 1970). "Análisis de los coeficientes de interacción de Hill y la invalidez de la ecuación de Kwon y Brown" . J. Biol. Chem. 245 (23): 6335–6. doi : 10.1016 / S0021-9258 (18) 62614-6 . PMID 5484812 .
- d'A Heck, Henry (1971). "Teoría estadística de la unión cooperativa a proteínas. Ecuación de Hill y el potencial de unión". Mermelada. Chem. Soc . 93 (1): 23-29. doi : 10.1021 / ja00730a004 . PMID 5538860 .
- Atkins, Gordon L. (1973). "Un simple programa de computadora digital para estimar el parámetro de la Ecuación de Hill" . EUR. J. Biochem . 33 (1): 175–180. doi : 10.1111 / j.1432-1033.1973.tb02667.x . PMID 4691349 .
- Endrenyi, Laszlo; Kwong, FHF; Fajszi, Csaba (1975). "Evaluación de pendientes de colinas y coeficientes de colinas cuando se desconoce la unión de saturación o la velocidad" . EUR. J. Biochem . 51 (2): 317–328. doi : 10.1111 / j.1432-1033.1975.tb03931.x . PMID 1149734 .
- Voet, Donald; Voet, Judith G. (2004). Bioquímica .
- Weiss, JN (1997). "La ecuación de Hill revisada: usos y abusos" . Revista FASEB . 11 (11): 835–841. doi : 10.1096 / fasebj.11.11.9285481 . PMID 9285481 . S2CID 827335 .
- Kurganov, BI; Lobanov, AV (2001). "Criterio de validez de la ecuación de Hill para la descripción de las curvas de calibración del biosensor". Anal. Chim. Acta . 427 (1): 11-19. doi : 10.1016 / S0003-2670 (00) 01167-3 .
- Goutelle, Sylvain; Maurin, Michel; Rougier, Florent; Barbaut, Xavier; Bourguignon, Laurent; Ducher, Michel; Maire, Pascal (2008). "La ecuación de Hill: una revisión de sus capacidades en el modelado farmacológico". Farmacología fundamental y clínica . 22 (6): 633–648. doi : 10.1111 / j.1472-8206.2008.00633.x . PMID 19049668 . S2CID 4979109 .
- Gesztelyi R; Zsuga J; Kemeny-Beke A; Varga B; Juhasz B; Tosaki A (2012). "La ecuación de Hill y el origen de la farmacología cuantitativa". Archivo de Historia de las Ciencias Exactas . 66 (4): 427–38. doi : 10.1007 / s00407-012-0098-5 . S2CID 122929930 .
- Colquhoun D (2006). "El análisis cuantitativo de las interacciones fármaco-receptor: una breve historia". Trends Pharmacol Sci . 27 (3): 149–57. doi : 10.1016 / j.tips.2006.01.008 . PMID 16483674 .
- Sonó HP (2006). "El concepto de receptor: la gran idea de la farmacología" . Br J Pharmacol . 147 : S9-16. doi : 10.1038 / sj.bjp.0706457 . PMC 1760743 . PMID 16402126 .

![{\ Displaystyle {\ begin {alineado} \ theta & = {[{\ ce {L}}] ^ {n} \ sobre K_ {d} + [{\ ce {L}}] ^ {n}} \\ & = {[{\ ce {L}}] ^ {n} \ over (K_ {A}) ^ {n} + [{\ ce {L}}] ^ {n}} \\ & = {1 \ más de 1+ \ left ({K_ {A} \ over [{\ ce {L}}]} \ right) ^ {n}} \ end {alineado}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/386ff885fdf558b83ca54868e1c90d7a27431451)

![{\ Displaystyle {\ ce {[L]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b3d168a8fcf5a74047be127a23620e6c9a5534c1)






![{\ Displaystyle \ theta = {\ frac {[LR]} {[R _ {\ rm {total}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a248ec0db4482331e558fa6a376b546a48ca62fe)





![{\ Displaystyle {\ theta \ over 1- \ theta} = {[{\ ce {L}}] ^ {n} \ over K_ {d}} = {[{\ ce {L}}] ^ {n} \ over (K_ {A}) ^ {n}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e62619f678cb95dde3c47e61e2aac4f144f10357)
![{\ Displaystyle {\ begin {alineado} \ log \ left ({\ theta \ over 1- \ theta} \ right) & = n \ log {[{\ ce {L}}]} - \ log {K_ {d }} \\ & = n \ log {[{\ ce {L}}]} - n \ log {K_ {A}} \ end {alineado}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/85e17bac0e7828741f0ce8943abbf129033f3fba)

![{\ Displaystyle \ log {[{\ ce {L}}]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cc44efcd14530f15374d04ede7e01db63da3ac6b)



![{\ Displaystyle {\ begin {alineado} {\ frac {E} {E _ {\ mathrm {max}}}} & = {\ frac {[A] ^ {n}} {{\ text {EC}} _ { 50} ^ {n} + [A] ^ {n}}} \\ & = {\ frac {1} {1+ \ left ({\ frac {{\ text {EC}} _ {50}} {[ A]}} \ right) ^ {n}}} \ end {alineado}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e59f5002b0fc98cc03c0931e09ee8c937da865a2)
![{\ Displaystyle {\ ce {[A]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/881146b6653b24508d87e34a81c84832f1d5ffea)











![{\ Displaystyle {\ ce {{P} + {\ mathit {n}} {L} <=> [k_ {a}] [k_ {d}] {P} {L} _ {\ mathit {n}} }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/30ac3fdcc0a8fffb8e177f213da2c5d9f48b3a29)


![{\ Displaystyle K _ {\ rm {d}} = {k _ {\ rm {d}} \ sobre k _ {\ rm {a}}} = {{[{\ rm {P}}] [{\ rm {L }}] ^ {\ mathit {n}}} \ sobre [{\ rm {PL _ {\ mathit {n}}}}]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cee93ffd577008a7e660672d95224d18aee261d5)
![{\ Displaystyle \ theta = {\ mathrm {Ocupado \ Receptor} \ over \ mathrm {Total \ Receptor}} = {[{\ rm {PL _ {\ mathit {n}}}}] \ over {[{\ rm { P}}] \ + \ [{\ rm {PL _ {\ mathit {n}}}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c3cd51c2f9c4a3453ad4a8bb3d71b65de7a3b3ae)
![{\ textstyle [{\ rm {PL _ {\ mathit {n}}}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/91dd9940fe6058a28b52b197652f5357b8a71656)
![{\ textstyle {[{\ rm {P}}] [{\ rm {L}}] ^ {\ mathit {n}} \ over K _ {\ rm {d}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/947c1d0e40f3d1d66dc9b4091399022ed47df1f1)

![{\ Displaystyle \ theta = {({[{\ rm {P}}] [{\ rm {L}}] ^ {\ mathit {n}} \ over K _ {\ rm {d}}}) \ over { [{\ rm {P}}] \ + \ ({[{\ rm {P}}] [{\ rm {L}}] ^ {\ mathit {n}} \ over K _ {\ rm {d}} })}} = {{[{\ rm {P}}] [{\ rm {L}}] ^ {\ mathit {n}}} \ over {K _ {\ rm {d}} [{\ rm { P}}] \ + \ {[{\ rm {P}}] [{\ rm {L}}] ^ {\ mathit {n}}}}} = {{[{\ rm {L}}] ^ {\ mathit {n}}} \ over {K _ {\ rm {d}} \ + \ {[{\ rm {L}}] ^ {\ mathit {n}}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af78324baf693dfda9800174bb7e7128223ac710)
![{\ textstyle [{\ rm {P_ {0}}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0258fc1d1c94f7b8c9de307e1367a7a7533838cb)
![{\ textstyle {[{\ rm {P}}] + [{\ rm {PL _ {\ mathit {n}}}}]} = [{\ rm {P_ {0}}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c6365d11270f9dc2456a5ea6cc159189909d6552)
![{\ textstyle \ theta = {[{\ rm {PL _ {\ mathit {n}}}}] \ over {[{\ rm {P_ {0}}}] \}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/02daf828c3a908319108a2bdb072f22df3a607ac)
![{\ Displaystyle [{\ rm {PL _ {\ mathit {n}}}}] = [{\ rm {P_ {0}}}] \ cdot {{[{\ rm {L}}] ^ {\ mathit { n}}} \ over {K _ {\ rm {d}} \ + \ {[{\ rm {L}}] ^ {\ mathit {n}}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4b9d33d4a1f61aba5e9239d5cf1f78d8833bf55d)
![{\ Displaystyle {\ mathrm {d} \ over \ mathrm {d} t} [{\ rm {X_ {producido}}}] = k \ \ cdot {{[{\ rm {Y_ {activo}}}] ^ {\ mathit {n}}} \ over {(K_ {A}) ^ {n} \ + \ {[{\ rm {Y_ {active}}}] ^ {\ mathit {n}}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ce8f1d4a7e5379a47f17d14efde6a9c497496bac)
![{\ Displaystyle {\ mathrm {d} \ over \ mathrm {d} t} [{\ rm {Y_ {producido}}}] = k \ \ cdot {{(K_ {A}) ^ {\ mathit {n} }} \ over {(K_ {A}) ^ {n} \ + \ {[{\ rm {Z_ {active}}}] ^ {\ mathit {n}}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c4fca0f3452f5c99014402ed5ed8f04e7286e4be)