Protoporfiria eritropoyética - Erythropoietic protoporphyria
| Protoporfiria eritropoyética | |
|---|---|
| Otros nombres | EPP |
 | |
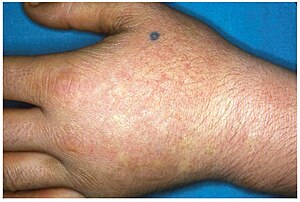
| Lesiones cutáneas crónicas de EPP | |
| Especialidad |
Endocrinología , dermatología |
| Factores de riesgo | dolor e irritación |
La protoporfiria eritropoyética (o comúnmente llamada EPP) es una forma de porfiria , que varía en severidad y puede ser muy dolorosa. Surge de una deficiencia en la enzima ferroquelatasa , que conduce a niveles anormalmente altos de protoporfirina en los glóbulos rojos (eritrocitos) , plasma, piel e hígado . La gravedad varía significativamente de un individuo a otro.
En 2008 se identificó una forma clínicamente similar de porfiria, conocida como protoporfiria dominante ligada al cromosoma X.
Presentación
La EPP suele presentarse en la infancia con el modo de presentación más común como fotosensibilidad aguda de la piel. Afecta áreas expuestas al sol y tiende a ser intratable. Unos minutos de exposición al sol inducen prurito, eritema, hinchazón y dolor. Los períodos de exposición más prolongados pueden provocar quemaduras de segundo grado. Después de exposiciones repetidas, los pacientes pueden presentar liquenificación, hipopigmentación, hiperpigmentación y cicatrización de la piel.
La EPP generalmente se presenta por primera vez en la infancia y, con mayor frecuencia, afecta la cara y la parte superior de los brazos, las manos y los pies y las superficies expuestas de las piernas. La mayoría de los pacientes, si la EPP no es tan grave, manifiestan síntomas con el inicio de la pubertad cuando los niveles de hormonas masculinas y femeninas se elevan durante el desarrollo y el mantenimiento sexual. La EPP más grave puede manifestarse en la infancia. La EPP se puede desencadenar por exposición al sol aunque el paciente esté detrás de un vidrio. Se sabe que incluso las emisiones de UV de la soldadura por arco con el uso de una máscara protectora completa desencadenan la EPP. La EPP también puede manifestarse entre los 3 y los 6 años.
La exposición prolongada al sol puede provocar edema de manos, cara y pies, raramente con ampollas y petequias. El engrosamiento de la piel a veces puede ocurrir con el tiempo.
Las personas con EPP también tienen un mayor riesgo de desarrollar cálculos biliares . Un estudio ha señalado que los pacientes con EPP sufren de deficiencia de vitamina D.
Insuficiencia hepática
La protoporfirina se acumula a niveles tóxicos en el hígado en 5 a 20% de los pacientes con EPP, lo que conduce a insuficiencia hepática. El espectro de enfermedad hepatobiliar asociada con EPP es amplio. Incluye colelitiasis, enfermedad hepática parenquimatosa leve, enfermedad hepatocelular progresiva y enfermedad hepática en etapa terminal.
La falta de marcadores de diagnóstico de insuficiencia hepática hace que sea difícil predecir qué pacientes pueden experimentar insuficiencia hepática y el mecanismo de la insuficiencia hepática es poco conocido. Un estudio europeo retrospectivo identificó a 31 pacientes con EPP que recibieron un trasplante de hígado entre 1983 y 2008, con reacciones fototóxicas en el 25% de los pacientes que no estaban protegidos por filtros de luz quirúrgica. El mismo estudio observó una recurrencia del 69% de la enfermedad en el órgano injertado. Se han identificado cinco trasplantes de hígado para EPP en el Reino Unido entre 1987 y 2009. Se recomiendan pruebas hepáticas frecuentes en pacientes con EPP donde no se ha identificado una terapia eficaz para controlar la insuficiencia hepática hasta la fecha.
El embarazo
Se informa que los síntomas de fotosensibilidad al EPP disminuyen en algunas pacientes durante el embarazo y la menstruación, aunque este fenómeno no es constante y no se comprende el mecanismo.
Genética
La mayoría de los casos de EPP son el resultado de errores innatos del metabolismo, pero el defecto metabólico en algunos pacientes puede ser adquirido. La mutación del gen que codifica la ferroquelatasa en el brazo largo del cromosoma 18 se encuentra en la mayoría de los casos. La ferroquelatasa (FECH) cataliza la inserción de hierro ferroso en el anillo de protoporfirina IX para formar hemo. EPP exhibe patrones de herencia recesivos y dominantes y un alto grado de heterogeneidad alélica con penetrancia incompleta. La mayoría de los heterocigotos son asintomáticos. Los síntomas no ocurren a menos que la actividad de FECH sea menor al 30% de lo normal, pero niveles tan bajos no están presentes en la mayoría de los pacientes.
Fisiopatología
Las células que sintetizan hemo son predominantemente eritroblastos / reticulocitos en la médula ósea (80%) y hepatocitos (20%). La deficiencia de FECH da como resultado una mayor liberación de protoporfirina, que se une a la albúmina en el plasma y posteriormente se somete a extracción hepática. Normalmente, la mayor parte de la protoporfirina en los hepatocitos se secreta en la bilis; el resto se transforma en hemo. Parte de la protoporfirina de la bilis regresa al hígado como consecuencia de la circulación enterohepática; la protoporfirina restante en el intestino se excreta por las heces. La protoporfirina es insoluble y, por tanto, no está disponible para la excreción renal. En EPP, la biotransformación subnormal de protoporfirina en hemo da como resultado la acumulación de protoporfirina en los hepatocitos.
Dado que la deficiencia de FECH se asocia con concentraciones elevadas de protoporfirina en eritrocitos, plasma, piel e hígado, la retención de protoporfirina en la piel predispone a la fotosensibilidad aguda. Como resultado de la absorción de luz ultravioleta y visible (sensibilidad máxima a 400 nm, con picos menores entre 500-625 nm) por la protoporfirina en el plasma y los eritrocitos cuando la sangre circula a través de los vasos dérmicos, se forman radicales libres, los eritrocitos se vuelven inestables y dañan a la piel se induce.
Un aumento significativo en la excreción hepatobiliar de protoporfirina puede dañar el hígado a través de fenómenos colestáticos y estrés oxidativo, lo que predispone a la enfermedad hepatobiliar de diversos grados de gravedad.
Diagnóstico
La EPP se sospecha generalmente por la presencia de fotosensibilidad aguda de la piel y puede confirmarse mediante la detección de un pico de fluorescencia plasmática a 634 nm. También es útil para encontrar niveles elevados de protoporfirina en las heces y la demostración de un exceso de protoporfirina libre en los eritrocitos.
El cribado de la mutación FECH en un alelo o la mutación de ganancia de función del ácido aminolevulínico sintasa 2 en miembros seleccionados de la familia puede ser útil, especialmente en el asesoramiento genético.
La biopsia hepática confirma la enfermedad hepática en la EPP por la presencia de depósitos de protoporfirina en los hepatocitos que se pueden observar como un pigmento marrón dentro de los canalículos biliares y los macrófagos portales. Macroscópicamente, el hígado cirrótico puede tener un color negro debido a los depósitos de protoporfirina. Utilizando luz polarizada se encuentra la característica forma de cruz de Malta de los depósitos de pigmentos cristalinos birrefringentes. El examen del tejido hepático bajo una lámpara de Wood revela una fluorescencia roja debido a la protoporfirina. La biopsia hepática no es útil para estimar el pronóstico de la enfermedad hepática.
Tratamiento
No existe cura para este trastorno; sin embargo, los síntomas generalmente se pueden controlar limitando la exposición al sol durante el día y algunos tipos de iluminación artificial. La mayoría de los tipos de iluminación artificial emiten luz en las longitudes de onda problemáticas, siendo la iluminación fluorescente la peor infractora. La temperatura del color puede ser un buen indicador de qué luz es más perjudicial, ya que cuanto mayor es la temperatura del color, más luz violeta (380-450 nm) se emite. La iluminación incandescente y LED en el rango de blanco suave (2700-3000K) produce la luz menos problemática. Además, la selección de bombillas de menor potencia puede reducir la salida general de luz.
Dado que la fotosensibilidad resulta de la luz en el espectro visible, la mayoría de los protectores solares son de poca utilidad (con la excepción del óxido de zinc no nano que proporciona una protección uniforme entre 290-400 nm y algo de protección hasta 700 nm). La ropa de protección solar también puede ser muy útil, aunque la ropa con valores de UPF solo se clasifica en función de su protección UV (hasta 400 nm) y no de su protección del espectro visible. Algunos fabricantes de ropa de protección solar utilizan óxido de zinc en sus tejidos, como la línea ZnO Suntect de Coolibar, que ofrecerá protección contra la luz visible.
Algunos pacientes construyen gradualmente una capa protectora de melanina al exponerse regularmente por períodos cortos a la radiación ultravioleta.
Las películas para ventanas que bloquean los rayos ultravioleta y la luz visible hasta 450 nm pueden aliviar los síntomas si se aplican en las ventanas del automóvil y de la casa del paciente. Un ejemplo de ello sería Madico Amber 81, que puede proteger a través del rango de 500 nm.
Los protectores de pantalla de bloqueo azul pueden ayudar a aliviar los síntomas causados por televisores, teléfonos, tabletas y pantallas de computadora.
La EPP se considera una de las porfirias menos graves. A menos que haya insuficiencia hepática, no es una enfermedad potencialmente mortal.
Terapias aprobadas
La afamelanotida , desarrollada por Clinuvel Pharmaceuticals con sede en Australia, fue aprobada en Europa en diciembre de 2014 para el tratamiento o la prevención de la fototoxicidad en adultos con EPP.
Uso no indicado en la etiqueta
Los pacientes con EPP usan varios medicamentos fuera de la etiqueta :
- El ácido ursodesoxicólico es un ácido biliar que se administra para promover la secreción biliar de protoporfirina. Los resultados de su uso en EPP son controvertidos. Sin embargo, se sabe que altera la composición de la bilis, protege a los hepatocitos del efecto citotóxico de los ácidos biliares hidrófobos y estimula la secreción biliar mediante varios mecanismos distintos.
- La hematina parece reducir el exceso de producción de protoporfirina en la médula ósea. Se ha administrado a pacientes con EPP (3-4 mg / kg iv) que desarrollan una crisis después del trasplante de hígado.
- La plasmaféresis también puede disminuir los niveles de protoporfirina en plasma, sin embargo, su uso en el tratamiento de episodios agudos es controvertido.
- La colestiramina es una resina administrada por vía oral que reduce los niveles circulantes de protoporfirina uniéndose a la protoporfirina en el intestino y, por tanto, interrumpiendo la circulación enterohepática. Por lo general, se usa en combinación con otros enfoques de tratamiento.
- El carbón activado , como la colestiramina, se une a la protoporfirina en el intestino y evita su absorción. Es barato y está fácilmente disponible. Parece ser eficaz para reducir los niveles de protoporfirina circulante.
El trasplante de médula ósea , el trasplante de hígado , la acetilcisteína , la diálisis extracorpórea con albúmina , el hierro parenteral y la transfusión de eritrocitos son planes alternativos para el tratamiento de la EEP.
Suplementos de venta libre
Algunos suplementos de venta libre pueden ayudar:
- Proferrin es un suplemento de hemo oral que puede funcionar de manera similar a Hematin.
- B. subtilis (un probiótico grampositivo del suelo) produce ferroquelatasa, que puede convertir parte de la protoporfirina en el intestino en hemo.
- Beta caroteno , aunque un metaanálisis reciente del tratamiento con caroteno ha puesto en duda su eficacia.
Epidemiología
Los informes de casos sugieren que la EPP prevalece a nivel mundial. La prevalencia se ha estimado entre 1 en 75,000 y 1 en 200,000, sin embargo, se ha observado que la prevalencia de EPP puede estar aumentando debido a una mejor comprensión de la enfermedad y un mejor diagnóstico. Se estima que entre 5.000 y 10.000 personas en todo el mundo tienen EPP. La EPP se considera la forma más común de porfiria en los niños. La prevalencia en Suecia se ha publicado como 1: 180.000.
Historia
La protoporfiria eritropoyética fue descrita por primera vez en 1953 por Kosenow y Treibs y completada en 1960 por Magnus et al. en el St John's Institute of Dermatology de Londres.
Ver también
Referencias
enlaces externos
- Protoporfiria eritropoyética en NLM Genetics Home Reference
| Clasificación | |
|---|---|
| Recursos externos |