Epiclorhidrina - Epichlorohydrin

|
|||
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC preferido
2- (clorometil) oxirano |
|||
| Otros nombres
(Clorometil) oxirano
Epiclorhidrina 1-Cloro-2,3-epoxipropano Óxido de γ-cloropropileno Cloruro de glicidilo |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 79785 | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.003.128 |
||
| Número CE | |||
| 164180 | |||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| un numero | 2023 | ||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| C 3 H 5 ClO | |||
| Masa molar | 92,52 g / mol | ||
| Apariencia | líquido incoloro | ||
| Olor | ajo o similar al cloroformo | ||
| Densidad | 1,1812 g / cm 3 | ||
| Punto de fusion | −25,6 ° C (−14,1 ° F; 247,6 K) | ||
| Punto de ebullición | 117,9 ° C (244,2 ° F; 391,0 K) | ||
| 7% (20 ° C) | |||
| Presión de vapor | 13 mmHg (20 ° C) | ||
| Riesgos | |||
| Ficha de datos de seguridad | MSDS externa | ||
| Pictogramas GHS |
    
|
||
| Palabra de señal GHS | Peligro | ||
| H226 , H301 , H311 , H314 , H317 , H331 , H350 | |||
| P201 , P202 , P210 , P233 , P240 , P241 , P242 , P243 , P260 , P261 , P264 , P270 , P271 , P272 , P280 , P281 , P301 + 310 , P301 + 330 + 331 , P302 + 352 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P308 + 313 , P310 , P311 | |||
| NFPA 704 (diamante de fuego) | |||
| punto de inflamabilidad | 32 ° C (90 ° F; 305 K) | ||
| Límites explosivos | 3,8-21% | ||
| Dosis o concentración letal (LD, LC): | |||
|
LC 50 ( concentración media )
|
3617 ppm (rata, 1 h) 2165 ppm (rata, 1 h) 250 ppm (rata, 8 h) 244 ppm (rata, 8 h) 360 ppm (rata, 6 h) |
||
|
LC Lo ( menor publicado )
|
250 ppm (rata, 4 horas) | ||
| NIOSH (límites de exposición a la salud de EE. UU.): | |||
|
PEL (permitido)
|
TWA 5 ppm (19 mg / m 3 ) [piel] | ||
|
REL (recomendado)
|
Carcinógeno | ||
|
IDLH (peligro inmediato)
|
Ca [75 ppm] | ||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
La epiclorhidrina (abreviado ECH ) es un compuesto organoclorado y un epóxido . A pesar de su nombre, no es una halohidrina . Es un líquido incoloro con un picante, ajo-como olor, moderadamente soluble en agua, pero miscible con la mayoría polares orgánicos disolventes . Es una molécula quiral que generalmente existe como una mezcla racémica de enantiómeros diestros y zurdos . La epiclorhidrina es un compuesto electrófilo altamente reactivo y se utiliza en la producción de glicerol , plásticos, colas y resinas epoxi, diluyentes epoxi y elastómeros .
Producción
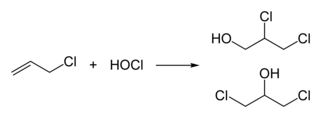
La epiclorhidrina se fabrica tradicionalmente a partir de cloruro de alilo en dos pasos, comenzando con la adición de ácido hipocloroso , que produce una mezcla de dos alcoholes isoméricos :
En el segundo paso, esta mezcla se trata con base para dar el epóxido :
De esta forma, se producen anualmente más de 800.000 toneladas (1997) de epiclorhidrina.
Rutas del glicerol
La epiclorhidrina fue descrita por primera vez en 1848 por Marcellin Berthelot . El compuesto se aisló durante estudios sobre reacciones entre glicerol y cloruro de hidrógeno gaseoso .
Con reminiscencias del experimento de Berthelot, se han comercializado plantas de glicerol a epiclorhidrina (GTE). Esta tecnología aprovecha la disponibilidad de glicerol barato procedente del procesamiento de biocombustibles . En el proceso desarrollado por Dow Chemical , el glicerol sufre dos reacciones de sustitución cuando se trata con cloruro de hidrógeno en presencia de un catalizador de ácido carboxílico . Este es el mismo intermedio formado en el proceso de cloruro de alilo / ácido hipocloroso, y luego se trata igualmente con una base para formar epiclorhidrina.
Otras rutas
Las rutas que involucran menos productos intermedios clorados han seguido atrayendo interés. Uno de estos procesos implica la epoxidación de cloruro de alilo.
Aplicaciones
Síntesis de glicerol y resinas epoxi.
La epiclorhidrina se convierte principalmente en bisfenol A diglicidil éter , un componente básico en la fabricación de resinas epoxi . También es un precursor de los monómeros para otras resinas y polímeros. Otro uso es la conversión a glicerol sintético . Sin embargo, el rápido aumento de la producción de biodiésel , donde el glicerol es un producto de desecho, ha provocado un exceso de glicerol en el mercado, lo que hace que este proceso sea antieconómico. El glicerol sintético ahora se usa solo en aplicaciones farmacéuticas y biotecnológicas sensibles donde los estándares de calidad son muy altos.
Aplicaciones menores y de nicho
La epiclorhidrina es un precursor versátil en la síntesis de muchos compuestos orgánicos. Por ejemplo, se convierte en nitrato de glicidilo , un aglutinante energético utilizado en composiciones explosivas y propulsoras. La epiclorhidrina se hace reaccionar con un nitrato alcalino, como el nitrato de sodio , produciendo nitrato de glicidilo y cloruro alcalino. Se usa como solvente para celulosa , resinas y pinturas, y ha encontrado uso como fumigante de insectos.
Los polímeros hechos de epiclorhidrina, por ejemplo, resinas de poliamida-epiclorhidrina, se utilizan en el refuerzo de papel y en la industria alimentaria para fabricar bolsas de té , filtros de café y tripas para salchichas / salami, así como con purificación de agua .
Una aplicación bioquímica importante de la epiclorhidrina es su uso como agente reticulante para la producción de resinas cromatográficas de exclusión por tamaño de Sephadex a partir de dextranos .
La seguridad
La epiclorhidrina está clasificada por varias agencias y grupos internacionales de investigación en salud como un carcinógeno probable o probable en humanos. El consumo oral prolongado de niveles altos de epiclorhidrina podría provocar problemas estomacales y un mayor riesgo de cáncer. La exposición ocupacional a la epiclorhidrina por inhalación podría provocar irritación pulmonar y un mayor riesgo de cáncer de pulmón.
Referencias
- ^ Índice de Merck , 12a edición, 3648 .
- ^ a b c d e f Guía de bolsillo de NIOSH sobre peligros químicos. "# 0254" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ a b "Epiclorhidrina" . Concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ "Ficha informativa del consumidor de la EPA" . Epa.gov . Consultado el 2 de diciembre de 2011 .
- ^ Braun, G. (1936). "Epiclorhidrina y Epybromohydrin". Síntesis orgánicas . 16 : 30. doi : 10.15227 / orgsyn.016.0030 .
- ^ Guenter Sienel; Robert Rieth; Kenneth T. Rowbottom. "Epóxidos". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a09_531 .
- ^ Ludger Krähling; Jürgen Krey; Gerald Jakobson; Johann Grolig; Leopold Miksche. "Compuestos de alilo". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a01_425 .
- ^ Berthelot, Marcelino (1854). "Sur les combinaisons de la glycérine avec les acides et sur la synthèse des principes immédiats des graisses animaux" . Ana. Chim. Phys . Serie 3. 41 : 216–319. Archivado desde el original el 2 de abril de 2015 . Consultado el 2 de marzo de 2015 .
- ↑ Doris de Guzman (20 de enero de 2011). "Cultivo de plantas de glicerina a ECH" . Productos químicos ecológicos ICIS.
- ^ Bell, Bruce M .; Briggs, John R .; Campbell, Robert M .; Chambers, Susanne M .; Gaarenstroom, Phil D .; Hippler, Jeffrey G .; Hook, Bruce D .; Kearns, Kenneth; et al. (2008). "Glicerina como materia prima renovable para la producción de epiclorhidrina. El proceso GTE" (PDF) . LIMPIO - Suelo, Aire, Agua . 36 (8): 657. doi : 10.1002 / clen.200800067 . Archivado desde el original (reimpresión de texto completo) el 18 de julio de 2012 . Consultado el 5 de marzo de 2012 .
- ^ Jun Li, Gongda Zhao, Shuang Gao, Ying Lv, Jian Li y Zuwei Xi (2006). "Epoxidación de cloruro de alilo a epiclorhidrina por un catalizador con soporte reversible con H2O2 en condiciones sin disolventes". Org. Proceso Res. Dev . 10 (5): 876–880. doi : 10.1021 / op060108k .Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )
- ^ Pham, Ha Q .; Marcas, Maurice J. (2012). "Resina epoxica". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a09_547.pub2 . ISBN 978-3527306732.
- ^ Taylor, Phil (16 de octubre de 2008). "¡La glicerina sintética está de regreso (pero nunca desapareció)!" . Tecnólogo en farmacia . Consultado el 29 de noviembre de 2018 .
- ^ Gould, RF Advanced Propellant Chemistry , ACS Chemistry Series 54, 1966
- ^ "Laboratorios de pruebas de agua suburbana: hoja de datos de la epiclorhidrina" . H2otest.com. Archivado desde el original el 5 de abril de 2012 . Consultado el 2 de diciembre de 2011 .
- ^ "Sustancias químicas del gobierno de Canadá: oxirano, (clorometil) - (epiclorhidrina) número de registro CAS 106-89-8" . 13 de febrero de 2008 . Consultado el 7 de mayo de 2013 .
- ^ "GE Healthcare Life Sciences - Instrucciones para Sephadex Media" . .gelifesciences.com. Archivado desde el original el 18 de febrero de 2012 . Consultado el 2 de diciembre de 2011 .
- ^ "Sistema de información de riesgo integrado EPA: epiclorhidrina (CASRN 106-89-8)" . Consultado el 7 de mayo de 2013 .
- ^ "Gobierno de Canadá: evaluación de detección de epiclorhidrina" . Consultado el 7 de mayo de 2013 .
- ^ "Guía de bolsillo de NIOSH sobre peligros químicos - epiclorhidrina" . Consultado el 20 de septiembre de 2013 .
- ^ "Información básica sobre la epiclorhidrina en el agua potable" . Consultado el 7 de mayo de 2013 .
- ^ "Gobierno de Canadá: evaluación de detección de epiclorhidrina" . Consultado el 7 de mayo de 2013 .