Citocromo c oxidasa - Cytochrome c oxidase
| Citocromo c oxidasa | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| Identificadores | |||||||||
| CE no. | 1.9.3.1 | ||||||||
| No CAS. | 9001-16-5 | ||||||||
| Bases de datos | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| FÁCIL | NiceZyme vista | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | camino metabólico | ||||||||
| PRIAM | perfil | ||||||||
| Estructuras PDB | RCSB PDB PDBe PDBsum | ||||||||
| Ontología de genes | AmiGO / QuickGO | ||||||||
| |||||||||
| Citocromo c oxidasa | |
|---|---|

| |
| Identificadores | |
| Símbolo | Citocromo c oxidasa |
| Superfamilia OPM | 4 |
| Proteína OPM | 2dyr |
| Membranome | 257 |
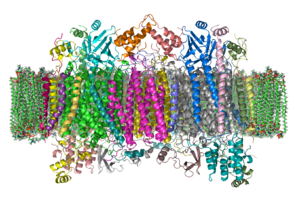
La enzima citocromo c oxidasa o Complejo IV , EC 1.9.3.1 , es un gran complejo proteico transmembrana que se encuentra en bacterias , arqueas y mitocondrias de eucariotas .
Es la última enzima en la cadena de transporte de electrones respiratorios de las células ubicadas en la membrana. Recibe un electrón de cada una de las cuatro moléculas del citocromo c y las transfiere a una molécula de dioxígeno, convirtiendo el oxígeno molecular en dos moléculas de agua. En este proceso, une cuatro protones de la fase acuosa interna para formar dos moléculas de agua y transloca otros cuatro protones a través de la membrana, aumentando la diferencia transmembrana del potencial electroquímico de protones que la ATP sintasa utiliza para sintetizar ATP .
Estructura
El complejo
El complejo es una gran proteína de membrana integral compuesta por varios sitios protésicos de metal y 14 subunidades de proteínas en mamíferos. En los mamíferos, once subunidades son de origen nuclear y tres se sintetizan en las mitocondrias. El complejo contiene dos hemes , un citocromo una y citocromo a 3 , y dos de cobre centros, los Cu A y Cu B centros. De hecho, el citocromo a 3 y Cu B forman un centro binuclear que es el sitio de reducción de oxígeno. El citocromo c , que es reducido por el componente anterior de la cadena respiratoria (complejo citocromo bc1, complejo III), se acopla cerca del centro binuclear de Cu A y le pasa un electrón, oxidándose de nuevo al citocromo c que contiene Fe 3+ . El centro binuclear de Cu A reducido ahora pasa un electrón al citocromo a, que a su vez pasa un electrón al centro binuclear 3 -Cu B del citocromo a . Los dos iones metálicos en este centro binuclear están separados por 4.5 Å y coordinan un ion hidróxido en el estado completamente oxidado.
Los estudios cristalográficos de la citocromo c oxidasa muestran una modificación postraduccional inusual, que une el C6 de Tyr (244) y el ε-N de His (240) (numeración de enzimas bovinas). Desempeña un papel vital al permitir que el centro binuclear citocromo a 3 -Cu B acepte cuatro electrones para reducir el oxígeno molecular a agua . Anteriormente se pensaba que el mecanismo de reducción implicaba un intermedio de peróxido , que se creía que conducía a la producción de superóxido . Sin embargo, el mecanismo actualmente aceptado implica una rápida reducción de cuatro electrones que implica la ruptura inmediata del enlace oxígeno-oxígeno, evitando cualquier intermedio que pueda formar superóxido.
Las subunidades conservadas
| No. | Nombre de la subunidad | Proteína humana | Descripción de proteínas de UniProt | Familia Pfam con proteína humana |
|---|---|---|---|---|
| 1 | Cox1 | COX1_HUMAN | Subunidad 1 del citocromo c oxidasa | Pfam PF00115 |
| 2 | Cox2 | COX2_HUMAN | Subunidad 2 del citocromo c oxidasa | Pfam PF02790 , Pfam PF00116 |
| 3 | Cox3 | COX3_HUMAN | Subunidad 3 del citocromo c oxidasa | Pfam PF00510 |
| 4 | Cox4i1 | COX41_HUMAN | Citocromo c oxidasa subunidad 4 isoforma 1, mitocondrial | Pfam PF02936 |
| 5 | Cox4a2 | COX42_HUMAN | Citocromo c oxidasa subunidad 4 isoforma 2, mitocondrial | Pfam PF02936 |
| 6 | Cox5a | COX5A_HUMAN | Subunidad 5A del citocromo c oxidasa, mitocondrial | Pfam PF02284 |
| 7 | Cox5b | COX5B_HUMAN | Subunidad 5B del citocromo c oxidasa, mitocondrial | Pfam PF01215 |
| 8 | Cox6a1 | CX6A1_HUMAN | Subunidad 6A1 del citocromo c oxidasa, mitocondrial | Pfam PF02046 |
| 9 | Cox6a2 | CX6A2_HUMAN | Subunidad 6A2 del citocromo c oxidasa, mitocondrial | Pfam PF02046 |
| 10 | Cox6b1 | CX6B1_HUMAN | Subunidad 6B1 del citocromo c oxidasa | Pfam PF02297 |
| 11 | Cox6b2 | CX6B2_HUMAN | Subunidad 6B2 del citocromo c oxidasa | Pfam PF02297 |
| 12 | Cox6c | COX6C_HUMAN | Subunidad 6C del citocromo c oxidasa | Pfam PF02937 |
| 13 | Cox7a1 | CX7A1_HUMAN | Subunidad 7A1 del citocromo c oxidasa, mitocondrial | Pfam PF02238 |
| 14 | Cox7a2 | CX7A2_HUMAN | Subunidad 7A2 del citocromo c oxidasa, mitocondrial | Pfam PF02238 |
| 15 | Cox7a3 | COX7S_HUMAN | Subunidad de citocromo c oxidasa supuesta 7A3, mitocondrial | Pfam PF02238 |
| dieciséis | Cox7b | COX7B_HUMAN | Subunidad 7B del citocromo c oxidasa, mitocondrial | Pfam PF05392 |
| 17 | Cox7c | COX7C_HUMAN | Subunidad 7C del citocromo c oxidasa, mitocondrial | Pfam PF02935 |
| 18 | Cox7r | COX7R_HUMAN | Proteína relacionada con la subunidad 7A del citocromo c oxidasa, mitocondrial | Pfam PF02238 |
| 19 | Cox8a | COX8A_HUMAN | Subunidad 8A del citocromo c oxidasa, P mitocondrial | Pfam PF02285 |
| 20 | Cox8c | COX8C_HUMAN | Subunidad 8C del citocromo c oxidasa, mitocondrial | Pfam PF02285 |
| Subunidades de ensamblaje | ||||
| 1 | Coa1 | COA1_HUMAN | Homólogo del factor de ensamblaje 1 de la citocromo c oxidasa | Pfam PF08695 |
| 2 | Coa3 | COA3_HUMAN | Homólogo del factor de ensamblaje 3 de la citocromo c oxidasa, mitocondrial | Pfam PF09813 |
| 3 | Coa4 | COA4_HUMAN | Homólogo del factor de ensamblaje 4 de la citocromo c oxidasa, mitocondrial | Pfam PF06747 |
| 4 | Coa5 | COA5_HUMAN | Factor de ensamblaje de citocromo c oxidasa 5 | Pfam PF10203 |
| 5 | Coa6 | COA6_HUMAN | Homólogo del factor de ensamblaje de oxidasa citocromo c 6 | Pfam PF02297 |
| 6 | Coa7 | COA7_HUMAN | Factor de ensamblaje de citocromo c oxidasa 7, | Pfam PF08238 |
| 7 | Cox11 | COX11_HUMAN | Proteína de ensamblaje de citocromo c oxidasa COX11 mitocondrial | Pfam PF04442 |
| 8 | Cox14 | COX14_HUMAN | Proteína de ensamblaje de citocromo c oxidasa | Pfam PF14880 |
| 9 | Cox15 | COX15_HUMAN | Homólogo de la proteína de ensamblaje de oxidasa del citocromo c COX15 | Pfam PF02628 |
| 10 | Cox16 | COX16_HUMAN | Proteína de ensamblaje de citocromo c oxidasa COX16 homólogo mitocondrial | Pfam PF14138 |
| 11 | Cox17 | COX17_HUMAN | Chaperona de cobre de citocromo c oxidasa | Pfam PF05051 |
| 12 | Cox18 | COX18_HUMAN | Proteína de la membrana interna mitocondrial (proteína 18 de ensamblaje de oxidasa del citocromo c) | Pfam PF02096 |
| 13 | Cox19 | COX19_HUMAN | Proteína de ensamblaje de citocromo c oxidasa | Pfam PF06747 |
| 14 | Cox20 | COX20_HUMAN | Homólogo de la proteína 20 de la citocromo c oxidasa | Pfam PF12597 |
Montaje
El ensamblaje de COX en levaduras es un proceso complejo que no se comprende del todo debido a la agregación rápida e irreversible de subunidades hidrofóbicas que forman el complejo de holoenzimas, así como la agregación de subunidades mutantes con parches hidrofóbicos expuestos. Las subunidades COX están codificadas tanto en el genoma nuclear como en el mitocondrial. Las tres subunidades que forman el núcleo catalítico de COX están codificadas en el genoma mitocondrial.
Los hemes y cofactores se insertan en las subunidades I y II. Las dos moléculas de hemo residen en la subunidad I, lo que ayuda con el transporte a la subunidad II, donde dos moléculas de cobre ayudan con la transferencia continua de electrones. Las subunidades I y IV inician el montaje. Diferentes subunidades pueden asociarse para formar subcomplejos intermedios que luego se unen a otras subunidades para formar el complejo COX. En modificaciones posteriores al ensamblaje, COX formará un homodímero. Esto es necesario para la actividad. Ambos dímeros están conectados por una molécula de cardiolipina , que se ha descubierto que juega un papel clave en la estabilización del complejo holoenzimático. La disociación de las subunidades VIIa y III junto con la eliminación de cardiolipina da como resultado una pérdida total de actividad enzimática. Se sabe que las subunidades codificadas en el genoma nuclear desempeñan un papel en la dimerización y estabilidad de la enzima. Las mutaciones en estas subunidades eliminan la función COX.
Se sabe que el ensamblaje se produce en al menos tres etapas distintas de determinación de la velocidad. Se han encontrado los productos de estos pasos, aunque no se han determinado las composiciones de subunidades específicas.
La síntesis y el ensamblaje de las subunidades I, II y III de COX se facilitan mediante activadores de traducción, que interactúan con las regiones 5 'no traducidas de los transcritos de ARNm mitocondrial. Los activadores de traducción están codificados en el núcleo. Pueden operar a través de la interacción directa o indirecta con otros componentes de la maquinaria de traducción, pero los mecanismos moleculares exactos no están claros debido a las dificultades asociadas con la síntesis de la maquinaria de traducción in vitro. Aunque las interacciones entre las subunidades I, II y III codificadas dentro del genoma mitocondrial hacen una menor contribución a la estabilidad de la enzima que las interacciones entre las subunidades bigenómicas, estas subunidades están más conservadas, lo que indica posibles roles inexplorados para la actividad enzimática.
Bioquímica
Reacción sumaria:
- 4 Fe 2+ - citocromo c + 4 H + en + O 2 → 4 Fe 3+ - citocromo c + 2 H 2 O + 4 H + fuera
Se pasan dos electrones desde dos citocromos c, a través de los sitios de Cu A y citocromo a hasta el centro binuclear del citocromo a 3 - Cu B , reduciendo los metales a la forma Fe 2+ y Cu + . El ligando de hidróxido se protona y se pierde como agua, creando un vacío entre los metales que se llena con O 2 . El oxígeno se reduce rápidamente, con dos electrones procedentes del citocromo a 3 Fe 2+ , que se convierte en la forma ferryl oxo (Fe 4+ = O). El átomo de oxígeno cercano a Cu B toma un electrón de Cu + y un segundo electrón y un protón del hidroxilo de Tyr (244), que se convierte en un radical tirosilo. El segundo oxígeno se convierte en un ion hidróxido al recoger dos electrones y un protón. Un tercer electrón que surge de otro citocromo c pasa a través de los dos primeros portadores de electrones hasta el centro binuclear del citocromo a 3 - Cu B , y este electrón y dos protones convierten el radical tirosilo de nuevo en Tyr y el hidróxido unido a Cu B 2+ a una molécula de agua. El cuarto electrón de otro citocromo c fluye a través de Cu A y el citocromo a hacia el centro binuclear del citocromo a 3 - Cu B , reduciendo el Fe 4+ = O a Fe 3+ , con el átomo de oxígeno recogiendo un protón simultáneamente, regenerando este oxígeno. como un ion hidróxido coordinado en el medio del citocromo un centro 3 -Cu B como estaba al comienzo de este ciclo. El proceso neto es que se utilizan cuatro citocromos c reducidos, junto con 4 protones, para reducir el O 2 a dos moléculas de agua.
Inhibición
La COX existe en tres estados conformacionales: totalmente oxidado (pulsado), parcialmente reducido y totalmente reducido. Cada inhibidor tiene una alta afinidad por un estado diferente. En el estado pulsado, tanto el centro nuclear hemo a 3 como el centro nuclear Cu B se oxidan; esta es la conformación de la enzima que tiene la mayor actividad. Una reducción de dos electrones inicia un cambio conformacional que permite que el oxígeno se una en el sitio activo a la enzima parcialmente reducida. Cuatro electrones se unen a la COX para reducir completamente la enzima. Su estado completamente reducido, que consiste en un Fe 2+ reducido en el citocromo a 3 grupo hemo y un centro binuclear Cu B + reducido , se considera el estado inactivo o de reposo de la enzima.
El cianuro , la azida y el monóxido de carbono se unen a la citocromo c oxidasa, inhibiendo el funcionamiento de la proteína y provocando la asfixia química de las células. Se necesitan concentraciones más altas de oxígeno molecular para compensar el aumento de las concentraciones de inhibidor, lo que conduce a una reducción general de la actividad metabólica en la célula en presencia de un inhibidor. Otros ligandos, como el óxido nítrico y el sulfuro de hidrógeno, también pueden inhibir la COX al unirse a los sitios reguladores de la enzima, lo que reduce la tasa de respiración celular.
El cianuro es un inhibidor no competitivo de la COX, que se une con alta afinidad al estado parcialmente reducido de la enzima y dificulta una mayor reducción de la enzima. En el estado pulsado, el cianuro se une lentamente, pero con alta afinidad. El ligando se coloca para estabilizar electrostáticamente ambos metales a la vez colocándose entre ellos. Una alta concentración de óxido nítrico, como la que se agrega exógenamente a la enzima, revierte la inhibición de la COX por cianuro.
El óxido nítrico puede unirse reversiblemente a cualquier ión metálico en el centro binuclear para oxidarse a nitrito. NO y CN : competirán con el oxígeno para unirse en el sitio, reduciendo la tasa de respiración celular. Endógeno NO, sin embargo, que se produce a niveles más bajos, aumenta CN - inhibición. Los niveles más altos de NO, que se correlacionan con la existencia de más enzima en el estado reducido, conducen a una mayor inhibición del cianuro. A estas concentraciones basales, se sabe que la inhibición del NO del Complejo IV tiene efectos beneficiosos, como el aumento de los niveles de oxígeno en los tejidos de los vasos sanguíneos. La incapacidad de la enzima para reducir el oxígeno al agua da como resultado una acumulación de oxígeno, que puede difundirse más profundamente en los tejidos circundantes. La inhibición del NO del Complejo IV tiene un efecto mayor a concentraciones de oxígeno más bajas, aumentando su utilidad como vasodilatador en los tejidos necesitados.
El sulfuro de hidrógeno se unirá a la COX de forma no competitiva en un sitio regulador de la enzima, similar al monóxido de carbono. El sulfuro tiene la mayor afinidad por los estados pulsados o parcialmente reducidos de la enzima y es capaz de reducir parcialmente la enzima en el centro del hemo a 3 . No está claro si H endógenos 2 niveles de S son suficientes para inhibir la enzima. No hay interacción entre el sulfuro de hidrógeno y la conformación completamente reducida de COX.
El metanol en alcoholes metilados se convierte en ácido fórmico , que también inhibe el mismo sistema oxidasa. Los niveles altos de ATP pueden inhibir alostéricamente la citocromo c oxidasa, uniéndose desde dentro de la matriz mitocondrial.
Localizaciones extramitocondriales y subcelulares
La citocromo c oxidasa tiene 3 subunidades que están codificadas por el ADN mitocondrial ( subunidad I , subunidad II y subunidad III de la citocromo c oxidasa ). De estas 3 subunidades codificadas por el ADN mitocondrial, dos se han identificado en ubicaciones extramitocondriales. En el tejido acinar pancreático , estas subunidades se encontraron en gránulos de zimógeno . Además, en la pituitaria anterior , se encontraron cantidades relativamente altas de estas subunidades en los gránulos secretores de la hormona del crecimiento . La función extramitocondrial de estas subunidades de la citocromo c oxidasa aún no se ha caracterizado. Además de las subunidades de la citocromo c oxidasa, también se ha observado la localización extramitocondrial de un gran número de otras proteínas mitocondriales. Esto plantea la posibilidad de la existencia de mecanismos específicos aún no identificados para la translocación de proteínas de las mitocondrias a otros destinos celulares.
Defectos y trastornos genéticos
Los defectos que involucran mutaciones genéticas que alteran la funcionalidad o estructura de la citocromo c oxidasa (COX) pueden resultar en trastornos metabólicos graves, a menudo fatales . Estos trastornos suelen manifestarse en la primera infancia y afectan predominantemente a tejidos con altas demandas de energía (cerebro, corazón, músculo). Entre las muchas enfermedades mitocondriales clasificadas , se cree que las que involucran un ensamblaje de COX disfuncional son las más graves.
La gran mayoría de los trastornos de la COX están relacionados con mutaciones en proteínas codificadas en el núcleo denominadas factores de ensamblaje o proteínas de ensamblaje. Estos factores de ensamblaje contribuyen a la estructura y funcionalidad de la COX, y están involucrados en varios procesos esenciales, incluida la transcripción y traducción de subunidades codificadas por mitocondrias, el procesamiento de preproteínas y la inserción de membranas, y la biosíntesis e incorporación de cofactores.
Actualmente, se han identificado mutaciones en siete factores de ensamblaje de COX: SURF1 , SCO1 , SCO2 , COX10 , COX15 , COX20 , COA5 y LRPPRC . Las mutaciones en estas proteínas pueden resultar en la alteración de la funcionalidad del ensamblaje de subcomplejos, el transporte de cobre o la regulación de la traducción. Cada mutación genética está asociada con la etiología de una enfermedad específica, y algunas tienen implicaciones en múltiples trastornos. Los trastornos que involucran el ensamblaje disfuncional de COX a través de mutaciones genéticas incluyen síndrome de Leigh , miocardiopatía , leucodistrofia , anemia y sordera neurosensorial .
Histoquímica
La mayor dependencia de las neuronas en la fosforilación oxidativa para obtener energía facilita el uso de la histoquímica de COX en el mapeo del metabolismo cerebral regional en animales, ya que establece una correlación directa y positiva entre la actividad enzimática y la actividad neuronal. Esto se puede ver en la correlación entre la cantidad y la actividad de la enzima COX, lo que indica la regulación de la COX a nivel de expresión génica. La distribución de COX es inconsistente en diferentes regiones del cerebro animal, pero su patrón de distribución es consistente entre animales. Este patrón se ha observado en el cerebro de mono, ratón y ternero. Una isoenzima de COX se ha detectado de forma constante en el análisis histoquímico del cerebro.
Tal mapeo cerebral se ha logrado en ratones mutantes espontáneos con enfermedad cerebelosa como reeler y un modelo transgénico de la enfermedad de Alzheimer . Esta técnica también se ha utilizado para mapear la actividad de aprendizaje en el cerebro animal.
Imágenes Adicionales
Ver también
- Subunidad I del citocromo c oxidasa
- Subunidad II del citocromo c oxidasa
- Subunidad III del citocromo c oxidasa
- Heme a
Referencias
enlaces externos
- La página de inicio de la citocromo oxidasa en la Universidad de Rice
- Modelo molecular interactivo de citocromo c oxidasa (Requiere MDL Chime )
- Orientación UMich de proteínas en familias de membranas / superfamilia-4
- Citocromo-c + oxidasa en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .



