Contraión - Counterion

Un contraión (pronunciado como dos palabras, es decir, "contra" "ión", ya veces escrito como dos palabras) es el ion que acompaña a una especie iónica para mantener la neutralidad eléctrica. En la sal de mesa (NaCl, también conocido como cloruro de sodio), el ion sodio (cargado positivamente) es el contraión del ion cloruro (cargado negativamente) y viceversa.
Un contraión se denominará más comúnmente anión o catión , dependiendo de si tiene carga negativa o positiva. Por tanto, el contraión de un anión será un catión y viceversa.
Química interfacial
Los contraiones son los iones móviles en los polímeros y coloides de intercambio iónico . Las resinas de intercambio iónico son polímeros con una carga neta negativa o positiva. Las resinas de intercambio catiónico consisten en un polímero aniónico con contracaciones, típicamente Na + (sodio). La resina tiene una mayor afinidad por las contracciones altamente cargadas, por ejemplo, por Ca 2+ (calcio) en el caso del ablandamiento del agua . En consecuencia, las resinas de intercambio aniónico se proporcionan típicamente en forma de cloruro Cl - , que es un couteranion muy móvil.
Los contraiones se utilizan en la catálisis de transferencia de fase . En una aplicación típica, el contracatión lipófilo, como el benzalconio, solubiliza los reactivos en disolventes orgánicos.
Química de la solución
La solubilidad de las sales en disolventes orgánicos es función tanto del catión como del anión. La solubilidad de los cationes en disolventes orgánicos se puede mejorar cuando el anión es lipófilo. De forma similar, la solubilidad de los aniones en disolventes orgánicos se mejora con cationes lipofílicos. Los cationes lipofílicos más comunes son los cationes de amonio cuaternario , llamados "sales quat".
- Contraaniones lipofílicos
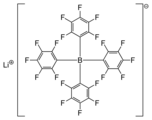
El tetraquis (pentafluorofenil) borato de litio es la sal de litio de un anión tetraarilborato altamente lipofílico, a menudo denominado anión débilmente coordinado .
El tetrafenilborato es menos lipofílico que el derivado perfluorado, pero se usa ampliamente como agente precipitante.
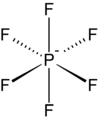
El hexafluorofosfato es un anión de coordinación débil común .
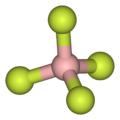
Como lo ilustra el tetrafluoroborato de contraanión pequeño ( BF -
4 ), los cationes lipofílicos tienden a ser simétricos y cargados individualmente.
- Contracciones lipofílicas
El cloruro de bis (trifenilfosfina) iminio es la sal de cloruro de un catión fosfonio lipófilo voluminoso [Ph 3 PNPPh 3 ] + .
El cloruro de tetrafenilfosfonio (C 6 H 5 ) 4 PCl, abreviado Ph 4 PCl o PPh 4 Cl es el cloruro de un catión de fosfonio simétrico que se utiliza a menudo en química organometálica . La sal de arsonio también es bien conocida.
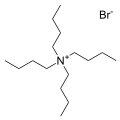
La sal de bromuro de tetrabutilamonio , uno de los contracationes más comunes. Se conocen muchas "sales de quat" análogas.
Los cationes de metales alcalinos unidos por éteres corona son contracaciones lipofílicas comunes, como lo ilustra [Li (12-corona-4) 2 ] + .
Muchos complejos organometálicos catiónicos se aíslan con contraiones inertes no coordinantes. El tetrafluoroborato de ferrocenio es uno de esos ejemplos.
Electroquímica
Para lograr una alta conductividad iónica, las mediciones electroquímicas se realizan en presencia de un exceso de electrolito. En el agua, el electrolito suele ser una sal simple, como el cloruro de potasio . Para las mediciones en soluciones no acuosas, se emplean sales compuestas tanto de cationes lipofílicos como de aniones, por ejemplo, hexafluorofosfato de tetrabutilamonio . Incluso en tales casos, los potenciales se ven influidos por el apareamiento de iones , efecto que se acentúa en los disolventes de baja constante dieléctrica .
Estabilidad de contraiones
Para muchas aplicaciones, el contraión simplemente proporciona carga y lipofilicidad que permite la manipulación de su ion asociado. Se espera que el contraión sea químicamente inerte. Para los contraaniones, la inercia se expresa en términos de basicidad de Lewis baja . Los contraiones son idealmente resistentes y no reactivos. Para las contracciones de amonio cuaternario y fosfonio, la inercia está relacionada con su resistencia a la degradación por bases fuertes y nucleófilos fuertes.