Barrera hematoencefálica - Blood–brain barrier
| Barrera hematoencefálica | |
|---|---|
 Permeabilidad de solutos en el BBB
frente al plexo coroideo | |
| Detalles | |
| Sistema | Sistema neuroinmune |
| Identificadores | |
| Acrónimo (s) | BBB |
| Malla | D001812 |
| Terminología anatómica | |
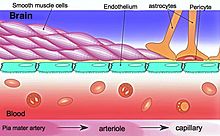
La barrera hematoencefálica ( BHE ) es un borde semipermeable altamente selectivo de células endoteliales que evita que los solutos en la sangre circulante crucen de forma no selectiva al líquido extracelular del sistema nervioso central donde residen las neuronas . La sangre cerebro barrera está formada por las células endoteliales de la pared capilar , astrocitos finales pies ensheathing el capilar, y pericitos incrustados en el capilar de la membrana basal . Este sistema permite el paso de algunas moléculas pequeñas por difusión pasiva , así como el transporte selectivo y activo de diversos nutrientes, iones, aniones orgánicos y macromoléculas como glucosa y aminoácidos que son cruciales para la función neural.
La barrera hematoencefálica restringe el paso de patógenos , la difusión de solutos en la sangre y moléculas grandes o hidrófilas en el líquido cefalorraquídeo , al tiempo que permite la difusión de moléculas hidrófobas (O 2 , CO 2 , hormonas) y pequeñas no polares. moléculas. Las células de la barrera transportan activamente productos metabólicos como la glucosa a través de la barrera utilizando proteínas de transporte específicas . La barrera también restringe el paso de factores inmunes periféricos, como moléculas de señalización, anticuerpos y células inmunes, al SNC, aislando así al cerebro del daño debido a eventos inmunes periféricos.
Las estructuras cerebrales especializadas que participan en la integración sensorial y secretora dentro de los circuitos neuronales del cerebro —los órganos circunventriculares y el plexo coroideo— tienen, en contraste, capilares altamente permeables.
Estructura

El BBB resulta de la selectividad de las uniones estrechas entre las células endoteliales de los capilares cerebrales, lo que restringe el paso de solutos. En la interfaz entre la sangre y el cerebro, las células endoteliales están unidas continuamente por estas uniones estrechas, que están compuestas por subunidades más pequeñas de proteínas transmembrana , como ocludina , claudinas (como Claudin-5 ), molécula de adhesión de la unión (como JAM- A). Cada una de estas proteínas de unión estrecha se estabiliza en la membrana de la célula endotelial por otro complejo proteico que incluye proteínas de andamiaje como la proteína de unión estrecha 1 (ZO1) y proteínas asociadas.
La BHE está compuesta por células endoteliales que restringen el paso de sustancias de la sangre de forma más selectiva que las células endoteliales de los capilares en otras partes del cuerpo. Las proyecciones de células de astrocitos llamadas pies astrocíticos (también conocidas como " glia limitans ") rodean las células endoteliales de la BHE, proporcionando apoyo bioquímico a esas células. La BHE es distinta de la barrera sangre-líquido cefalorraquídeo bastante similar , que es una función de las células coroideas del plexo coroideo , y de la barrera hemato-retiniana , que puede considerarse parte de todo el ámbito de tales barreras.
No todos los vasos del cerebro humano exhiben propiedades BBB. Algunos ejemplos de esto incluyen los órganos circunventriculares , el techo del tercer y cuarto ventrículos , los capilares de la glándula pineal en el techo del diencéfalo y la glándula pineal . La glándula pineal secreta la hormona melatonina "directamente en la circulación sistémica", por lo que la melatonina no se ve afectada por la barrera hematoencefálica.
Desarrollo
La BBB parece ser funcional en el momento del nacimiento. La glicoproteína P , un transportador , ya existe en el endotelio embrionario.
La medición de la captación cerebral de varios solutos transmitidos por la sangre mostró que las células endoteliales del recién nacido eran funcionalmente similares a las de los adultos, lo que indica que una BHE selectiva está operativa al nacer.
En ratones, la pérdida de Claudin-5 durante el desarrollo es letal y da como resultado un aflojamiento selectivo del tamaño de la BBB.
Función
La barrera hematoencefálica actúa eficazmente para proteger al cerebro de los patógenos circulantes . En consecuencia, las infecciones cerebrales transmitidas por la sangre son raras. Las infecciones del cerebro que ocurren a menudo son difíciles de tratar. Los anticuerpos son demasiado grandes para cruzar la barrera hematoencefálica y solo ciertos antibióticos pueden pasar. En algunos casos, un fármaco debe administrarse directamente en el líquido cefalorraquídeo, donde puede ingresar al cerebro cruzando la barrera sangre-líquido cefalorraquídeo .
La barrera hematoencefálica puede tener fugas en determinadas enfermedades neurológicas , como la esclerosis lateral amiotrófica , la epilepsia , el traumatismo cerebral y el edema, y en enfermedades sistémicas , como la insuficiencia hepática . La barrera hematoencefálica se vuelve más permeable durante la inflamación , lo que potencialmente permite que los antibióticos y los fagocitos se muevan a través de la BHE.
Órganos circunventriculares
Los órganos circunventriculares (CVO) son estructuras individuales ubicadas adyacentes al cuarto ventrículo o al tercer ventrículo en el cerebro, y se caracterizan por densos lechos capilares con células endoteliales permeables a diferencia de los de la barrera hematoencefálica. Incluidos entre CVOs que tienen capilares altamente permeables son el área postrema , órgano subfornical , órgano vascular de las lámina terminal , eminencia media , glándula pineal , y tres lóbulos de la glándula pituitaria .
Los capilares permeables de los CVO sensoriales (área postrema, órgano subfornical, órgano vascular de la lámina terminal) permiten la detección rápida de señales circulantes en la sangre sistémica, mientras que los de los CVO secretores (eminencia media, glándula pineal, lóbulos pituitarios) facilitan el transporte del cerebro -Señales derivadas a la sangre circulante. En consecuencia, los capilares permeables al CVO son el punto de comunicación bidireccional sangre-cerebro para la función neuroendocrina .
Zonas permeables especializadas
Las zonas fronterizas entre el tejido cerebral "detrás" de la barrera hematoencefálica y las zonas "abiertas" a las señales sanguíneas en ciertos CVO contienen capilares híbridos especializados que tienen más fugas que los capilares cerebrales típicos, pero no tan permeables como los capilares CVO. Estas zonas existen en el límite del área postrema, núcleo tractus solitarii (NTS), y eminencia media, núcleo arqueado hipotalámico . Estas zonas parecen funcionar como regiones de tránsito rápido para las estructuras cerebrales involucradas en diversos circuitos neuronales, como el NTS y el núcleo arqueado, para recibir señales sanguíneas que luego se transmiten a la salida neuronal. La zona capilar permeable compartida entre la eminencia media y el núcleo arqueado hipotalámico aumenta con espacios pericapilares amplios, lo que facilita el flujo bidireccional de solutos entre las dos estructuras e indica que la eminencia media no es solo un órgano secretor, sino que también puede ser un órgano sensorial. .
Investigación terapéutica
Como objetivo de las drogas
La barrera hematoencefálica está formada por el endotelio capilar cerebral y excluye del cerebro el 100% de los neuroterapéuticos de moléculas grandes y más del 98% de todos los fármacos de moléculas pequeñas. Superar la dificultad de administrar agentes terapéuticos a regiones específicas del cerebro presenta un desafío importante para el tratamiento de la mayoría de los trastornos cerebrales. En su función neuroprotectora, la barrera hematoencefálica funciona para dificultar la administración de muchos agentes diagnósticos y terapéuticos potencialmente importantes al cerebro. Las moléculas terapéuticas y los anticuerpos que de otro modo podrían ser eficaces en el diagnóstico y la terapia no atraviesan la BHE en cantidades adecuadas para ser clínicamente eficaces.
Los mecanismos para el direccionamiento de fármacos en el cerebro implican pasar "a través" o "detrás" de la BHE. Las modalidades de administración de fármacos al cerebro en dosis unitarias a través de la BHE implican su disrupción por medios osmóticos , o bioquímicamente mediante el uso de sustancias vasoactivas, como la bradicinina , o incluso por exposición localizada a ultrasonido focalizado de alta intensidad (HIFU) .
Otros métodos utilizados para atravesar la BHE pueden implicar el uso de sistemas de transporte endógenos, incluidos los transportadores mediados por portadores, como los portadores de glucosa y aminoácidos, la transcitosis mediada por receptores para insulina o transferrina y el bloqueo de transportadores de salida activos como p -glicoproteína . Algunos estudios han demostrado que los vectores que se dirigen a los transportadores de BBB, como el receptor de transferrina , permanecen atrapados en las células endoteliales cerebrales de los capilares, en lugar de ser transportados a través de la BBB al área objetivo.
Nanopartículas
La nanotecnología se encuentra bajo investigación preliminar por su potencial para facilitar la transferencia de medicamentos a través de la BBB. Las células endoteliales capilares y los pericitos asociados pueden ser anormales en los tumores y es posible que la barrera hematoencefálica no siempre esté intacta en los tumores cerebrales. Otros factores, como los astrocitos , pueden contribuir a la resistencia de los tumores cerebrales a la terapia con nanopartículas. Las moléculas liposolubles de menos de 400 Daltons de peso pueden difundirse libremente más allá de la BBB a través de la difusión pasiva mediada por lípidos .
Historia
Paul Ehrlich era un bacteriólogo que estudiaba la tinción , un procedimiento que se utiliza en muchos estudios de microscopía para hacer visibles estructuras biológicas finas utilizando tintes químicos. Cuando Ehrlich inyectó algunos de estos tintes (en particular, los tintes de anilina que entonces se usaban ampliamente), el tinte tiñó todos los órganos de algunos tipos de animales excepto sus cerebros . En ese momento, Ehrlich atribuyó esta falta de tinción a que el cerebro simplemente no captaba tanto tinte.
Sin embargo, en un experimento posterior en 1913, Edwin Goldmann (uno de los estudiantes de Ehrlich) inyectó el tinte directamente en los fluidos cerebroespinales de los cerebros de los animales. Entonces descubrió que los cerebros se tiñeron, pero el resto del cuerpo no, lo que demuestra la existencia de una compartimentación entre los dos. En ese momento, se pensó que los propios vasos sanguíneos eran los responsables de la barrera, ya que no se podía encontrar una membrana obvia. El concepto de barrera hematoencefálica (entonces denominada barrera hematoencefálica ) fue propuesto por un médico de Berlín, Lewandowsky, en 1900.
Ver también
- Barrera sangre-aire : membrana que separa el aire alveolar de la sangre en los capilares pulmonares
- Barrera hemato -ocular: barrera física entre los vasos sanguíneos locales y la mayor parte del ojo.
- Barrera hemato -retiniana : parte de la barrera hemato-ocular que evita que ciertas sustancias entren en la retina.
- Barrera hemato -testicular: barrera física entre los vasos sanguíneos y los túbulos seminíferos de los testículos de los animales.
- Barrera sangre-timo : barrera formada por los capilares sanguíneos continuos en la corteza tímica